Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
Crackinh isobutan có thể sinh ra các sản phẩm theo hướng sau:
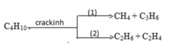
Hỗn hợp khí sau phản ứng crackinh dẫn qua dung dịch brom thì brom mất màu hoàn toàn
=> khí đi qua khỏi bình brom gồ ankan và có thể còn anken dư.
Ta có: Mtb khí = 44.0,5 = 22 > MCH4 = 16
=> anken còn dư sau khi ra khỏi bình brom
Vậy: MCH4 = 16 < Mtb khí < M anken => phản ứng crackinh xảy ra theo hướng (1)
Ta có: nC3H6 phản ứng = nBr2 = 11,2/160 = 0,07 mol
nhh khí = 2,912/22,4 = 0,13 mol => m hh khí = nhh khí .M(tb) hh khí = 0,13.22 = 2,86 (g)
Áp dụng định luật bảo toàn khối lượng ta có:
mC4H10 = mhhA = mC3H6 phản ứng + mhh khí = 0,07.42 + 2,86 = 5,8(g)

Đáp án C
Craking isobutan có thể sinh ra các hướng sau:
![]() (1)
(1)
hoặc ![]() (2)
(2)
Hỗn hợp khí A sau khi qua dung dịch brom thì brom mất màu hoàn toàn. Do đó khí đi ra khỏi bình brom gồm ankan và có thể còn anken dư.
Ta có:
![]()
Suy ra anken còn dư sau khi ra khỏi bình brom
Vậy: ![]()
phản ứng crakinh xảy ra theo hướng (1)
Ta có: ![]()
Khối lượng hỗn hợp khí thoát ra khỏi bình brom là:
mkhí thoát ra = 0,13.44.0,5 = 2,86 (g)
Áp dụng định luật bảo toàn khối lượng:
mC4H10=m hhA=m C3H6 phản ứng+ m khí thoát ra
=5,8 g

\(CH_3CH\left(CH_3\right)CH_3\underrightarrow{cracking}A\left\{{}\begin{matrix}C_3H_6\\CH_4\end{matrix}\right.\)
Ta có: \(n_{C_3H_6\left(pư\right)}=n_{Br_2}=\dfrac{11,2}{160}=0,07\left(mol\right)\)
- Khí thoát ra khỏi bình Br2 gồm: CH4 và C3H6 dư.
Gọi: \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_3H_6}=y\left(mol\right)\end{matrix}\right.\) \(\Rightarrow x+y=\dfrac{2,912}{22,4}=0,13\left(1\right)\)
Mà: tỉ khối hơi của khí so với CO2 là 0,5
\(\Rightarrow\dfrac{16x+42y}{x+y}=0,5.44\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{C_3H_6}=0,07+0,03=0,1\left(mol\right)\)
\(\Rightarrow m=m_{C_3H_6}+m_{CH_4}=0,1.42+0,1.16=5,8\left(g\right)\)

Ta thấy trong X có các ancol có đặc điểm: số C = số nhóm OH
=> Khi đốt cháy X : \(n_{CO_2}=n_{C\left(X\right)}=n_{OH}=0,25mol\)
=> Khi phản ứng vớ Na => \(n_{H_2}=\frac{1}{2}n_{OH}=0,125mol\)
=> V = 2,8 lít

Ta có: \(n_{COOH\left(X\right)}=n_{CO_2}=0,7mol\)
Khi đốt X có: \(n_{CO_2}=0,4mol;n_{CO_2}=0,8mol\)
Theo ĐLBT oxi có \(n_O=2n_{COOH\left(X\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=y=0,6mol\)

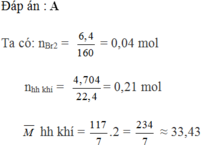
Khi dẫn hỗn hợp A gồm các hidrocacbon qua dung dịch brom, brom bị mất màu hết => anken trong hỗn hợp A có thể còn dư.
Ta thấy: hh khí = 33,43 < MC3H6 = 42
=> khí đi ra khỏi dung dịch brom có C3H6 => nC3H6 phản ứng = nBr2 = 0,04 mol
Áp dụng định luật bảo toàn khối lượng ta có:
mC4H10 = mC3H6 phản ứng + mhh khí = 0,04.42 + 0,221.234/7 = 8,7 (g)

104,48gam104,48gam
Giải thích các bước giải:
Sơ đồ phản ứng:
⎧⎪ ⎪ ⎪⎨⎪ ⎪ ⎪⎩AlMgFeOFe3O4+HNO3−−−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩NO,N2OH2O⎧⎪⎨⎪⎩Al(NO3)2Mg(NO3)2Fe(NO3)2to→⎧⎨⎩Al2O3MgOFe2O3+NO2+O2{AlMgFeOFe3O4→+HNO3{NO,N2OH2O{Al(NO3)2Mg(NO3)2Fe(NO3)2→to{Al2O3MgOFe2O3+NO2+O2
Oxi chiếm 20,22%20,22% khối lượng hỗn hợp.
mO=25,32%.25,32=5,12gammO=25,32%.25,32=5,12gam
→nO=0,32mol→nO=0,32mol
Gọi số mol của NONO và N2ON2O lần lượt là xx và yy mol
⎧⎨⎩x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02{x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02
Quy đổi hỗn hợp X thành các nguyên tố: Al,Mg,Fe,OAl,Mg,Fe,O
→mKl=25,32−5,12=20,2g→mKl=25,32−5,12=20,2g
→mO(cr)=30,92−20,2=10,72gam→mO(cr)=30,92−20,2=10,72gam
→nO=0,67mol→nO=0,67mol
3nAl+3nFe+2nMg=2nO(cr)3nAl+3nFe+2nMg=2nO(cr)
Gọi số mol của NH4NO3NH4NO3 là xx mol
Bảo toàn e:
3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O
0,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.80,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.8
→nNH4NO3=0,015mol→nNH4NO3=0,015mol
Khối lượng muối:
m=mKl+mNO−3+mNH4NO3m=mKl+mNO3−+mNH4NO3
=20,2+0,67.2.62+0,015.80=104,48gam

nH+=0,4+0,1.a
nNO3-=0,1a
bạn viết phương trình Mg+H+ +NO3- dưới dạng pt ion
H++NO3 ttuowng đương với HNO3 loãng
rồi bạn sử dụng phương pháp đường chéo, định luật bảo toàn nguyên tố và electron
Đáp án C
Crackinh m gam (CH3)3CH
→ hhX gồm CH4 và CH2=CH-CH3.
hhX + 0,07 mol Br2 thì dd Br2 mất màu hoàn toàn
→ nCH2=CH-CH3 phản ứng = 0,07 mol.
Có 0,13 mol hh CH4 và CH2=CH-CH3 dư thoát ra có d/CO2 = 0,5.
• Theo BTKL: m = mCH2=CH-CH3phản ứng + mhh khí thoát ra
= 0,07 x 42 + 0,5 x 44 x 0,13 = 5,8 gam