Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

H2SO4 + nSO3 => H2SO4.nSO3
H2SO4.nSO3 + nH2O >> n+1H2SO4
H2SO4 + 2NaOH >> Na2SO4 + 2H2O
Số mol NaOH = 0,008 , số mol H2SO4 200ml = 0,008/2 . 200/10 =0,08
Theo (2) nH2SO4.nSO3 =0,08/n+1
MH2SO4.nSO3 =98 +80n = 6,76/0,08/n+1 =84,5n+ 84,5
13,5 =4,5n
=>n=3
%SO3=3.80/2.80+98 =71%
c,Theo câu b , hàm lượng % của SO3 có trong oleum trên là 71
Cứ 100g oleum có 71g SO3 và 29g H2SO4 Khi đó mdd = 1,31.100 = 131g
a g có 71a/100 ...............29a/100
Vì dd H2SO4 có C=40%
Cứ 100g dd có 40g H2SO4 và 60g H2O
=>131g >> 131.40/100 = 52,4g H2SO4 và 131.60/100 = 78,6 g H2O
Khi cho oleum vào dd H2SO4 thì SO3+H2O
SO3 + H2O >> H2SO4
Cứ 80g cần 18g >> 98g
Vậy ..x..g cần 78,6g >>..y..g
x= 78,6.80/18 = 349,3g
y= 78,6.98/18 = 427,9g
Trong loại oleum mới 10% thì mSO3 = 71a/100 -349,3g
và mH2SO4 = 29a/100 +52,4+ 427,9
=> 71a/100 -349,4 / 29a/100 +480,3 = 10/90
=> Bạn ấn máy tìm a nhé

n HCl = 0,8.1,5 = 1,2(mol)
n HCl dư = n NaOH = 0,2.1 = 0,2(mol)
=> n HCl pư = 1,2 - 0,2 = 1(mol)
$2H^+ + O^{2-} \to H_2O$
n O(oxit) = 1/2 n HCl = 0,5(mol)
m Fe + m O = m oxit
=> n Fe = (29 - 0,5.16)/56 = 0,375(mol)
Ta có :
n Fe / n O = 0,375 / 0,5 = 3 / 4 nên oxit là Fe3O4

Câu 2 :
$n_{HCl} = 0,2.1 + 0,3.1,5 = 0,65(mol)$
$V_{dd} = 0,2 + 0,3 = 0,5(mol)$
$C_{M_{HCl}} = \dfrac{0,65}{0,5} =1,3M$
Câu 3 :
Gọi $m_{H_2O\ cần\ thêm} =a (gam)$
Sau khi thêm :
$m_{NaOH} = 100.35\% = 35(gam)$
$m_{dd} = 100 + a(gam)$
Suy ra: $\dfrac{35}{100 + a}.100\% = 20\%$
Suy ra: a = 75(gam)
Câu 4 :
Gọi $V_{dd\ HCl\ 2M} =a (lít) ; V_{dd\ HCl\ 3M} = b(lít)$
Ta có :
$a + b = 4$
$2a + 3b = 4.2,75$
Suy ra a = 1(lít) ; b = 3(lít)

PTHH : HCl+NaOH-----> NaCl +H2O
................0,3...0,3(mol)
\(C_{M\left(NaOH\right)}=\frac{0,3}{0,1}=3\left(M\right)\)
#Walker

Đầu bài cho oxit kim loại tác dụng với 300 ml dd x thôi mà, trong khi 1,2 mol HCl lại là số mol có trong 500 ml dd.
Tuy vậy thì tính theo 300 ml cũng ko ra. :vv

Đáp án D
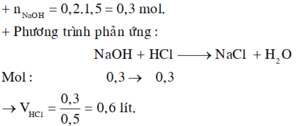
nNaOH = 0,2.1,5=0,3 (mol)
NaOH + HCl → NaCl + H2O
0,3 → 0,3 (mol)
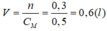

HCl+NaOH => NaCl+\(H_2O\)
\(n_{NaOH}=C_M.V=0,3.0,2=0,06\) (mol)
=> \(n_{HCl}=n_{NaOH}=0,06\) (mol)
=> \(V_{HCl}=\dfrac{n}{C_M}=\dfrac{0,06}{0,4}=0,15\)(l)=150(ml)
=> C