Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Trong các đơn chất halogen, chất điều kiện thường ở trạng thái rắn là I 2 .
Chọn đáp án D.

ãy chỉ ra mệnh đề không chính xác:
A. Tác cả muối AgX (X là halogen) đều ko tan trg nc
B. Tất cả các hidro halogenua đều tồn tại ở thể khí, điều kiện thường
C. Tất cả các hidro halogenua khi tan vào nc đều cho dd axit
D. Các halogen (từ F2 đến I2) td trực tiếp vs hầu hết các kim loại

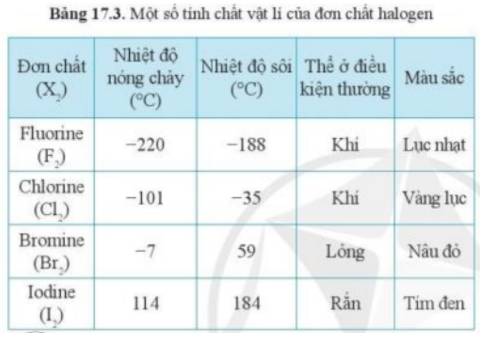
- Theo bảng 17.3, xu hướng biến đổi trạng thái của các halogen ở điều kiện thường từ: khí → lỏng → rắn
- Mà astatine đứng dưới cùng trong nhóm halogen
=> Astatine tồn tại ở thể rắn trong điều kiện thường
- Giải thích: Do sự tăng khối lượng phân tử và sự tăng tương tác van dể Waals

Chọn đáp án C
1. Bán kính của S lớn hơn bán kính F. Chuẩn
2. Tính khử và tính oxi hóa của HBr đều mạnh hơn HF. Sai tính oxh của HF max
3. Có 2 HX ( X: halogen ) có thể điều chế bằng cách cho NaX tác dụng với dung dịch H2SO4 đậm đặc.
Chuẩn đó là HCl và HF (HI và HBr không điều chế được vì phản ứng với H2SO4 đậm đặc)
4. Tính khử của I- mạnh hơn F-. Chuẩn
5. Trong công nghiệp, người ta không sản xuất các khí SO2, H2S.Chuẩn
6. Tất cả các halogen đều không có ở dạng đơn chất trong thiên nhiên. Chuẩn
7. Để thu được dung dịch H2SO4, trong công nghiệp, người ta cho nước vào oleum
Sai.Phải cho ngươc lại (oleum vào nước)

- Quan sát Bảng 17.3, nhận thấy trong điều kiện thường có Iodine (I2) là ở thể rắn
- Giải thích:
+ Khối lượng phân tử cao
+ Lực tương tác van der Waals giữa phân tử iodine mạnh
Hầu hết các halogen đều là chất khí ở điều kiện thường trừ :
Br2 dạng lỏng ; I2 dạng rắn
Ý kiến này sai.