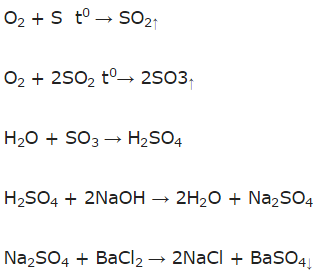Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

ch4 và so2.
theo đề Mmox=32x,MRhy=4y--->32X=16Y--->2X=Y.hợp chất dạng mox có Xmax=3(so3)kẻ bảng cho x chạy từ 1 đến 3 thì có X=2 thì tòm ra được là so2(64=32*2)---.y=4-->ch4
cách giải này khó hiểu lắm ... các bn nếu có cách khác dễ hiểu hơn thì đăng lên dùm![]()

pư tạo khí H2 : Fe+ 2Hcl-------------------> FeCl2 + H2
0,05<------------------------------------0,05mol
FexOy+ Hcl------------------------------> xFeCl2y/x+ h20
11,6/(56x+16y)------------------------>11,6x/(56x+16y)
=> mFe=0,05.56=2,8g=>%=...........................=> mFexOy=11,6g=>%
b. Fe(2+) + 2 Oh- ---------------------> Fe(oh)2
0,05-----------------------------------------0,05
Fe(2y/x) + 2y/xOH ------------------------------------> Fe(Oh)2y/x
11,6x/(56x+16y)----------------------------------------------------------->11,6x/(56x+16y)
nung trong kk 2(Fe(oh)2;Fe(oh)2y/x)------------------> Fe2O3
0,2mol ---------------------------- 0,1 mol
<=> (0,05+11,6x/(56x+16y) )=0,2 => x/y=3/4
vậy là Fe3O4

a. PTHH: \(2SO_2+O_2\rightarrow^{t^o}_{V_2O_5}2SO_3\) (đoạn này Latex OLM đánh nhiều hơi rối nên không hiểu thì hỏi nhé)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(300ml=0,3l\)
\(\rightarrow n_{H_2SO_4}=1.0,3=0,3mol\)
Theo phương trình \(n_{O_2}=n_{SO_3}=n_{H_2SO_4}=0,3mol\)
\(\rightarrow m_{SO_2}=64.0,3=19,2g\)
b. PTHH: \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
\(n_{Al_2O_3}=\frac{15,3}{102}=0,15mol\)
Xét tỉ lệ \(n_{Al_2O_3}>\frac{n_{H_2SO_4}}{3}\)
Vậy \(Al_2O_3\) dư
Theo phương trình \(n_{Al_2\left(SO_4\right)_3}=\frac{1}{3}n_{H_2SO_4}=0,1mol\)
\(\rightarrow C_{M_{Al_2\left(SO_4\right)_3}}=\frac{0,1}{0,3}=0,33M\)

Al+NaOH+H2O---> NaAlO2+3/2H2
0,2 <---- 0,3
---> nCu=0,15mol
BTe: 3nAl+2nCu=3nNO
nNO=0,3
Al+NaOH+H2O---> NaAlO2+3/2H2
0,2 <---- 0,3
---> nCu=0,15mol
BTe: 3nAl+2nCu=3nNO
nNO=0,3

Giải
a) Các phương trình hóa học
CuCl2 (dd) + 2NaOH (dd) → Cu(OH)2 (r) + 2NaCl (dd) (1)
Cu(OH)2 (r) →t0 CuO (r) + H2O (h) (2)
b) Khối lượng CuO thu được sau khi nung:
Số mol NaOH đã dùng : nNaOH = 20/40=0,5 (mol).
Số mol NaOH đã tham gia phản ứng :
nNaOH = 2nCuCl2 =0,2.2 = 0,4 (mol).
Vậy NaOH đã dùng là dư. Số mol CuO sinh ra sau khi nung :
+ Theo ( 1 ) và (2)
nCuO = nCu(OH)2 = nCuCl2 = 0,2 mol
+ Khối lượng CuO thu được : mCuO = 80.0,2 = 16 (g)
c) Khối lượng các chất tan trong nước lọc:
Khối lượng NaOH dư :
+ Số mol NaOH trong dd : nNaOH = 0,5 -0,4 =0,1 (mol)
+ Có khối lượng là : mNaOH = 40.0,1 = 4 (g).
Khối lượng NaCl trong nước lọc :
+ Theo (1), số mol NaCl sinh ra là : nNaCl = 2nCuCl2 = 20.0,2 = 0,4 (mol).
+ Có khối lượng là : mNaCl = 58,5.0,4 = 23,4 (g).

Câu C đúng
Fe + CuSO4 -------- > FeSO4 + Cu
Khi cho đinh sắt vào dung dịch CuSO4 , đinh sắt bị hòa tan , kim loại đồng bám ngoài đinh sắt, dung dịch CuSO4 tham gia phản ứng ( tạo nên Fe SO4) nên màu xanh của dung dịch ban đầu bị nhạt dần.
Câu c đúng.
Fe + CuSO4 → FeSO4 + Cu
Khi cho đinh sắt vào dung dịch CuSO4, đinh sắt bị hòa tan, kim loại đồng sinh ra bám ngoài đinh sắt, dung dịch CuSO4 tham gia phản ứng (tạo thành FeSO4) nên màu xanh của dung dịch ban đầu sẽ bị nhạt dần.
(Lưu ý: Kim loại mạnh đẩy kim loại yếu ra khỏi dung dịch muối của chúng)

Phương trình hóa học:
a) H2 + F2 → 2HF (k)
b) S + O2 → SO2(to)
c) Fe + S → FeS (to).
d) C + O2 → CO2(to).
e) H2 + S → H2S.(to)

a) Sơ đồ phản ứng:
S → SO2 → SO3 → H2SO4 → Na2SO4 → BaSO4.
b) Phương trình phản ứng:

(1) 2naoh + co2 -> na2co3 + h2o
(2) na2co3 + co2 + h2o -> 2nahco3
nCo2 = v/22.4 = 16.8/22.4=0.75 mol
600ml=0.6 l
=> nNaoh=n.cM=0.6. 2 =1.2 mol
lập tỉ lệ ta có
nNaoh/nCo2=1.2/0.6=2
=> xảy ra phương trình 1 không xảy ra phương trình 2
theo phương trình 1
nNa2co3=nCo2=0.6 mol
=> mNa2co3=n.M=0.6106=63.6g
(3) bacl2 + na2co3 -> baco3 + 2nacl
theo phương trình 3
nBaco3=nNa2co3=0.6 mol
=>mBaco3= n.M=0.6 .197=118.2g