Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt nA = x, nB = y.
Xét phản ứng 2, nCl- = 0,6 mol => nNO3- = 0,6 mol
Ta có 6m + 1,32 = 0,6.62 => m = 5,76
=> 2a + 3b = 0,6 mol
MA . x + MB . y = 5,76
Thử 4 đáp án => Mg và Al
=> Đáp án A

Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.

Đáp án D
n h h k h i = 0 , 2 m o l
cho BaCl2 vào kết tủa thu được là BaSO4
n B a S O 4 = 0 , 605 m o l
n H 2 S O 4 = 0 , 605 m o l
n N a O H = 1 , 085 m o l
n N H 3 = 0 , 025 m o l
⇒ n i o n k i m l o a i = 1 , 06 m o l
hỗn hợp khí có chứa H2 nên muối sắt là muối Fe2+
NO3- hết, các muối trung hòa là
MgSO4, FeSO4, K2SO4 và (NH4)2SO4
m F e + m M g = 24,88 gam (1)
nđiện tích - = 2nSO42-= 1,21 mol
nđiện tích += 1,085 + n K +
=> n K + = 0,125 mol
=>nN khí = 0,125 – 0,025 =0,1 mol
Mặt khác bảo toàn khối lượng
m X + m H 2 S O 4 + m K N O 3 = m m u ố i + m k h í + m H 2 O
=> m H 2 O = 8,91 mol
=> n H 2 O = 0,495 mol
Bảo toàn nguyên tố H có
nH axit = nH ( H 2 O )+ nH ( H 2 ) +nH muối amoni
0,605.2 =0,495.2 +2 n H 2 + 0,025.4
=> n H 2 = 0,06 mol
=> n C O 2 = 0,2 – 0,1 – 0,06 = 0,04 mol
=> n F e C O 3 = 0,04 mol
=> mFe + mMg + m F e 3 O 4 = 26,48 g
m KL (hỗn hợp trên)= 22,64 gam (2)
từ (1) và (2) => mO ( F e 3 O 4 )= 3,84 gam
=> n F e 3 O 4 =0,06 mol
mặt khác vì tổng ion dương kim loại F e 2 + v à M g 2 +
Gọi n F e = a m o l , n M g = b m o l
⇒ 2 a + 2 b = 0 , 2 56 a + 24 b = 12 , 56
⇒ a = 0 , 16 , b = 0 , 15 m o l

Chọn đáp án C
![]()
||► Thu được rắn X ⇒ muối dư, H2SO4 hết.
⇒ nH2SO4 = nH2O = nCO2 = 0,2 mol. Bảo toàn khối lượng:
mX = 115,3 + 0,2 × 98 - 0,2 × 44 - 0,2 × 18 - 12 = 110,5(g).
Bảo toàn khối lượng: mZ = 110,5 - 0,5 × 44 = 88,5(g).

Chọn đáp án A
BTNT.H Þ nH trong M = 0,26x2 = 0,52
Đặt ancol T là R'(OH)n Þ nT = 0,035x2/n = 0,07/n và mT = 2,17 + 0,035x2 = 2,24
Þ MT = R' + 17n = 2,24/(0,07/n) = 32n Þ n = 1 và R' = 15 phù hợp Þ T là CH3OH (0,07 mol)
Đề bài không nói este mạch hở Þ Khả năng cao có este của phenol
Đặt nNaOH phản ứng = a Þ nH2O (từ phenol) = (a - 0,07)/2 = 0,5a - 0,035 = nEste phenol
BTNT.Na Þ nNa2CO3 = 0,5a; BTNT.C Þ nC trong M = 0,415 + 0,5a + 0,07 = 0,485 + 0,5anO trong M = 2nX + 2nY = 0,07x2 + 2x(0,5a - 0,035) = a + 0,07Þ 10,32 = 12x(0,485 + 0,5a) + 0,52 + 16x(a + 0,07) Þ a = 0,13 Þ Đúng thật là có este phenol
Chọn X là este của ancol thường, Y là este có gốc phenol Þ Cx> 2, CY > 7
Biện luận nghiệm nguyên: 0,07CX + 0,03CY = 0,485 + 0,5x0,13 + 0,07 Þ CX = 4, CY = 9
Biện luận nghiệm nguyên: 0,07HX + 0,03HY = 0,26x2 Þ HX = 4, HY = 8
Þ Công thức các este là: HCºC-COOCH3 (0,07) và H2C=CH-COOC6H5 (0,03)
Þ mC2H3COONa = 0,03x94 = 2,82.

Đáp án B
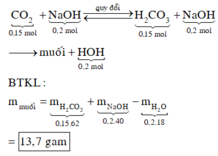
+ C O 2 ⏟ 0 , 15 m o l + N a O H ⏟ 0 , 2 m o l → q u y đ ổ i H 2 C O 3 ⏟ 0 , 15 m o l + N a O H ⏟ 0 , 2 m o l → m u ố i + H O H ⏟ 0 , 2 m o l B T K L : m m u ố i = m H 2 C O 3 ⏟ 0 , 15 . 62 + m N a O H ⏟ 0 , 2 . 40 - m H 2 O ⏟ 0 , 2 . 18 = 13 , 7 g a m ∙ P S : n H + / H 2 C O 3 > n O H - ⇒ n H O H = n O H - .
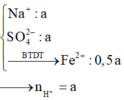
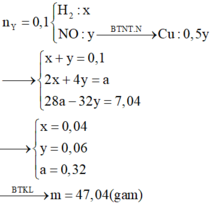
ĐÁP ÁN D
Tổng quát : MBr -> MCl
Mol x -> x
=> mtrước – msau = (80 – 35,5)x = 4,45g => x = 0,1 mol
=> nCl2 = ½ nMCl = 0,05 mol
=> VCl2 = 1,12 lit