Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- H: ô số 1, nhóm IA, chu kì 1
- C: ô số 6, nhóm IVA, chu kì 2
- N: ô số 7, nhóm VA, chu kì 2
- O: ô số 8, nhóm VIA, chu kì 2
- Trong cùng 1 chu kì, theo chiều tăng dần điện tích hạt nhân, tính phi kim tăng dần
=> Tính phi kim: C < N < O
- H có tính phi kim yếu
=> Nguyên tố O có tính phi kim mạnh nhất

a) Ảnh hưởng của nồng độ: Dùng bình chứa oxygen có nồng độ oxygen cao hơn không khí => Phản ứng cháy dễ dàng xảy ra
b) Ảnh hưởng của áp suất: Dùng nồi áp suất làm tăng áp suất trong nồi => Thực phẩm trong nồi áp suất sẽ nhanh chín hơn
c) Ảnh hưởng của diện tích tiếp xúc: Đậy nắp lò làm hạn chế diện tích tiếp xúc của than với oxygen trong không khí => Phản ứng cháy diễn ra chậm => Giữ than cháy được lâu hơn
d) Ảnh hưởng của nhiệt độ: Khi để thức ăn trong tủ lạnh => Nhiệt độ bị giảm => Kìm hãm phản ứng oxi hóa thức ăn => Thức ăn sẽ lâu bị ôi thiu
- Hình 16.9a) Ảnh hưởng của nồng độ đến tốc độ phản ứng:
Nồng độ oxygen trong không khí chỉ chiếm 21%. Dùng bình chứa oxygen mục đích làm tăng nồng độ chất tham gia ⇒ Tăng tốc độ phản ứng cháy
- Hình 16.9b) Ảnh hưởng của áp suất đến tốc độ phản ứng.
Dùng nồi áp suất làm tăng áp suất trong nồi ⇒ tăng tốc độ phản ứng ⇒ Làm thức ăn nhanh chín hơn.
- Hình 16.9c) Ảnh hưởng của diện tích tiếp xúc đến tốc độ phản ứng.
Đậy nắp lò làm giảm diện tích tiếp xúc của than với oxygen trong không khí ⇒ Giảm tốc độ phản ứng cháy ⇒ Than cháy được lâu hơn.
- Hình 16.9d) Ảnh hưởng của nhiệt độ đến tốc độ phản ứng.
Bảo quản thức ăn trong tủ lạnh ⇒ Giảm nhiệt độ ⇒ Giảm tốc độ phản ứng oxi hóa thức ăn ⇒ Thức ăn lâu bị ôi thiu.

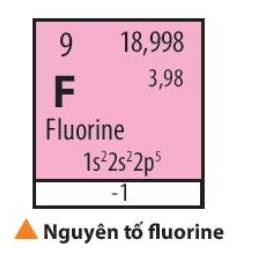
- Fluorine thuộc chu kì 2, nhóm VIIA
=> Có 7 electron ở lớp ngoài cùng
=> Có xu hướng nhận thêm 1 electron tạo thành F- có cấu hình electron bền vững
=> Fluorine có tính phi kim, tính oxi hóa mạnh và có khả năng phản ứng mãnh liệt vì có độ âm điện lớn

\(^{28}_{14}Si,^{29}_{14}Si,^{30}_{14}Si\)
- Số khối = 28: \({}_{14}^{28}Si\)
- Số khối = 29: \({}_{14}^{29}Si\)
- Số khối = 30: \({}_{14}^{30}Si\)

Theo Bảng 4.2 lithium có 1 electron ở lớp ngoài cùng
=> Lithium là nguyên tố kim loại

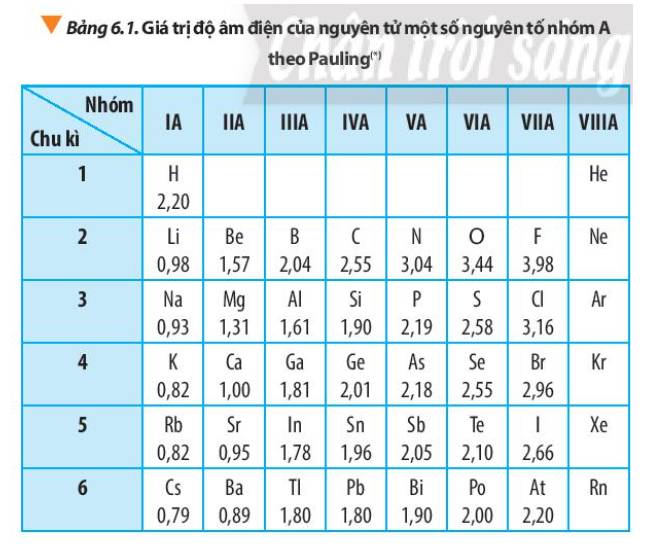
- Các nguyên tố nhóm VIIIA là các nguyên tố khí hiếm, bền ở điều kiện thường và không tham gia liên kết hóa học
=> Không hút electron vì cấu hình electron đã đạt cấu hình bền vững
=> Không có giá trị độ âm điện

- Độ âm điện của nguyên tử các nguyên tố nhóm A có xu hướng biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân:
+ Trong một chu kì: theo chiều tăng dần của điện tích hạt nhân, lực hút giữa hạt nhân với các electron lớp ngoài cùng cũng tăng. Do đó, độ âm điện của nguyên tử các nguyên tố có xu hướng tăng dần
+ Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử tăng nhanh, lực hút giữa hạt nhân với các electron lớp ngoài cùng giảm. Do đó độ âm điện của nguyên tử các nguyên tố có xu hướng giảm dần

- Phản ứng có kèm theo sự thay đổi năng lượng dưới dạng nhiệt năng đóng vai trò quan trọng trong đời sống:
+ Cung cấp nhiệt cho các nhu cầu đun nấu thức ăn
+ Giảm nhiệt độ của môi trường xung quanh




Z = 14: 1s22s22p63s23p2
- Ô nguyên tố: 14
- Chu kỳ: 3
- Nhóm: IV A