Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

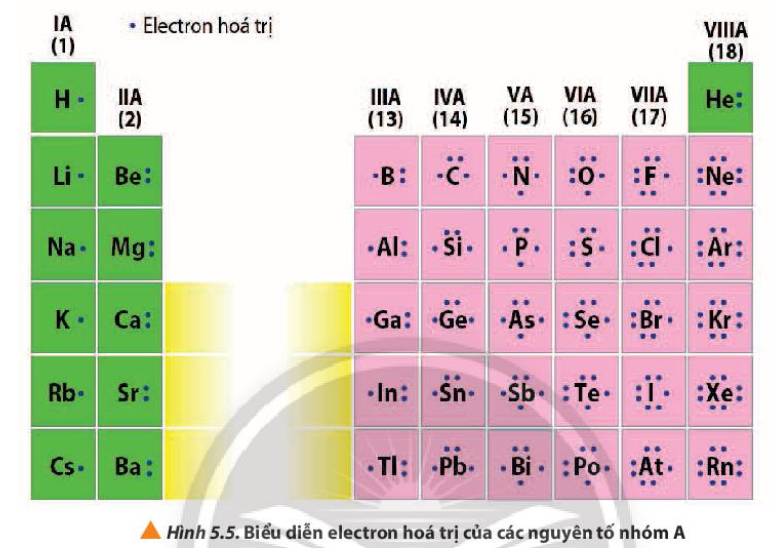
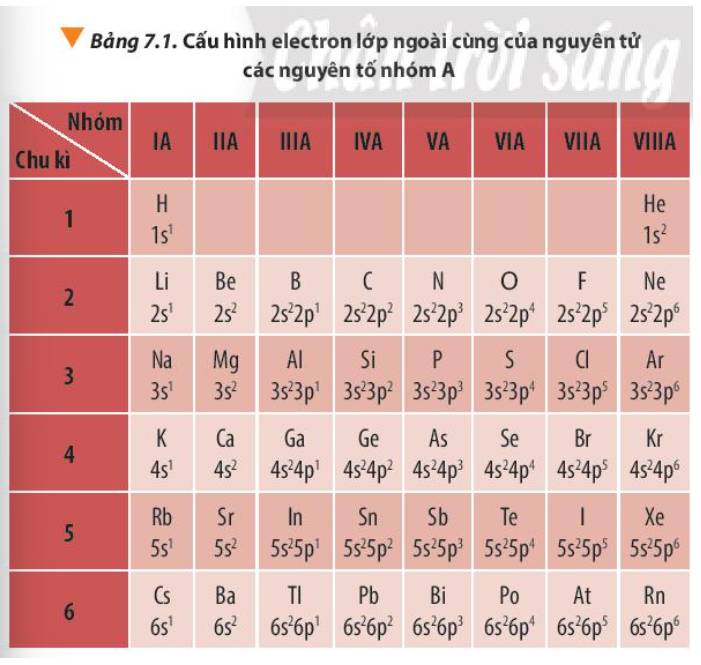
- Số electron hóa trị của nguyên tử = số thứ tự nhóm của nguyên tố nhóm A
Ví dụ:
+ Nhóm IA, các nguyên tố đều có 1 electron hóa trị
+ Nhóm IIIA, các nguyên tố đều có 3 electron hóa trị
+ Nhóm VIIIA (trừ He) các nguyên tố đều có 8 electron hóa trị

- Ion sodium: có 10 electron ở lớp vỏ và 11 proton trong hạt nhân
- Ion oxide: có 10 electron ở lớp vỏ và 8 proton trong hạt nhân

- Lớp 1 có 1 phân lớp
- Lớp 2 có 2 phân lớp
- Lớp 3 có 3 phân lớp
- Lớp 4 có 4 phân lớp
=> Từ lớp 1 đến lớp 4, số phân lớp trong mỗi lớp bằng số thứ tự của lớp đó

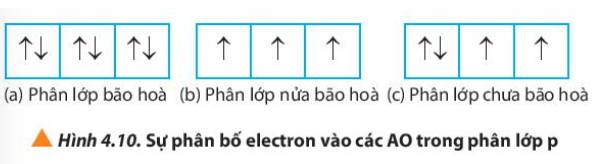
(a) Phân lớp bão hòa => Không có electron độc thân
(b) Phân lớp nửa bão hòa => Số electron độc thân = số orbital của phân lớp đó
(c) Phân lớp chưa bão hòa => số electron độc thân nhỏ hơn số orbital trong phân lớp đó
Trường hợp a) không có electron độc thân
Trường hợp b) có 3 electron độc thân
Trường hợp hợp c) có 2 electron độc thân
Nhận xét:
Phân lớp bão hòa chứa đủ số electron tối đa.
Phân lớp nửa bão hòa chứa một nửa số electron tối đa.
Phân lớp chưa bão hòa chưa đủ số electron tối đa.

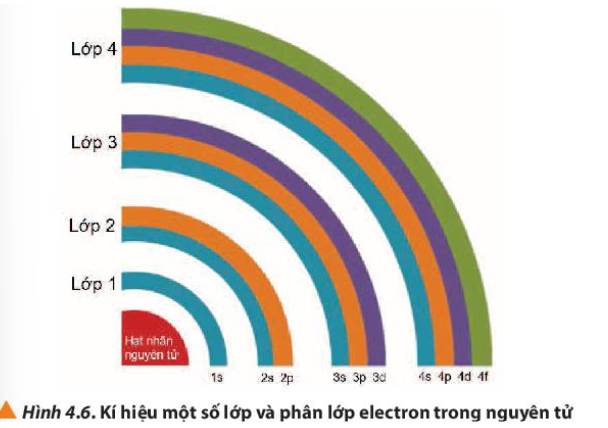
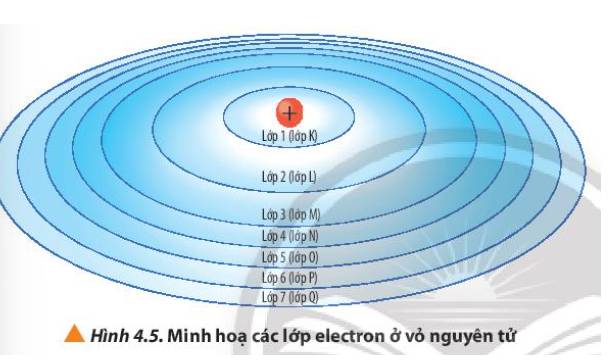
- Lớp 1 – Lớp K
- Lớp 2 – Lớp L
- Lớp 3 – Lớp M
- Lớp 4 – Lớp N
- Lớp 5 – Lớp O
- Lớp 6 – Lớp P
- Lớp 7 – Lớp Q
=> Cách gọi tên theo bảng chữ cái từ K đến Q lần lượt ứng với các lớp từ 1 đến 7
Các electron được sắp xếp thành từng lớp kí hiệu K, L, M, N, O, P, Q từ gần đến xa hạt nhân theo thứ tự từ lớp n = 1 đến n = 7.

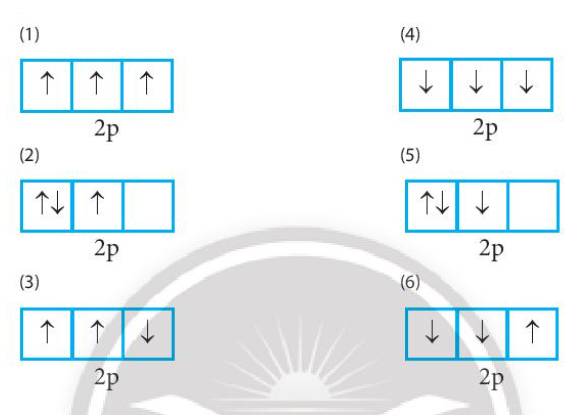
(1): đúng vì chứa tối đa electron và biểu diễn electron độc thân bằng mũi tên đi lên
(2): sai vì số electron độc thân chưa tối đa
(3): sai vì biểu diễn 1 electron độc thân bằng mũi tên đi xuống
(4): sai vì biểu diễn electron độc thân bằng mũi tên đi xuống
(5): sai vì số electron độc thân chưa tối đa, biểu diễn electron độc thân bằng mũi tên đi xuống
(6): sai vì biểu diễn 2 electron độc thân bằng mũi tên đi xuống

- Số electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm `A` trong cùng `1` chu kì có xu hướng tăng dần từ trái qua phải và `2` nguyên tố cạnh nhau hơn kém `1 e.`
- Số electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm `A` trong cùng `1` nhóm thì có số electron lớp ngoài cùng bằng nhau.
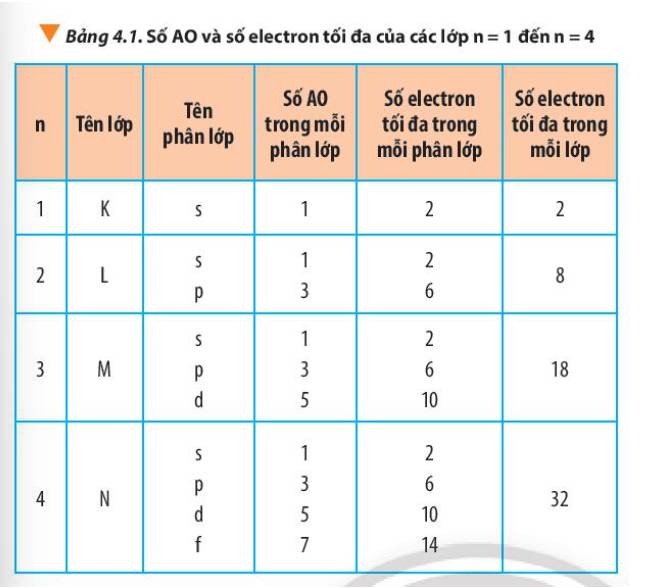


- Lớp 1 có tối đa 2 electron = 2.12
- Lớp 2 có tối đa 8 electron = 2.22
- Lớp 3 có tối đa 18 electron = 2.32
- Lớp 4 có tối đa 32 electron = 2.42
=> Số electron tối đa trong lớp n là 2n2