Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Sử dụng đường chéo ta tính được phần trăm số nguyên tử H 1 và H 2 :
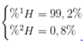
Thành phần % về khối lượng của 2H trong H2O là:
2 . 0 , 008 . 2 16 + 2 . 1 , 008 = 0 , 178 %

\(\%^1H=a;\%^2H=100\%-a\left(a>0\right)\\\overline{NTK}_H=1,008\\ \Leftrightarrow\dfrac{1.a+2.\left(100\%-a\right)}{100\%}=1,008\\ \Leftrightarrow a=99,2\%\\ \Rightarrow^1H=99,2\%;\%^2H=0,8\%\)
Số nguyên tử của đồng vị 2H có trong 9ml nước là:
\(\dfrac{9.1}{18}.6.10^{23}.\dfrac{2}{18}.0,8\%\approx2,667.10^{20}\left(nguyên.tử\right)\)

1 ml có khối lượng là 1 gam. Số mol H2O = 1/18 = 0,056 mol.
H2O ---> 2H + O
Nên số mol H = 2.0,056 = 0,112 mol. Số nguyên tử H là 0,112.6,023.1023 = 674576.1017.
Gọi a, b tương ứng là tỉ lệ % của 11H và 12H.
Ta có: a + 2b = 1,008 và a + b = 1 Suy ra b = 0,008 (0,8%); a = 0,992 (99,2%)
Như vậy, số nguyên tử 11H là 0,992.674576.1017 = 669179392.1014 nguyên tử. Số nguyên tử 12H là 0,008.674576.1017 = 5396608.1014 nguyên tử

\(Đặt:\%^1H=a\\ \%^2H=100\%-a\\ Vì:\overline{NTK}_H=1,008\\ \Leftrightarrow\dfrac{1.a+2.\left(100\%-a\right)}{100\%}=1,008\\ \Leftrightarrow a=99,2\%\Rightarrow\%^1H=99,2\%;\%^2H=0,8\%\)
Số nguyên tử 2H có trong 1ml nước là:
\(0,8\%.\dfrac{1.1.2}{18}\approx8,889\%\)

Gọi x là thành phần phần trăm của H 1 thành phần phần trăm của H 1 2 sẽ là 100 –x
![]()
Giải ra ta được: x = 99,2.
Kết quả:thành phần : H 1 1 là 99,2%
H 1 2 là 0.8%

Câu 1 :
Gọi :
số khối của 2 đồng vị của nguyên tố X lần lượt là A1,A2
tỉ lệ số nguyên tử của đồng vị 1 và đồng vị 2 lần lượt là x1 , x2
Theo đề bài ta có :
A1 = Z + N = P + N = 51+70 = 121
A2 = Z + N = P + N = 51 + 72 = 123
Ta có tỉ lệ : \(\dfrac{x1}{x2}=\dfrac{31}{19}=>x1=\dfrac{31}{19}x2\)
mà x1 + x2 = 100 <=> \(\dfrac{31}{19}x2+x2=100=>x2=38\%\) => x1= 62%
=> \(\overline{A_X}=\dfrac{A1.x1+A2.x2}{100}=\dfrac{121.62+123.38}{100}=121,76\)
Vậy....
câu 2 :
Gọi tỉ lệ số nguyên tử của \(^1_1H\) và \(^2_1H\) lần lượt là x1 và x2
Ta có : \(\overline{A_H}=\dfrac{1.x1+2.x2}{100}< =>1,008=\dfrac{x1+2x2}{100}\) <=> x1+2x2=1,008.100 (1)
mà x1+x2 =100 (2)
từ (1) và (2) => x1 = 99,2 và x2= 0,8
Ta có mH2O = V.D = 1.1=1(g)
=> nH2O=1/18(mol)
trong 1 mol H2O có chứa 6,02.10^23 phân tử H2O
vậy trong 1/18mol H2O có chứa 1/18.6,02.10^23 phân tử H2O
Ta lại có :
1 phân tử H2O thì có chứa 2 nguyên tử H
vậy 1/18.6,02.10^23 phân tử H2O thì có chứa \(2.\dfrac{1}{18}.6,02.10^{23}\) nguyên tử H
=> Số nguyên tử của đồng vị \(^2_1H\) là : \(2.\dfrac{1}{18}.6,02.10^{23}.0,8\%~5,35.10^{20}\)(nguyên tử)