Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Trong phân tử mỗi hợp chất ở Bảng 7.1, tích hóa trị và số nguyên tử của nguyên tố này bằng tích hóa trị và số nguyên tử của nguyên tố kia.

Ta có:
- Hóa trị của Mg: II
- Hóa trị của Cl: I
Vì vậy hai nguyên tử Cl sẽ bằng 1 nguyên tử Mg ⇒ Mg có thể liên kết với 2 nguyên tử Cl ⇒ Công thức hóa học tổng quát: MgCl2.

Cu hóa trị II
Mg hóa trị II
K hóa trị I
C hóa trị IV
S hóa trị II

| Nguyên tố | Si | O |
| Hóa trị | IV | II |
| Số nguyên tử | 1 | 2 |
| Tích hóa trị và số nguyên tử | IV x 1 II.2 |
=> Tích hóa trị và số nguyên tử của nguyên tố Si = tích hóa trị và số nguyên tử của nguyên tố O

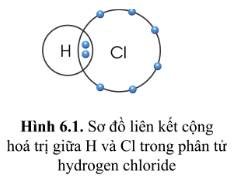
Hóa trị của H và Cl đều là I, bằng với số electron mà nguyên tử H và Cl góp chung để tạo ra liên kết.

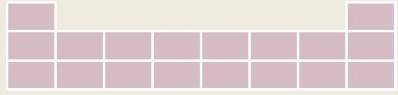
- Sự thay đổi số electron ở lớp ngoài cùng trong cùng 1 hàng khi đi từ trái sang phải:
+ Hàng thứ 1: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 2
+ Hàng thứ 2: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 8
+ Hàng thứ 3: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 8

Gọi ct chung: \(H^I_xS^{II}_y\)
Theo qui tắc hóa trị: `I.x = II.y =>`\(\dfrac{x}{y}=\dfrac{II}{I}\)
`-> x=2, y=1`
`-> CTHH: H_2S`
\(K.L.P.T_{H_2S}=1.2+32=34< amu>.\)
\(\%H=\dfrac{1.2.100}{34}\approx5,88\%\)
`%S = 100%-5,88% =94,12%`




Ta thấy: 1.II = 2.I ⇒ Tích của chỉ số và hóa trị của nguyên tố lưu huỳnh bằng tích của chỉ số và hóa trị của nguyên tố hydrogen.
Ta có: 1 x IV = 4 x I = IV=> Tích của chỉ số và hóa trị của nguyên tố carbon = tích chỉ số và hóa trị của nguyên tố hydrogen