Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sách giáo khoaa cần cải cách vấn đề này, chứ dạy học sinh theo sách mà đáp án lại ra theo thí nghiệm thì căn cứ ở đâu mà chấm? Hồi đó tỉnh em cũng bị cái này :v trong sgk bảo màu vàng :v nhưng thi ra lại là màu nâu đất :v mọi người đều nói là lấy sgk làm căn cứ :))) nhưng người ra đề lấy thực tế và học sinh đều bị trừ câu đó 0,25 đ (trừ mấy người làm sai ^_^). 0,25 đ :))) đủ khiến một vài ai đó rớt tốt nghiệp cấp II và tuyển sinh lớp 10 :v
nói tóm tác vấn đề của cô giáo đã nói :
| muối tạo bởi | bazơ mạnh | bazơ yếu |
| axit mạnh | không đổi màu quì tím | đổi màu quì tím sang màu đỏ |
| axit yếu | đổi màu quì tím sang màu xanh | trường hợp này thì chưa chắc được và độ pH của nó gần bằng 7 |

TRẢ LỜI:
CO - Cacbon monoxit
CO2 - Cacbon đioxit
HNO3 - Axit nitric
Cl2O - Điclo monoxit
B2H6 - Điboran
PH3 - Photphin
PH5 - Photphoran
C6H12 - Xiclohexan
CO : cacbon oxit
\(CO_2\): cacbon đioxit
\(HNO_3\): axit nitric
\(Cl_2O\): điclo monooxxit
\(B_2H_6\): điboran
\(PH_3\): photphin
\(PH_5\): ??? làm g có
\(C_6H_{12}\): xiclohexan

Câu 1 :
\(a.CH_4+Cl_2\underrightarrow{as,1:1}CH_3Cl+HCl\)
\(b.C_2H_4+H_2O\underrightarrow{^{H^+,t^0}}C_2H_5OH\)
\(c.CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)
\(d.C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\)
\(e.CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
\(f.\left(RCOO\right)_3C_3H_5+3NaOH\rightarrow3RCOONa+C_3H_5\left(OH\right)_3\)
Câu 2 :
a) CTCT C2H2 và C2H6 :
\(CH\equiv CH\)
\(CH_3-CH_3\)
b) Nhận biết CH4, C2H4 :
Sục lần lượt các khí qua dung dịch Br2 dư :
- Mất màu : C2H4
- Không HT : CH4
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
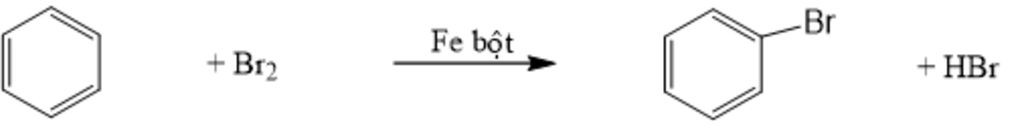
c)
TN1 : Mất màu nâu đỏ Br2 và có khí HBr thoát ra.
 TN2 :
TN2 :
Dầu ăn không tan trong nước , nổi trên bề mặt
Câu 3 :
\(n_{CH_4}=a\left(mol\right),n_{C_2H_6}=b\left(mol\right)\)
\(n_X=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(\Rightarrow a+b=0.2\left(1\right)\)
\(n_{CaCO_3}=\dfrac{30}{100}=0.3\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{^{t^0}}CO_2+2H_2O\)
\(C_2H_6+\dfrac{7}{2}O_2\underrightarrow{^{t^0}}2CO_2+3H_2O\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(..............0.3......0.3\)
\(n_{CO_2}=a+2b=0.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%V_{CH_4}=\%V_{C_2H_6}=\dfrac{0.1}{0.2}\cdot100\%=50\%\)
Câu 4 :
\(\text{ Trong 100 ml cồn 70 độ có 70 ml rượu etylic và 30 ml nước.}\)
\(V_{C_2H_5OH}=\dfrac{70}{100}\cdot50=35\left(ml\right)\)
\(n_{C_2H_5OH}=\dfrac{9.2}{46}=0.2\left(mol\right)\)
\(n_{CH_3COOH}=\dfrac{6}{60}=0.1\left(mol\right)\)
\(CH_3COOH+C_2H_5OH\underrightarrow{H^+,t^0}CH_3COOC_2H_5+H_2O\)
\(0.1.........................0.1....................0.1\)
\(H\%=\dfrac{5.28}{0.1\cdot88}\cdot100\%=60\%\)

-lấy mỗi chất một ít làm mẫu thử , cho tác dụng với Ca phản ứng nào xuất hiện kết tủa thì chất ban đầu là BaCo3và Na2Co3(1),phản ứng nào không cho kết tủa thì chất ban đầu là MgCl2 , CaCl2 , NaCl(2)
BaCo3+Ca\(\rightarrow\)CaCo3\(\downarrow\) +Ba
Na2Co3+Ca\(\rightarrow\) CaCo3\(\downarrow\) +2Na
-cho nhóm (1) tác dụng với H2SO4 , phản ứng nào xuất hiên kết tủa thì chất ban đầu là BaCo3 , phản ứng nào không xuất hiện kết tủa thì chất ban đầu là Na2Co3
BaCo3+H2SO4 \(\rightarrow\) BaSO4\(\downarrow\) +H2O+CO2\(\uparrow\)
Na2CO3+H2SO4 \(\rightarrow\) Na2SO4+ H2O+CO2\(\uparrow\)
-cho nhóm (2) tác dụng với KOH , phản ứng nào xuất hiện kết tủa thì chất ban dầu là MgCl2 , phản ứng nào không thấy hiện tượng gì thì chất ban dầu là CaCl2 và NaCl (3) :
MgCl2+ 2KOH \(\rightarrow\) Mg(OH)2\(\downarrow\) + 2KCl
- cho nhóm (3) tác dụng với H2SO4,phản ứng nào xuát hiện kết tủa thì chất ban đầu là CaCl2 , phản ứng nào không thấy có hiện tượng gì thì chất ban đầu là NaCl
CaCl2+H2SO4\(\rightarrow\) CaSO4\(\downarrow\) + 2HCl
- Trích thành những mẫu thư nhỏ
- Cho các mẫu thử trên vào nước
+ Mẫu thử không tan trong nước là BaCO3
+ 3 mẫu thử tan dần ra trong nước là MgCl2, CaCl2 và Na2CO3
- Cho HCl lần lượt vào 3 mẫu thửu còn lại
+ Mẫu thử có bọt khí không màu xuất hiện là Na2CO3
Na2CO3+2HCl→2NaCl+CO2\(\uparrow\)+H2O
+ Hai mẫu thử không có hiện tượng gì là MgCl2 và CaCl2
- Cho dung dịch NaOH lần lượt vào hai mẫu thử còn lại
+ Mẫu thử xuất hiện kết tủa trắng trong dung dịch là MgCl2
MgCl2+2NaOH→2NaCl+Mg(OH)2↓
+ Mẫu thử không có hiện tượng gì là CaCl2

4.
Quỳ tím:-NaCl: quỳ tím không đổi màu
-hcl: quỳ tím hóa đỏ
-Ba(Oh)2: quỳ tím hóa xanh
-Na2CO3: quỳ tím không đổi màu
Dùng AgNO3 để tìm dd chứa NaCl và Na2CO3 nhờ kết tủa trắng.
-Kết tủa trắng: AgCl =>NaCl
pthh: NaCl+ AgNO3 -> AgCl +NaNO3
- ko có hiện tượng gì => Na2CO3
bạn nào giúp mik giải những bài nay nhé
thank bạn!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!1

Bài 1:
a) K: 2K + 2HCl---> 2KCl+ H2
2K + 2H2O ---> 2KOH + H2 (nếu K dư)
Zn: Zn+ 2HCl--> ZnCl2 + H2
Cu: ko có pứ
AgNO3: AgNO3+ HCl ---> AgCl + HNO3
CuO : CuO + 2HCl --> CuCl2 + H2O
NaOH: NaOH + HCl --> NaCl + H2O
Na2SO4: ko có pứ
Mg(OH)2: Mg(OH)2 + 2HCl--> MgCl2 + 2H2O
K2CO3: K2CO3 + 2HCl --- > 2KCl + CO2 + H2O
Al2O3: Al2O3 + 6HCl --> 2AlCl3 + 3H2O
b) Na: 2Na + 2H2O --> 2NaOH
CO2: CO2 + Ba(OH)2 ---> BaCO3 + H2O (nếu Ba(OH)2 dư)
2CO2 + Ba(OH)2 ---> Ba(HCO3)2 (nếu CO2 dư)
H2SO4: Ba(OH)2 + H2SO4 --> BaSO4 + 2H2O
HCl: Ba(OH)2 + 2HCl ---> BaCl2 + H2O
MgSO4: MgSO4 + Ba(OH)2 --> Mg(OH)2 + BaSO4
Al2O3: Al2O3 + 3H2SO4 --> Al2(SO4)3 + 3H2O
NaCl: ko pứ
CuCl2: CuCl2 + Ba(OH)2 ---> Cu(OH)2 + BaCl2
c) K: 2K + 2H2O --> 2KOH + H2
Mg: ko pứ
H2SO4: Na2CO3 + H2SO4 --> Na2SO4 + CO2 + H2O
KOH: ko pứ
Ca(OH)2: Ca(OH)2 + Na2CO3 --> 2NaOH + CaCO3
BaCl2: BaCl2 + Na2CO3 --> 2NaCl + BaCO3
KCl: ko pứ
Bài 2: A: Fe2O3 B: FeCl3
D: Fe(OH)3 E: Fe2O3
4Fe + 3O2 ---> 2Fe2O3
Fe2O3 + 6HCl---> 2FeCl3+ 3H2O
FeCl3 + 3NaOH --> Fe(OH)3 + 3NaCl
2Fe(OH)3 ----> Fe2O3 + 3H2O

Câu 1: Hãy viết các PTHH theo các sơ đồ phản ứng sau đây:
1) AgNO3 + HCl ---> AgCl↓+HNO3
2) Cu + H2SO4đnóng ---> CuSO4+SO2↑+H2O
3) BaCO3 + H2SO4 ---> BaSO4+CO2+H2O
4) 2NaOH + CuSO4 ---> Na2SO4+Cu(OH)2↓
5) Al(OH)3
6) K2CO3 + 2HCl --->2KCl + CO2↑+H2O
7) Ba(NO3)2 + Na2SO4 ---> NaNO3 + BaSO4↓
8) CuSO4 + 2KOH ---> K2SO4 + Cu(OH)2↓
9) AgNO3 + HCl ---> KNO3 + AgCl↓
Câu 2: Viết PTHH thực hiện chuỗi biến hóa sau:
a. Al2O3 ---> Al ---> Al(NO3)3 ---> Al(OH)3 ---> Al2O3 ---> Al2(SO4)3 ---> AlCl3 ---> Al ---> Cu
\(2Al_2O_3--dpnc->4Al+3O_2\)
\(Al+4HNO_3-->Al\left(NO_3\right)_3+NO\uparrow+2H_2O\)
\(Al\left(NO_3\right)_3+3NaOH-->Al\left(OH\right)_3\downarrow+3NaNO_3\)
\(2Al\left(OH\right)_3-to->Al_2O_3+3H_2O\)
\(Al_2O_3+3H_2SO_4-->Al_2\left(SO_4\right)_3+3H_2O\)
\(Al_2\left(SO_4\right)_3+3BaCl_2-->2AlCl_3+3BaSO_4\downarrow\)
\(3Mg+2AlCl_3-->3MgCl_2+2Al\)
\(3CuCl_2+2Al-->2AlCl_3+3Cu\)
b. Fe ---> FeCl3 ---> Fe(OH)3 ---> Fe2O3 ---> Fe ---> FeCl2 ---> Fe(NO3)2 ---> FeCO3 ---> FeSO4.
\(2Fe+3Cl_2--to->2FeCl_3\)
\(FeCl_3+3NaOH-->Fe\left(OH\right)_3\downarrow+3NaCl\)
\(2Fe\left(OH\right)_3-to->Fe_2O_3+3H_2O\)
\(Fe_2O_3+3CO-to->2Fe+3CO_2\uparrow\)
\(Fe+2HCl-->FeCl_2+H_2\uparrow\)
\(FeCl_2+2AgNO_3-->Fe\left(NO_3\right)_2+AgCl\downarrow\)
\(Fe\left(NO_3\right)_2+Na_2CO_3--->FeCO_3+2NaNO_3\)
\(FeCO_3+H_2SO_4-->FeSO_4+CO_2\uparrow+H_2O\)
c. Mg ---> MgO ---> MgCl2 ---> Mg(OH)2 ---> MgSO4 ---> MgCl2 ---> Mg(NO3)2 ---> MgCO3
\(2Mg+O_2--to->MgO\)
\(MgO+2HCl-->MgCl_2+H_2O\)
\(MgCl_2+2NaOH-->Mg\left(OH\right)_2\downarrow+2NaCl\)
\(Mg\left(OH\right)_2+H_2SO_4-->MgSO_4+2H_2O\)
\(MgSO_4+BaCl_2-->MgCl_2+BaSO_4\downarrow\)
\(MgCl_2+2AgNO_3-->Mg\left(NO_3\right)_2+2AgCl\downarrow\)
\(Mg\left(NO_3\right)_2+Na_2CO_3-->MgCO_3\downarrow+2NaNO_3\)
d. Cu(OH)2 ---> CuO ---> CuSO4 ---> CuCl2 ---> Cu(NO3)2 ---> Cu ---> CuO.
\(Cu\left(OH\right)_2-->CuO+H_2O\)
\(CuO+H_2SO_4-->CuSO_4+H_2O\)
\(CuSO_4+BaCl_2-->CuCl_2+BaSO_4\downarrow\)
\(CuCl_2+2AgNO_3-->Cu\left(NO_3\right)_2+2AgCl\downarrow\)
\(Fe+Cu\left(NO_3\right)_2-->Fe\left(NO_3\right)_2+Cu\)
\(2Cu+O_2-->2CuO\)

Câu 1: Chất tác dụng với nước tạo ra dung dịch bazơ là:
A. K2O. B. CuO. C. CO. D. SO2.
Câu 2: Chất tác dụng với nước tạo ra dung dịch axit là:
A. CaO, B. BaO, C. Na2O D. SO3.
Câu 3: Sắt (III) oxit (Fe2O3) tác dụng được với:
A. Nước, sản phẩm là axit. B. Axit, sản phẩm là muối và nước.
C. Nước, sản phẩm là bazơ. D. Bazơ, sản phẩm là muối và nước.
Câu 4: Dãy chất sau là oxit lưỡng tính:
A. Al2O3, ZnO, PbO2, Cr2O3. B. Al2O3, MgO, PbO, SnO2.
C. CaO, ZnO, Na2O, Cr2O3. D. PbO2, Al2O3, K2O, SnO2
Câu 5: Dãy oxit vừa tác dụng nước, vừa tác dụng với dung dịch kiềm là:
A.CuO, Fe2O3, SO2, CO2. B. CaO, CuO, CO, N2O5.
C. SO2, MgO, CuO, Ag2O. D. CO2, SO2, P2O5, SO3.
Câu 6: Sản phẩm của phản ứng phân hủy canxicacbonat bởi nhiệt là:
A. CaO và CO B. CaO và CO2 C. CaO và SO2 D. CaO và P2O5
Câu 7: Hòa tan hết 12,4 gam Natrioxit vào nước thu được 500ml dung dịch A . Nồng độ mol của dung dịch A là:
A. 0,8M B. 0,6M C. 0,4M D. 0,2M
Câu 8: Hòa tan hết 5,6 gam CaO vào dd HCl 14,6% . Khối lượng dung dịch HCl đã dùng là:
A. 50 gam B. 40 gam C. 60 gam D. 73 gam
Câu 9: Để thu được 5,6 tấn vôi sống với hiệu suất phản ứng đạt 95% thì lượng CaCO3 cần dùng là :
A. 9,5 tấn B. 10,5 tấn C. 10 tấn D. 9,0 tấn
Câu 10: Cặp chất tác dụng với nhau tạo thành sản phẩm có chất khí:
A Bari oxit và axit sunfuric loãng B. Bari hiđroxit và axit sunfuric loãng
C. Bari cacbonat và axit sunfuric loãng D Bari clorua và axit sunfuric loãng
Câu 11: Có 3 lọ mất nhãn đựng riêng biệt 3 dung dịch của 3 chất: HCl, Na2SO4, NaOH . Chỉ dùng một hóa chất nào sau đây để phân biệt chúng?
A. Dung dịch BaCl2 B. Quỳ tím C. Dung dịch Ba(OH)2 D. Zn
Câu 12: Khi cho từ từ dung dịch NaOH cho đến dư vào ống nghiệm đựng dung dịch hỗn hợp gồm HCl và một ít phenolphtalein. Hiện tượng quan sát được trong ống nghiệm là:
A. Màu đỏ mất dần. B. Không có sự thay đổi màu
C. Màu đỏ từ từ xuất hiện. D. Màu xanh từ từ xuất hiện.
Câu 13: Dùng thuốc thử nào sau đây để nhận biết các chất chứa trong các ống nghiệm mất nhãn: HCl, KOH, NaNO3, Na2SO4.
A. Dùng quì tím và dung dịch CuSO4.
B. Dùng dung dịch phenolphtalein và dung dịch BaCl2.
C. Dùng quì tím và dung dịch BaCl2. D. Dùng dung dịch phenolphtalein và dung dịch H2SO4.
Câu 14: Cho 100 ml dung dịch H2SO4 2M tác dụng với 100 ml dung dịch Ba(NO3)2 1M. Nồng độ mol của dung dịch sau phản ứng lần lượt là:
A. H2SO4 1M và HNO3 0,5M.
B. BaSO4 0,5M và HNO3 1M.
C. HNO3 0,5M và Ba(NO3)2 0,5M.
D. H2SO4 0,5M và HNO3 1M.
Câu 15:. Dãy các bazơ bị nhiệt phân huỷ tạo thành oxit bazơ tương ứng và nước:
A. Cu(OH)2 ; Zn(OH)2; Al(OH)3; Mg(OH)2
B. Cu(OH)2 ; Zn(OH)2; Al(OH)3; NaOH
C. Fe(OH)3; Cu(OH)2; KOH; Mg(OH)2
D. Fe(OH)3; Cu(OH)2; Ba(OH)2; Mg(OH)2
Câu 16: Dãy các bazơ làm phenolphtalein hoá đỏ:
A. NaOH; Ca(OH)2; Zn(OH)2; Mg(OH)2
B. NaOH; Ca(OH)2; KOH; LiOH
C. LiOH; Ba(OH)2; KOH; Al(OH)3
D. LiOH; Ba(OH)2; Ca(OH)2; Fe(OH)3
Câu 17:. Sục 2,24 lít khí CO2 vào dung dịch chứa 0,2 mol NaOH. Dung dịch thu được sau phản ứng chứa:
A. NaHCO3 B. Na2CO3 C. Na2CO3 và NaOH dư D. NaHCO3 và NaOH dư


Câu 17 : Đáp án B
Câu 18 : $n_{NaOH} = n_{ion\ dương} = 2n_{SO_4^{2-}} + n_{Cl^-} = 0,35(mol)$
$V_{dd\ NaOH} = \dfrac{0,35}{1} = 0,35(lít)$
Đáp án A
Câu 19 : Đáp án B
Câu 17. Hãy cho biết dãy các chất nào sau đây đều tác dụng với NaOH?
A. NaCl, BaCl2, CuCl2 và BaCO3
B. NaHCO3, NH4Cl, FeCl2 và Zn(OH)2
C. Na2HPO4, CH3COONa, FeCl2 và Al(OH)3
D. NaHSO4, NH4NO3, BaCl2 và Pb(OH)2
Câu 18. Dung dịch X chứa Al3+, Fe2+; Cl- 0,15 mol và SO42- 0,10 mol. Xác định thể tích dung dịch NaOH 1,0M cần cho vào dung dịch X để thu được kết tủa có khối lượng lớn nhất?
A. 0,35 lít B. 0,30 lít C. 0,25 lít D. 0,40 lít
Câu 19. Cho 200 ml dd chứa NaOH 1,0M và Ba(OH)2 0,8M vào 100,0 ml dd Al2(SO4)3 0,8M. Tính khối lượng kết tủa thu được sau PƯ?
A. 49,76 gam B. 46,64 gam C. 68,40 gam D. 65,28 gam