Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nH2=\(\dfrac{1,68}{22,4}\)=0,075mol
Fe + H2SO4 -> FESO4 + H2
n ban đầu: 0,2mol
n pứ: 0,075mol 0,075mol 0,075mol
Vì \(\dfrac{0,2}{1}\)>\(\dfrac{0,075}{1}\) nên H2SO4 dư
a) mFe pứ= 0,075.56=4,2g
b) Fe2O3 + 3H2 -> 2Fe + 3H2O
n pứ: 0,0375mol 0,075mol
mFe2O3 pứ=0,0375.160=6g

\(n_{Mg}=\frac{m}{M}=\frac{9,6}{24}=0,4mol\)
PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
1 : 1 : 1 : 1 mol
0,4 0,4 0,4 0,4 mol
a. \(m_{MgSO_4}=n.M=0,4.\left(24+32+16.4\right)=48g\)
b. \(V_{H_2}=n.22,4=0,4.22,4=8,96l\)
c. \(n_{Fe_2O_3}=\frac{m}{M}=\frac{64}{56.2}+16.3=0,4mol\)
PTHH: \(3H_2+Fe_{2O_3}\rightarrow2Fe+3H_2O\left(ĐK:t^o\right)\)
3 : 1 : 2 : 3 mol
1, 7 0,4 0,8 1,2 mol
\(m_{Fe}=n.M=0,8.56=44,8g\)

PTHH: Fe2O3 + CO =(nhiệt)=> Fe + CO2
Áp dụng định luật bảo toàn khối lượng, ta có:
mFe = mFe2O3 + mCO - mCO2 = 16,8 + 32 - 26,4 = 22,4 kg

a)\(Fe2O3+3H2-->2Fe+3H2O\)
b)\(n_{H2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{Fe}=\frac{2}{3}n_{H2}=0,2\left(mol\right)\)
\(m_{Fe}=0,2.56=11,2\left(g\right)\)
c)\(Fe+H2SO4-->FeSO4+H2\)
\(n_{H2SO4}=n_{Fe}=0,2\left(mol\right)\)
\(m_{H2SO4}=0,2.98=19,6\left(g\right)\)

+n H2 = 11,2 / 22,4 = 0,5 mol
PT
Fe + H2SO4 -> FeSO4 + H2
0,5__0,5_____0,5______0,5 (mol)
-> mFe phản ứng = 0,5 * 65 = 28 (g)
gọi mdd H2SO4 = x (g)
-> mH2SO4 (dd đầu) = x*24,5%=0,245x (g)
->nH2S04 (dd đầu) = 0,245x /98 = 0,0025x mol
Theo PT nH2SO4 phản ứng = nH2 = 0,5 mol
-> m dd H2SO4 phản ứng = m H2S04 (dd đầu) phản ứng = 0,5 * 98 = 49 (g)
-> x = 0,5/ 0,0025= 200 (g)
m muối FeSO4 = 0,5 * 152 = 76 g
m H2 = 0,5 *2 = 1 (g)
m dd sau = m Fe + m dd H2SO4 - m H2
= 28 + 200 -1=227 g
C% FeSO4 (ddsau) = 76/227 *100% = 33,48%

Phải dùng 4,2 g Fe
Cần 6g sắt (III) oxit tác dụng với H2 dư

PTHH ( I ) : \(Fe_xO_y+yH_2\rightarrow xFe+yH_2O\)
PTHH ( II ) : \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{H_2O}=\frac{m_{H_2O}}{M_{H_2O}}=\frac{3,6}{2+16}=0,2\left(mol\right)\)
-> \(n_{\left(O\right)}=n_{H_2O}=0,2\left(mol\right)\)
\(n_{H_2}=\frac{V_{H_2}}{22,4}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
- Theo PTHH ( II ): \(n_{Fe}=n_{H_2}=0,15\left(mol\right)\)
-> \(n_{\left(Fe\right)}=n_{Fe}=0,15\left(mol\right)\)
Ta có : \(n_{Fe}:n_O=0,15:0,2=3:4\)
Vậy công thức hóa học của oxit sắt đó là Fe3O4 .
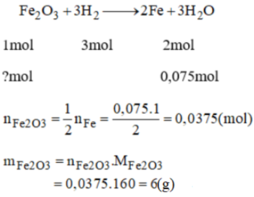
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3
a)\(m_{Fe}=0,3\cdot56=16,8g\)
b)\(Fe_2O_3+3H_2\rightarrow3Fe+3H_2O\)
0,1 0,3 0,3
\(m_{Fe_2O_3}=0,1\cdot160=16g\)
a)nH2 =6,72:22,4=0,3(mol)
PTHH Fe+H2SO4--->FeSO4+H2
theo pt , nFe = nH2 = 0,3 (mol)
=> mFe =n.M=0,3.56=16,8(g)
b) Ta có nH2=nFe=0,3(MOL)
Pthh: Fe2O3 + 3H2 ---> 2Fe + 3H2O
theo pt , nFe2O3=1/3 nH2=0,1(mol)
=> mFe2O3= n.M=0,1.(56.2+16.3)=16(g)
Vậy để có lượng sắt tham gia phản ứng trên phải có 16g Fe2O3 để tác dụng với H2