Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình điện li :
a) K2S → 2K+ + S2_
b) Na2HPO4 → 2Na+ +. HPO42-
HPO42- H+ + PO43-
c) NaH2PO4 → Na+ + H2PO4-
H2PO4- H+ + HPO42-
HPO42- H+ + PO43-
d) Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơ
H2PbO2 2H+ + PbO22- : phân li kiểu axit
e) HBrO H+ + BrO-
g) HF H+ + F-
h) HClO4 → H+ + ClO4-.
a/ K2S -> 2K+ S2_
b/ Na2HPO4 -> 2Na +. HPO42-HPO42- H + + PO43-
c/ NaH2PO4 -> Na + + H2PO4-H2PO4 - H+ + HPO42-HPO42- H+ + PO43-
d/ Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơH2PbO2 2H+ + PbO22- : phân li kiểu axit
e/ HBrO H+ + BrO-
g/ HF H+ +F-
h/ HCIO4 -> H+ +CIO4-

a) K2S → 2K+ + S2_
b) Na2HPO4 → 2Na+ +. HPO42-HPO42- H+ + PO43-
c) NaH2PO4 → Na+ + H2PO4-H2PO4- H+ + HPO42-HPO42- H+ + PO43-
d) Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơH2PbO2 2H+ + PbO22- : phân li kiểu axit
e) HBrO H+ + BrO-
g) HF H+ + F-
h) HClO4 → H+ + ClO4-.
K2S 2K+ + S2-
Na2HPO4 2Na+ + HPO42-
HClO4 H+ +ClO4-
Pb(OH)2 Pb2+ + 2OH-
Pb(OH)2 2H+ + PbO22-
HF H+ +F-
HPO42- H+ + PO43-
NaH2PO4 Na+ + H2PO4-
H2PO4- H+ + HPO42-
HPO42- H+ + PO43-
HBrO H+ + BrO-
viết phương trình điện ly của các chất sau : K2S , Na2HPO4 , NaH2PO4 , Pb(OH)2 , HBrO , HF , HClO4 .

Phân trình điện li:
a) K2S → 2K+ + S2_
b) Na2HPO4 → 2Na+ +. HPO42-HPO42- H+ + PO43-
c) NaH2PO4 → Na+ + H2PO4-H2PO4- H+ + HPO42-HPO42- H+ + PO43-
d) Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơH2PbO2 2H+ + PbO22- : phân li kiểu axit
e) HBrO H+ + BrO-
g) HF H+ + F-
h) HClO4 → H+ + ClO4-.

a) Các chất điện li mạnh phân li hoàn toàn nên phương trình điện li và nồng độ các ion trong dung dịch như sau:
Ba(NO3)2 \(\rightarrow\) Ba2+ + 2NO-3
0,01M 0,10M 0,20M
HNO3 \(\rightarrow\) H+ + NO-3
0,020M 0,020M 0,020M
KOH \(\rightarrow\) K+ + OH-
0,010M 0,010M 0,010M
b) Các chất điện li yếu phân li không hoàn toàn nên phương trình điện li như sau:
HClO H+ + ClO-
HNO2 H+ + NO-2.

Viết các phương trình phân tử và ion rút gọn (nếu có) xảy ra trong dung dịch giữa các chất sau :
a) Na2CO3 + Ca(NO3)2 -> CaCO3 + 2NaNO3
b) FeSO4 + 2NaOH -> Na2SO4 + Fe(OH)2
c) NaHCO3 + HCl -> H2O + NaCl + CO2
d) NaHCO3 + NaOH -> H2O + Na2CO3
e) K2CO3 + NaCl -> ko có PTHH
g) Pb(OH)2 + 2HNO3 -> 2H2O + Pb(NO3)2
h) Pb(OH)2 + 2NaOH -> Na2\(\left[Pb\left(Oh\right)_4\right]\)
i) CuSO4 + Na2S -> CuS + Na2SO4.

Cho hai giọt dung dịch phenolphtalein vào dung dịch Ca(OH)2 ta thu được dung dịch A có màu hồng.
Dẫn ba chất khí đó lần lượt vào ba ống nghiệm riêng biệt.
Nhỏ vài giọt dung dịch A vào trong ba ống nghiệm đựng CO, HCl, SO2
Nếu có kết tủa trắng và dung dịch mất màu, đó là ống nghiệm đựng SO2.
Nếu dung dịch A mất màu, đó là ống nghiệm đựng HCl.
Nếu màu dung dịch không thay đổi, đó là ống nghiệm đựng CO.
Ngoài ra có thể sử dụng các thuốc thử khác vẫn có thể nhận biết được từng lọ đựng khí.
CHÚC BẠN HỌC TỐT
Cho hai giọt dung dịch phenolphtalein vào dung dịch Ca(OH)2 ta thu được dung dịch A có màu hồng.
Dẫn ba chất khí đó lần lượt vào ba ống nghiệm riêng biệt.
Nhỏ vài giọt dung dịch A vào trong ba ống nghiệm đựng CO, HCl, SO2
Nếu có kết tủa trắng và dung dịch mất màu, đó là ống nghiệm đựng SO2.
Nếu dung dịch A mất màu, đó là ống nghiệm đựng HCl.
Nếu màu dung dịch không thay đổi, đó là ống nghiệm đựng CO.
Ngoài ra có thể sử dụng các thuốc thử khác vẫn có thể nhận biết được từng lọ đựng khí.

Phương trình điện li :
a) K2S → 2K+ + S2_
b) Na2HPO4 → 2Na+ +. HPO42-
HPO42- H+ + PO43-
c) NaH2PO4 → Na+ + H2PO4-
H2PO4- H+ + HPO42-
HPO42- H+ + PO43-
d) Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơ
H2PbO2 2H+ + PbO22- : phân li kiểu axit
e) HBrO H+ + BrO-
g) HF H+ + F-
h) HClO4 → H+ + ClO4-.
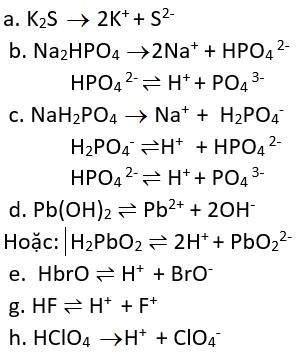
Các axit yếu H2S; H2CO3:
H2S ⇆ H+ + HS-
HS- ⇆ H+ + S2-
H2CO3 ⇆ H+ + HCO3-
HCO3- ⇆ H+ + CO32-