Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Dung dịch thu được có pH = 2 nên H+ dư.
[ H+ ](dư) = 0,01 M ⇒ nH+ (dư) = 0,01(0,1+0,001V) (mol)
Ta có: \(\Sigma n_{OH^-}=2n_{Ba\left(OH\right)_2}+n_{NaOH}=2.0,1.0,1+0,1.0,1=0,03\left(mol\right)\)
\(\Sigma n_{H^+}=2n_{H_2SO_4}+n_{HCl}=2.0,001V.0,0375+0,001V.0,0125=8,75.10^{-5}V\left(mol\right)\)
PT ion: \(OH^-+H^+\rightarrow H_2O\)
______0,03 → 0,03 _________ (mol)
\(\Rightarrow\Sigma n_{H^+}=n_{H^+\left(pư\right)}+n_{H^+\left(dư\right)}\)
\(\Leftrightarrow8,75.10^{-5}V=0,03+0,01\left(0,1+0,001V\right)\)
\(\Rightarrow V=400\left(ml\right)\)
Bạn tham khảo nhé!

nHCl=0,06 mol=nH+
nNaOH= 0,1V mol=nOH-
pHA=4=>H+ dư, [H+] dư =10-4M => nH+ dư= 10-4*(V+0,2)
nH+ bđ= nOH- + nH+ dư
<=> 0,06= 0,1V + 10-4*(V+0,2)
=>V=0,6 (l)

\(n_{OH^-}=0.01\cdot10^{-3}\cdot V\left(mol\right)\)
\(n_{H^+}=0.03\cdot10^{-3}\cdot V\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(n_{H^+\left(dư\right)}=0.03\cdot10^{-3}V-0.01\cdot10^{-3}V=0.02\cdot10^{-3}V\left(mol\right)\)
\(\left[H^+\right]=\dfrac{0.02\cdot10^{-3}}{2}=0.01\cdot10^{-3}=10^{-5}\)
\(pH=-log\left(10^{-5}\right)=5\)

Câu 1: nOH-=0,01V(mol) nH+ =0,03V(mol)
nOH-<nH+ nên axit dư -->nH+dư =0,02V(mol)--->CM H+=0,01(M)=10-2->pH=2
Chú thích do thể tích như nhau nên ko cần đổi
Câu 2:nOH-=0,03a(mol) nH+=0,01a(mol)-->OH-dư
noh-dư=0,02a(mol) mà v=2a-->Cm oh-=0,01=10-2(M)->pH=12
Câu 3:nOH-=0,03 nH+=0,035->H+dư nH+dư=0,005 mol
V=0,5(l) CmH+=10^-2 pH=2

_Dung dịch HCl và HNO3 có pH=1:
=>[H+] = 10^-1 (mol/l)
=>Σ nH{+} = 10^-1*0.1 = 0.01(mol)
+nNaOH = 0.1a (mol)
NaOH => Na{+} + OH{-}
0.1a.........0.1a.......0.1a(mol)
=>nOH{-} = 0.1a (mol)
_Sau phản ứng thu được dung dịch có pH = 12:
+pH = 12:môi trường có tính bazơ => bazơ dư , axit hết.
+pH = 12 => pOH = 14 - 12 = 2 => [OH-] = 10^-2 (mol/l)
=>nOH{-} dư = 10^-2*0.2 = 2*10^-3 (mol)
H{+} + OH{-} => H2O
0.01....0.1a
0.01....0.01........0.01(mol)
..0....0.1a - 0.01.0.01(mol)
=>nOH{-} dư = 0.1a - 0.01 = 2*10^-3 (mol)
<=>0.1a = 0.012
<=>a = 0.12
Vậy a = 0.12 (M)

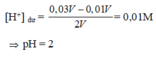
Đáp án A