Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có : nAl = 10,8 / 27 = 0,4 mol ;
nFe3O4 = 34,8 / 232 = 0,15 mol ; n H2 = 10,752 / 22,4 = 0,48 mol
8 Al + 3 Fe3O4 → 4Al2O3 + 9 Fe
8x/3 x 3x
Gọi số mol Fe3O4 phản ứng là x mol
Vì hiệu suất không đạt 100% nên cả Al và Fe3O4 đều chưa phản ứng hết.
⇒ hỗn hợp chất rắn Al dư, Fe3O4 dư , Al2O3 và Fe.
Theo phản ứng :
n Alp/ư = 8x/3 mol ⇒ nAldư = (0,4 - 8x/3) mol
2 Al + 3 H2SO4 → Al2(SO4)3 + 3H2
(0,4 - 8 3 x ) 3 2 0 , 4 - 8 3 x
Fe + H2SO4 → FeSO4 + H2
3x 3x
⇒ 3/2(0,4 - 8x/3) + 3x = 0,48 ⇒ x = 0,12 mol
⇒ H = 0,12/0,15 . 100% = 80%

Phản ứng nhiệt nhôm không hoàn toàn nên ta không thể xác định được rõ sản phẩm Y gồm những chất nào. Ta quy đổi hỗn hợp Y thành X ( theo nguyên BTKL )
=> m = 0,02( 27 + 160) = 3,74 gam
Để đơn giản ta coi hỗn hợp X tác dụng với HNO3 loãng dư:
Các bán phản ứng Oxi hóa - khử:
\(Al\rightarrow Al^{3+}+3e\)
x--------------->3x
\(N^{+5}+3e\rightarrow N^{+2}\)
...........0,06<--0,02
\(\Rightarrow3x=0,06\Rightarrow x=0,02mol\)
\(m=m_{Al}+m_{Fe_2O_3}=27.0,02+160.0,02=3,74\) gam

Xem hỗn hợp ban đầu được tạo thành từ: Fe, Cu và O2
Fe -------> Fe3+ + 3e
x.........................3x
Cu -------> Cu2+ + 2e
y..........................2y
O2 + 4e -----> 2O2-
z.........4z
S+6 + 2e -------> S+4
...........0,045..........0,0225
Gọi x, y, z là số mol Fe, Cu, O2. Ta có hệ gồm 3 pt:
56x + 64y + 32z = 2,44
3x + 2y = 4z + 0,045
0,5*400x + 160y = 6,6
=> x = 0,025, y = 0,01, z = 0,0125
=> %mCu = 0,01*64/2,44*100% = 26,23%
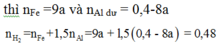
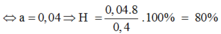

Giải thích:
nAl = 0,4 mol ; nFe3O4 = 0,15 mol
Giả sử H = x
Bd: 0,4 0,15
Pu: 0,4x 0,15x 0,2x 0,45x
Sau: 0,4 – 0,4x 0,45x
nH2 = 1,5nAl + nFe → 0,48 = 1,5(0,4 – 0,4x) + 0,45x
→ x = 0,8
→ H = 80%
Đáp án D