Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Ta có:
\(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\\ n_{Cu}=\dfrac{64}{64}=1\left(mol\right)\\ n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
b) Ta có:
Thể tích của 0,175 mol CO2 (ở đktc):
\(V_{CO_2\left(đktc\right)}=0,175.22,4=3,92\left(l\right)\)
Thể tích của 1,25 mol H2 (ở đktc):
\(V_{H_2\left(đktc\right)}=1,25.22,4=28\left(l\right)\)
Thể tích của 3 mol N2 (ở đktc):
\(V_{N_2\left(đktc\right)}=22,4.3=67,2\left(l\right)\)
c) Ta có: \(n_{CO_2}=\dfrac{0,44}{44}=0,01\left(mol\right)\\ n_{H_2}=\dfrac{0,04}{2}=0,02\left(mol\right)\\ n_{N_2}=\dfrac{0,56}{28}=0,02\left(mol\right)\)
Số mol hỗn hợp: \(n_{hh}=0,01+0,02+0,02=0,05\left(mol\right)\)
Thể tích hỗn hợp (đktc):\(V_{hh}=0,01.22,4+0,02.22,4+0,02.22,4=1,12\left(l\right)\)
a)
nFe = = 0,5 mol
nCu = = 1 mol
nAl = = 0,2 mol
b) Thể tích khí ở đktc:
= 22,4 . 0,175 = 3,92 lít
= 22,4 . 1,25 = 28 lít
= 22,4 . 3 = 67,2 lít
c) Số mol và thể tích của hỗn hợp:
=
= 0,01 mol;
= 22,4 . 0,01 = 0,224 lít
=
= 0,02 mol;
= 22,4 . 0,2 = 0,448 lít;
=
= 0,02 mol;
= 22,4 . 0,02 = 0,448 lít.
Vậy số mol của hỗn hợp là:
nhh = 0,01 + 0,02 + 0,02 = 0,05 mol
Thể tích hỗn hợp là:
Vhh = 0,224 + 0,448 + 0,448 = 1,12 lít
Hoặc Vhh = 0,05 . 22,4 = 1,12 lít

Trước tiên ta cần chuyển đổi khối lượng các khí ra số mol phân tử. Số mol của các chất khí:
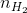 =
=  = 0,5 mol;
= 0,5 mol; 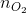 =
= 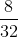 = 0,25 mol
= 0,25 mol
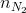 =
= 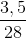 = 0,125 mol;
= 0,125 mol; 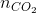 =
= 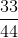 = 0,75 mol.
= 0,75 mol.
Tỉ lệ về số mol các khí cũng là tỉ lệ về thể tích các chất khí ở cùng một điều kiện, ta có sơ đồ biểu diễn:
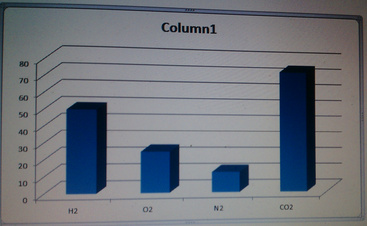

a/ mH2SO4 = 0,05 x 98 = 4,9 gam
b/ nNH3 = 3,36 / 22,4 = 0,15 mol
=> mNH3 = 0,15 x 17 = 2,55 gam
c/ nCaO = \(\frac{0,6.10^{23}}{6.10^{23}}=0,1\left(mol\right)\)
=> mCaO = 0,1 x 56 = 5,6 gam
a, mH2SO4=0.05.98=4.9g chua biết phần b biết vì phải có số mol c,

- Trong các chất khí, hiđro là khí nhẹ nhất. Khí hiđro có tính khử.
- Trong phản ứng giữa H2 và CuO, H2 là chất khử vì chiếm oxi của chất khác; CuO là oxi hóa vì nhường oxi cho chất khác.
Trong các chất khí, hiđro là khí nhẹ nhất. Khí hiđro có tính khử.
Trong phản ứng giữa H2 và CuO, H2 có tính khử vì chiếm oxi của chất khác, CuO có tính oxi hoá vì nhường oxi cho chất khác.

a, nCaCO3=10/100=0,1 mol
PTHH: CaCO3+2HCl---> CaCl2+CO2+H2O
Theo pthh ta có: nCaCl2=nCaCO3=0,1 mol
=> mCaCl2=0,1.111=11,1 (g)
b, nCaCO3=5/100=0,05 mol
Theo pthh ta có : nCO2=nCaCO3=0,05 mol
=> VO2(điều kiện phòng)= 0,05.24= 1,2 l
a) Số mol canxi cacbonat tham gia phản ứng
=
= 0,1 mol
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Theo phương trình hóa học, ta có:
=
= 0,1 mol
Khối lượng của canxi clotua tham gia phản ứng:
= 0,1 . (40 + 71) = 11,1 g
b) Số mol canxi cacbonat tham gia phản ứng:
=
= 0,05 mol
Theo phương trình hóa học, ta có:
=
= 0,05 mol
Thể tích khí CO2 ở điều kiện phòng là:
= 24 . 0,05 = 1,2 lít

a) Trong số các chất khí, khí hiđro nhẹ nhất. Tỉ khối của các khí đối với hiđro:
=
=
= 14, Vậy khí N2 nặng hơn khí H2 14 lần;
=
=
= 16, Vậy O2 nặng hơn khí H2 16 lần;
=
=
= 35,5, Vậy khí Cl2 nặng hơn khí H2 35,5 lần;
=
=
= 14, Vậy khí CO nặng hơn khí H2 14 lần;
=
=
= 32, Vậy khí SO2 nặng hơn khí H2 32 lần;
b) Tỉ khối của các khí đối với không khí:
=
=
≈ 0,966, vậy khí N2; nhẹ hơn không khí 0,966 lần;
=
=
≈ 1,103, vậy khí O2 nặng hơn không khí 1,103 lần;
=
=
≈ 2,448, vậy khí Cl2 nặng hơn không khí 2,448 lần;
=
=
≈ 0,966, vậy khí CO nhẹ hơn không khí 0,966 lần;
=
=
≈ 2,207, vậy khí SO2 nặng hơn không khí 2,207 lần.

a) Ta có: \(n_{CO_2}=\frac{m_{CO_2}}{M_{CO_2}}=\frac{11}{44}=0,25\left(mol\right)\)
\(V_{CO_2}=n_{CO_2}.22,4=0,25.22,4=5,6\left(l\right)\)
b) Ta có: \(n_{Fe_2O_3}=\frac{m_{Fe_2O_3}}{M_{Fe_2O_3}}=\frac{80}{160}=0,5\left(mol\right)\)
a) nCO2 = mCO2 : MCO2 = 11 : 18 = 0,6 (mol)
=> VCO2 = nCO2 * 22,4 = 0,6 * 22,4 = 13,44 (lít)
b) nFe2O3 = mFe2O3 : MFe2O3 = 80 : 160 = 0,5 (mol)

Bài 1:
\(n_{C_4H_{10}}=\frac{m}{M}=\frac{11,6}{58}=0,2mol\)
PTHH: \(2C_4H_{10}+13O_2\rightarrow^{t^o}8CO_2\uparrow+10H_2O\)
0,2 1,3 0,8 1 mol
\(\rightarrow n_{O_2}=n_{C_4H_{10}}=\frac{13.0,2}{2}=1,3mol\)
\(V_{O_2\left(ĐKTC\right)}=n.22,4=1,3.22,4=29,12l\)
\(\rightarrow n_{CO_2}=n_{C_4H_{10}}=\frac{8.0,2}{2}=0,8mol\)
\(m_{CO_2}=n.M=0,8.44=35,2g\)
\(\rightarrow n_{H_2O}=n_{C_4H_{10}}=\frac{10.0,2}{2}=1mol\)
\(m_{H_2O}=n.M=1.18=18g\)

Theo định luật BTKL ta có :
\(m_{C_2H_2}+m_{H_2}=m+m_y\)
\(\Rightarrow0,06.26+0,04.2=m+0,02.0,5.32\)
\(\Rightarrow m=1,32g\)

PTHH: 2H2 + O2 -to-> 2H2O
Ta có: \(\dfrac{8,4}{2}>\dfrac{2,8}{1}\)
=> H2 dư, O2 hết nên tính theo \(V_{O_2}\)
Theo PTHH và đề bài, ta có:
\(m_{H_2O}=2.\dfrac{2,8}{22,4}.18=4,5\left(g\right)\)


c)
\(n_{H_2}=\dfrac{m}{M}=\dfrac{13,2}{2}=6,6\left(mol\right)\)
d)
\(n_{SO_2}=\dfrac{m}{M}=\dfrac{12,8}{32+16\cdot2}=0,2\left(mol\right)\)
đề cho khối lượng thì tính số mol của các chất khí ơ dktc là sao vậy bn?=))
cô mình cho đề như vậy mà, chứ mình có biết đâu