Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

NaHCO3 + HCl → CO2↑ + H2O + NaCl
HCO3− + H+ → CO2↑ + H2O
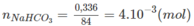
Theo phản ứng cứ 1 mol N a H C O 3 tác dụng với 1 mol HCl và tạo ra 1 mol C O 2 . Từ đó :
Thể tích HCl được trung hoà :
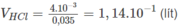
Thể tích khí C O 2 tạo ra :
V C O 2 = 4.10−3.22,4 = 8,96.10−2 (lít).

- Xét phản ứng giữa OH- và H+:
pH = 13 > 7 → Bazo còn dư
→ pOH = 14 - 13 = 1 → [OH-] = 0,1 M
→ nOH- dư = 0,1.0,5 = 0,05 mol
nH+ = nHCl + nHNO3 = 0,04 + 0,06 = 0,1 mol
PT ion: H+ + OH- → H2O
Bđ:___0,1___x
Pư:___0,1___0,1
Sau:___0___x-0,1
→ nOH- dư = x - 0,1 = 0,05 → x = 0,15 mol
- Xét phản ứng của X với H2O dư:
2X + 2nH2O → 2X(OH)n + nH2 → nOH- = 2nH2
X2On + nH2O → 2X(OH)n → nOH- = 2nO
Vậy nOH- = 2nH2 + 2nO → 0,15 = 2.0,015 + 2.nO
→ nO = 0,06
→ mO = 0,06.16 = 0,96 gam
Do O chiếm 10% hỗn hợp → m = 9,6 gam

_Dung dịch HCl và HNO3 có pH=1:
=>[H+] = 10^-1 (mol/l)
=>Σ nH{+} = 10^-1*0.1 = 0.01(mol)
+nNaOH = 0.1a (mol)
NaOH => Na{+} + OH{-}
0.1a.........0.1a.......0.1a(mol)
=>nOH{-} = 0.1a (mol)
_Sau phản ứng thu được dung dịch có pH = 12:
+pH = 12:môi trường có tính bazơ => bazơ dư , axit hết.
+pH = 12 => pOH = 14 - 12 = 2 => [OH-] = 10^-2 (mol/l)
=>nOH{-} dư = 10^-2*0.2 = 2*10^-3 (mol)
H{+} + OH{-} => H2O
0.01....0.1a
0.01....0.01........0.01(mol)
..0....0.1a - 0.01.0.01(mol)
=>nOH{-} dư = 0.1a - 0.01 = 2*10^-3 (mol)
<=>0.1a = 0.012
<=>a = 0.12
Vậy a = 0.12 (M)

Ta có: nC3H5(OH)3 = 28 mol
=> nCu(OH)2 = 1/2 nC3H5(OH)3 = 0,14 mol
=> mCu(OH)2 = 13,72 (g)

_Dung dịch HCl và HNO3 có pH=1:
=>[H+] = 10^-1 (mol/l)
=>Σ nH{+} = 10^-1*0.1 = 0.01(mol)
+nNaOH = 0.1a (mol)
NaOH => Na{+} + OH{-}
0.1a.........0.1a.......0.1a(mol)
=>nOH{-} = 0.1a (mol)
_Sau phản ứng thu được dung dịch có pH = 12:
+pH = 12:môi trường có tính bazơ => bazơ dư , axit hết.
+pH = 12 => pOH = 14 - 12 = 2 => [OH-] = 10^-2 (mol/l)
=>nOH{-} dư = 10^-2*0.2 = 2*10^-3 (mol)
H{+} + OH{-} => H2O
0.01....0.1a
0.01....0.01........0.01(mol)
..0....0.1a - 0.01.0.01(mol)
=>nOH{-} dư = 0.1a - 0.01 = 2*10^-3 (mol)
<=>0.1a = 0.012
<=>a = 0.12
Vậy a = 0.12 (M)

_Dung dịch HCl và HNO3 có pH=1:
=>[H+] = 10^-1 (mol/l)
=>Σ nH{+} = 10^-1*0.1 = 0.01(mol)
+nNaOH = 0.1a (mol)
NaOH => Na{+} + OH{-}
0.1a.........0.1a.......0.1a(mol)
=>nOH{-} = 0.1a (mol)
_Sau phản ứng thu được dung dịch có pH = 12:
+pH = 12:môi trường có tính bazơ => bazơ dư , axit hết.
+pH = 12 => pOH = 14 - 12 = 2 => [OH-] = 10^-2 (mol/l)
=>nOH{-} dư = 10^-2*0.2 = 2*10^-3 (mol)
H{+} + OH{-} => H2O
0.01....0.1a
0.01....0.01........0.01(mol)
..0....0.1a - 0.01.0.01(mol)
=>nOH{-} dư = 0.1a - 0.01 = 2*10^-3 (mol)
<=>0.1a = 0.012
<=>a = 0.12
Vậy a = 0.12 (M)

M g ( O H ) 2 + 2HCl → M g C l 2 + 2 H 2 O
58 g ← 2 mol
Số mol HCl cần trung hoà:
Khối lượng M g ( O H ) 2 đã phản ứng:
1 ml sữa magie có 0,08 g M g ( O H ) 2 .
Vậy thể tích sữa magie chứa 0,8 g M g ( O H ) 2 :
Thể tích sữa magie cần dùng là 10 ml.