Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

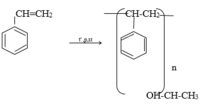
Khác với ankan là phân tử chỉ chứa liên kết σ, phân tử anken có chứa 1 liên kết \(\pi\) kém bền, dễ gẫy, do đó không giống với ankan là cho phản ứng thế là phản ứng đặc trưng, anken cho phản ứng cộng là phản ứng đặc trưng,
Ví dụ:
C2H4 + H2\(\rightarrow\)C2H6 (xúc tác : Ni)
C2H4 + Br2\(\rightarrow\)C2H4Br2
C2H4 + HBr\(\rightarrow\)C2H5Br
Ngoài ra anken còn cho phản ứng trùng hợp phản ứng làm mất màu dung dịch thuốc tím.
Ví dụ :

∗ So sánh tính chất hóa học anken và ankin:
- Giống nhau :
+ Cộng hiđro.
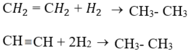
+ Cộng brom (dung dịch).
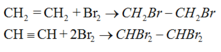
+ Cộng HX theo quy tắc Mac-côp-nhi-côp.
+ Làm mất màu dung dịch KMnO4.
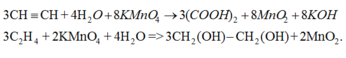
- Khác nhau :
+ Anken : Không có phản ứng thế bằng ion kim loại.
+ Ankin : Ank-1-in có phản ứng thế bằng ion kim loại.
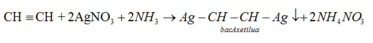

Lời giải:
* So sánh tính chất hóa học anken và ankin:
- Giống nhau :
+ Cộng hiđro.
+ Cộng brom (dung dịch).
+ Cộng HX theo quy tắc Mac-côp-nhi-côp.
+ Làm mất màu dung dịch KMnO4.
- Khác nhau :
+ Anken : Không có phản ứng thế bằng ion kim loại.
+ Ankin : Ank-1-in có phản ứng thế bằng ion kim loại.
* So sánh tính chất hóa học ankan với ankylbenzen:
- Giống nhau :
+ Phản ứng thế (halogen).
+ Phản ứng oxi hóa .
- Khác nhau :
+ Ankan : Phản ứng tách .
+ Ankylbenzen : Phản ứng cộng.

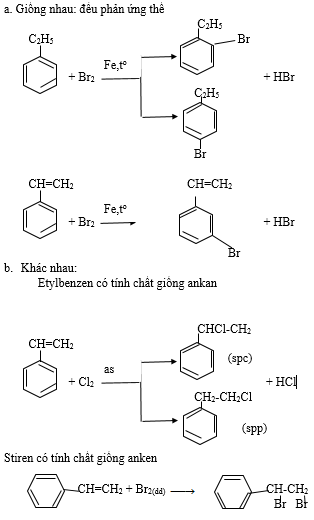
a. Giống nhau: đều phản ứng thế
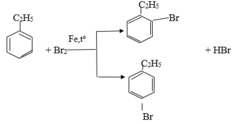
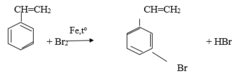
b. Khác nhau:
Etylbenzen có tính chất giống ankan
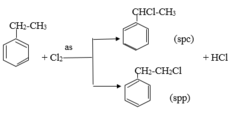
Stiren có tính chất giống anken
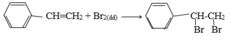

Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi có ít nhất một trong các điều kiện sau:
- Tao thành chất kết tủa
Ví dụ: AgNO3 + NaCl \(\rightarrow\)AgCl\(\downarrow\)+ NaNO3
- Tạo thành chất điện li yếu
Ví dụ: CH3COONa + HCl \(\rightarrow\) CH3COOH + NaCl
- Tạo thành chất khí
Ví dụ: Na2CO3 + H2SO4 -> Na2SO4 + CO2\(\uparrow\) + H2O
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất một trong các chất sau :
- Chất kết tủa :
Ví dụ: AgNO3+HCl→AgCl↓+HNO3AgNO3+HCl→AgCl↓+HNO3
- Chất điện li yếu :
Ví dụ : HCl+CH3COONa→CH3COOH+NaClHCl+CH3COONa→CH3COOH+NaCl
- Chất khí:
Ví dụ: 2HCl+Na2CO3→2NaCl+CO2↑+H2O
bạn xem thêm tại link này nhé: https://cunghocvui.com/bai-viet/bai-1-trang-20-sach-giao-khoa-hoa-11.html

- Tạo thành chất kết tủa: NH4Cl + AgNO3 → NH4NO3 + AgCl\(\downarrow\)
Ag+ + cl‑ \(\rightarrow\) AgCl\(\downarrow\)
- Tạo thành chất điện li yếu: NaOH + HCl \(\rightarrow\)NaCl + H2O
H+ + OH– \(\rightarrow\) H2O
- Tạo thành chất khí: K2CO3 + 2HCl \(\rightarrow\) 2KCl + CO2\(\uparrow\) + H2O
2H+ + CO32– → CO2\(\uparrow\) + H2O
- Tạo thành chất kết tủa: NH4Cl + AgNO3 \(\rightarrow\) NH4NO3 + AgCl\(\downarrow\)
Ag+ + cl‑ → AgCl\(\downarrow\)
- Tạo thành chất điện li yếu: NaOH + HC1 \(\rightarrow\)NaCl + H2O
H+ + OH– \(\rightarrow\)H2O
- Tạo thành chất khí: K2CO3 + 2HC1 \(\rightarrow\) 2KC1 + CO2\(\uparrow\) + H2O
2H+ + CO32– \(\rightarrow\) CO2\(\uparrow\) + H2O

Theo thuyết A-rê-ni-ut thì:
– Axit là chất khi tan trong nước phân li ra cation H+
Ví dụ: HCl → H+ + Cl–
– Bazơ là chất khi tan trong nước phân li ra anion OH–
Ví dụ : NaOH → Na+ + OH–
– Hiđroxit lưỡng tính là hiđroxit khi tan trong nước vừa có thể phân li như axit, vừa có thể phân li như bazơ.
Zn(OH)2 ⇔ Zn2+ +20H– ; Zn(OH)2 ⇔ ZnO2-2 + 2H+
2. Những axit mà tan trong nước phân li nhiều nấc ra ion H+ gọi là các axit nhiều nấc.
Ví dụ : H2SO4, H3PO4….
Những bazơ khi tan trong nước phân li nhiều nấc ra ion OH– gọi là các bazơ nhiều nấc. Ví dụ : Mg(OH)2, Ca(OH)2,….
3. Muối là hợp chất, khi tan trong nước phân li ra cation kim loại (hoặc cation NH4+) và anion gốc axit. Ví dụ : Na2CO3 → 2Na+ + CO32-
Muối trung hòa là muối mà anion gốc axit không có khả năng phân li ra ion H+. Muối axit là muối mà anion gốc axit có khá năng phân li ra ion H+.
Sự điện li cùa muối trong nước tạo cation kim loại (hoặc NH4+ , ion phức) và anion gốc axil.

Cho hai giọt dung dịch phenolphtalein vào dung dịch Ca(OH)2 ta thu được dung dịch A có màu hồng.
Dẫn ba chất khí đó lần lượt vào ba ống nghiệm riêng biệt.
Nhỏ vài giọt dung dịch A vào trong ba ống nghiệm đựng CO, HCl, SO2
Nếu có kết tủa trắng và dung dịch mất màu, đó là ống nghiệm đựng SO2.
Nếu dung dịch A mất màu, đó là ống nghiệm đựng HCl.
Nếu màu dung dịch không thay đổi, đó là ống nghiệm đựng CO.
Ngoài ra có thể sử dụng các thuốc thử khác vẫn có thể nhận biết được từng lọ đựng khí.
CHÚC BẠN HỌC TỐT
Cho hai giọt dung dịch phenolphtalein vào dung dịch Ca(OH)2 ta thu được dung dịch A có màu hồng.
Dẫn ba chất khí đó lần lượt vào ba ống nghiệm riêng biệt.
Nhỏ vài giọt dung dịch A vào trong ba ống nghiệm đựng CO, HCl, SO2
Nếu có kết tủa trắng và dung dịch mất màu, đó là ống nghiệm đựng SO2.
Nếu dung dịch A mất màu, đó là ống nghiệm đựng HCl.
Nếu màu dung dịch không thay đổi, đó là ống nghiệm đựng CO.
Ngoài ra có thể sử dụng các thuốc thử khác vẫn có thể nhận biết được từng lọ đựng khí.
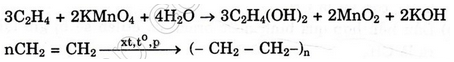
∗ So sánh tính chất hóa học ankan và ankybenzen:
- Giống nhau:
+ Phản ứng thế (halogen):
CH4 + Cl2 → CH3Cl + HCl
+ Phản ứng oxi hóa:
CH4 + 2O2 → CO2 +2H2O
C7H8 + 8O2 → 7CO2 + 4H2O
- Khác nhau:
+ Ankan: có phản ứng tách
C2H6 -500oC, xt→ CH2 = CH2 + H2
+ Ankylbenzen: có phản ứng cộng