Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cái nguyên tử X mình làm ko ra bạn xem lại đề cái 53,125 nếu là 53,125% thì bạn giải ra đươc p = 16 và n = 17 đó là lưu huỳnh ( ra nghiệm đẹp mình nghĩ là đúng )
Ta có 2p + n = 8 và n = 52,63/100 . ( p + n ) từ hệ trên bạn giải ra p = 9 và n = 10 đó là Flo

a) Từ kí hiệu ta thấy nguyên tử Ar có số đơn vị điện tích hạt nhân là 18; vậy Ar có 18 prôtn, 18 electron và có 40-18= 22 nơtron
b) Lớp vỏ electron của nguyên tử có 18e được phân bố như sau : 1s2 2s2 2p6 3s2 3p6.

Bài 1
a) ta có
2p+n=40=>n=40-2p
Mặt khác
\(p\le n\le1,5p\)
=> p\(\le40-2p\le1,5p\)
=>3p\(\le40\le3,5p\)
=>11,42\(\le p\le13,33\)
=> p=12=e => n=16 (loại do 12+ 16=28)
p=13---->n=14(nhận)
b) làm tương tự nhé

MX: \(\left\{{}\begin{matrix}2Z+N=84\\2Z-N=28\end{matrix}\right.\)⇔ \(\left\{{}\begin{matrix}Z=28\\N=28\end{matrix}\right.\)
⇒\(Z_M+Z_X=28\left(1\right)\)
Ta có : \(2Z_M-2-2Z_X-2=20\)
⇔ \(2Z_M-2Z_X=24\) (2)
Từ (1) và (2)⇒ \(\left\{{}\begin{matrix}Z_M+Z_X=28\\2Z_M-2Z_X=24\end{matrix}\right.\)
⇔\(\left\{{}\begin{matrix}Z_M=20\\Z_X=8\end{matrix}\right.\)
⇒ M là Canxi , X là Oxi
⇒ \(A_M\)= 40 , \(A_X\)= 16
Vậy công thức phân tử của A là CaO

Các electron của nguyên tử nguyên tố X được phân bố trên 3 mức năng lượng, lớp thứ 3 có 6 electron, như vậy có sự phân bô” như sau: ls2 2s2 2p6 3s2 3p4
Số đơn vị điện tích hạt nhân của nguyên tử X là 16+
Các electron của nguyên tử nguyên tố X được phân bố trên 3 lớp, lớp thứ ba có 6 electron.
=> Sự phân bố electron trong nguyên tử là: 1s2 2s2 2p6 3s2 3p4 ( Lớp 1 có 1 phân lớp chứa đủ 2 e, lớp 2 có 2 phân lớp chứa đủ 8 e, lớp 3 phân lớp s chứa đủ 2e => lớp p chứa: 6 (số e lớp thứ 3) - 2 (số e phân lớp s trong lớp thứ 3) = 4e )
Vậy nguyên tử nguyên tố X có 16 electron
=> Số đơn vị điện tích hạt nhân của nguyên tử X là 16+ ( số p = số e )
Nguyên tố X là lưu huỳnh ( S )

1.
a) Gọi p là số proton của nguyên tố X
Đồng vị X1 có 3 loại hạt bằng nhau nên 3p = 18 suy ra p = 6
Đồng vị X2 có tổng số hạt 20 nên 2p + n’ = 20 suy ra n’ = 8
Số khối của các đồng vị X1, X2 lần lượt là 12, 14
Phần trăm hai đồng vị bằng nhau suy ra mỗi đồng vị chiếm 50%
Atb = (12.50 + 14.50) / 100 = 13 đvC
b)
Gọi số khối của hai đồng vị X, Y là A1 và A2; phần trăm số nguyên tử của hai đồng vị này là x1 và x2. Theo giả thiết ta có:
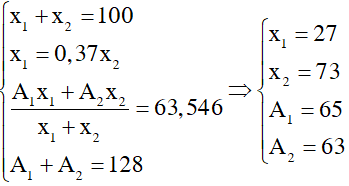
1
a , các loại hạt trong X1 bằng nhau <=> p=n1=e=6 (hạt) => A1 = 12
=> n2 = 20-6.12=8(hạt) => A2 = 8+6=14
%X1 = %X2 = 50%
\(\overline{\text{A}}=\frac{14.50+12.50}{100}=13\)
2 , gọi 2 đồng vị A1p Y và A2p Z , phần trăm của 2 đồng vị lần lượt la x1 , x2
Theo bài ra
A1 + A2 =128
x1 + x2 = 100
\(\overline{M}=\frac{A_1x_1+A_2x_2}{100}=\) 63,54
x1 - 0,37x2 = 0
=> A1 = 65 , A2 = 63
P + N + E = 58 => 2P + N = 58 (vì P=E)
Lại có N-P=1 (chú ý N luôn lớn hơn hoặc bằng P)
=> P=19 => Số hiệu nguyên tử của X là 19
Đáp án A