Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sắt (III) sunfat + Natri hidroxit →Sắt (III) hidroxit + natri sunfat
Áp dụng ĐLBTKL, ta có :msắt (III) sunfat + mnatri hidroxit = msắt (III) hidroxit + mnatri sunfat
mnatri hidroxit = msắt (III) hidroxit + mnatri sunfat - msắt (III) sunfat
= 10,7 + 21,3 – 20 = 12 (gam).
Những câu nào có trên mạng thì mk tham khảo nha k phải làm lai nx
PTHH: Fe2(SO4)3 + NaOH ----> Fe(OH)3↓ + Na2SO4
Theo định luật bảo toàn khối lượng và PTHH, ta có:
mFe2(SO4)3 + mNaOH = mFe(OH)3 + mNa2SO4
=> Khối lượng NaOH đã phản ứng là:
mNaOH = ( mFe(OH)3 + mNa2SO4 ) - mFe2(SO4)3
= (10,7+21,3)-20 = 12 (g)
Chúc bạn học tốt!!

Tham khảo :
PTHH :
Fe3O4 + 4CO -----> 3Fe + 4CO2
Fe3O4 + 4H2 -----> 3Fe + 4H2O
Phản ứng đủ
Theo Định luật BTKL ta có :
mFe3O4 + mhh (khí) - mCO2 - mH2O = mFe
=> 139,2 + 36 - 74,4 = mFe
=> 100,8 (g) = mFe
Vậy khối lượng sắt thu được sau phản ứng là 100,8 (g)
Tham khảo:
m_Fe=m=139,2+36-74,4=100,8 gam

Có thể thay bằng cách sau
2Fe(OH)3 + 3H2SO4 --->Fe2(SO4)3 + 6H2O
(Do nếu chỉ thay x, y vào thì không hợp phương trình nên mik thêm vào cả hệ số)

a) Fe2O3 + 3H2 => 2Fe + 3H2O (1:3:2:3) (Phải H2O không cậu? cậu ghi thiếu)
b) 2HgO => 2Hg + O2 (2:2:1)
c) 4Al + 3O2 => 2Al2O3 (4:3:2)
d) Fe2O3 + 6HCl => 2FeCl3 + 3H2O (1:6:2:3)
e) 2KNO3 => 2KNO2 + O2 (2:2:1)
f) N2 + 3H2 => 2NH3 (1:3:2)
g) Fe2O3 + 3CO => 2Fe + 3CO2 (1:3:2:3)
h) P2O5 + 3H2O => 2H3PO4 (1:3:2)
Tỉ lệ dễ thôi, cậu tự tính nhé. Mị làm xong 8 ý mờ cả mắt rồi :v . Tích giùm mị nha, cảm ơn <333
b) 2HgO -> 2Hg+ O2
Tỉ lệ:
Số phâu tử HgO : Số nguyên tử Hg: Số phân tử O2 = 2:2:1

Bài 10: nH2= 0,125 mol
2H2 + O2 → 2H2O
0,125 mol 0,0625 mol 0,125 mol
a) VO2= 0,0625 x 22,4= 1,4 (l) ; mO2= 0,0625 x 32= 2 (g)
b) mH2O= 0,125 x 18 = 2,25 (g)
Bài 11: nH2= 22,4/22,4 = 1 mol; nO2= 16,8/22,4 =0,75 mol
2H2 + O2 → 2H2O
Ban đầu: 1 mol 0,75 mol
PƯ: 1 mol 0,5 mol 1 mol
Còn lại: 0 mol 0,25 mol 1 mol
mH2O= 1 x 18= 18 (g)

Bài 1:
a) Số mol kẽm là:
nZn = m/M = 32,5/65 = 0,5 (mol)
PTHH: Zn + 2HCl -> ZnCl2 + H2↑
--------0,5-----1-------0,5---------0,5--
b) Thể tích H2 ở đktc là:
VH2 = 22,4.n = 22,4.0,5 = 11,2 (l)
c) Khối lượng ZnCl2 tạo thành:
mZnCl2 = n.M = 0,5.136 = 68 (g)
Vậy ...
Bài toán 1: Cho 32,5 gam kẽm tác dụng với dung dịch axit clohiđric dư.
a) Viết PTHH.
b) Tính thể tích khí hiđro sinh ra (đktc)
c) Tính khối lượng lượng muối kẽm clorua tạo thành ?
giải:
a, PTHH: Zn + 2HCl->ZnCl2+H2
Ta có nZn=32,5/65=0,5mol
Theo PTHH ta có nH2=nZn=0,5mol
=>VH2=0,5.22,4=11,2l
c,Theo PTHH ta có nZnCl2=nH2=0,5mol
=>mZnCl2=0,5.136=68g
Cho mik 1 tick đúng nha, đề dài quá nên mình ko làm hết

a. FexOy + (6x-2y) HNO3 = x Fe(NO3)3 + (3x-2y) NO2+(3x-y) H2O
b. MxOy + 2yHCl ---> xMCl 2y/x + yH2O
c. 2yHCl + FexOy → (3x-2y)FeCl2 + yH2O + (2y-2x)FeCl3

CaCO3 + 2HCl -> CaCl2 + CO2 + H2O (1)
2NaOH + CO2 -> Na2CO3 + H2O (2)
nCaCO3=0,15(mol)
nHCl=0,2(mol)
Vì \(\dfrac{0,2}{2}< 0,15\) nên CaCO3 dư
Theo PTHH 1 ta có:
nCO2=\(\dfrac{1}{2}\)nHCl=0,1(mol)
Theo PTHH 2 ta có:
nCO2=nNa2CO3=0,1(mol)
mNa2CO3=106.0,1=10,6(g)
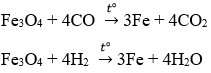
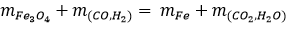

PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)=n_{Fe}\)
\(\Rightarrow n_{Fe_2O_3}=0,15\left(mol\right)\) \(\Rightarrow m_{Fe_2O_3}=x=0,15\cdot160=24\left(g\right)\)