Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: Cu + 2AgNO3 → Cu(NO3)2 + 2Ag ↓
Theo PTHH: 1 mol Cu tác dụng với 2 mol AgNO3 thì khối lượng tăng 152g.
x mol Cu tác dụng với y mol AgNO3 tăng 1,52g.
=> x = 0,02 mol AgNO3.
Nồng độ dung dịch AgNO3: CMAgNO3 = n/V = 0,02/0,02 = 1(M).
Giải cách này nhé:
Cu+2AgNO3\(\rightarrow\)Cu(NO3)2+2Ag
- Gọi số mol Cu phản ứng là x\(\rightarrow\)số mol Ag tạo thành là 2x
- Độ tăng khối lượng lá Cu=khối lượng Ag sinh ra bám vào Cu- khối lượng Cu bị mất đi do phản ứng. Tức là:
108.2x-64x=1,52\(\rightarrow\)152x=1,52\(\rightarrow\)x=0,01mol
Số mol AgNO3=2x=0,02mol
\(C_{M_{AgNO_3}}=\dfrac{n}{v}=\dfrac{0,02}{0,02}=1M\)

Cu → 2Ag
1 2 → mtang = 2.108-64 = 152g
x 2x → mtang = =1,52g
⇒ x = 1,52/152 = 0,01 mol
⇒ n A g N O 3 = n A g = 2x = 0,02 mol
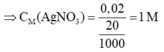
⇒ Chọn C.

Khối lượng thanh sắt tăng 28,8 - 28 = 0,8 gam
PTHH: Fe + CuSO4 ===> FeSO4 + Cu
56 g__ 1 mol_____________64 gam ____ tăng 64 - 56 = 8 gam
5,6 g__0,1 mol____________6,4 gam ____ tăng 6,4 - 5,6 = 0,8 ga,
CM(CuSO4) = 0,1 / 0,25 = 0,4M

Khối lượng thanh sắt tăng: 28,8-28=0,8 g
PT:
Fe + CuSO4 ---> FeSO4 + Cu
56g---1 mol----------------------64g----tăng 64-56=8 g
5,6g---0,1 mol-------------------6,4g---tăng 0,8 g
Nồng độ CM của dd CuSO4:
CM =0,1/0,25=0,4 m

bài 3
Cu +2 AgNO3 -> Cu(NO3)2 + 2Ag
x...............2x.................................2x (mol)
theo bài ta có : 216x-64x=152x=2,28
==> x=0,015 (mol)=> n AgNO3=2x=0,03
==> CMAgNO3 =\(\dfrac{0,03}{\dfrac{30}{1000}}=1\left(M\right)\)
vậy............
bài 1
Zn + CuSO4 -> ZnSO4 + Cu
x x x (mol)
theo bài có 161x-160x=0,2==> x=0,2 = nZn
==> mZn tham gia = 0,2.65=13 (g)
vậy.........

Ta có: mCuSO4=(320x10):100=32g=>nCuSO4=32:160=0...
ptpu: Fe + CuSO4 => FeSO4 + Cu
0,2 0,2 mol 0,2 mol
Độ tăng khối lượng của miếng sắt là: 0,2x(64-56)=1,6g
Theo đề: độ tăng của miếng sắt là 8% nên
1,6g -------> 8%
20g <--------- 100%
Vậy khối lượng miếng sắt ban đầu là 20g
BẠN THAM KHẢO

có n NO = 0,04 mol và dd có axit dư => ko tạo muối amoni
Al : x mol
Fe y mol
=> 27x + 56y = 1,95
3x +3y = 0,04.3
=> x =0,01 , y = 0,03
=> m Al = 0,27g, m Fe = 1,68 g
bạn gọi số mol của Fe(OH)2 : x mol
Fe(OH)3 : y mol
vì sau khi nung chỉ có Fe2O3 và Al2O3
0,015 0,0075
x + y = n Fe = 0,03 mol
n OH- = 4n Al 3+ - n kết tủa
=> 0,165 - 2x -3y = 4.0,03 - 0,015
=> 2x + 3y = 0,06
=> x = 0,03, y = 0 => Al đẩy Fe 3+ xuống Fe 2+ hoàn toàn
=> n Al tác dụng với HNO3 còn lại = 0,01 mol
=> n NO thoát ra = 0,01 mol
=> tổng n NO thoát ra = 0,05 mol
=> n HNO3 = 0,05.4 = 0,2 mol
=> Cm = 1,25 M

Bài tập 2 :
PTHH: \(Cu+2AgNO_3->Cu\left(NO_3\right)_2+2Ag\downarrow\)
Gọi số mol Cu phản ứng là x
\(\Rightarrow Cu\left(pư\right)=64x\left(g\right)\)
Theo PT : \(\Rightarrow Ag\left(pư\right)=2x\left(g\right)\)
Khối lượng lá đồng tăng thêm 1,52g:
Ta có: \(m_{Ag}-m_{Cu\left(pư\right)}=1,52\)
\(\Leftrightarrow2x\times108-64x=1,52\)
\(\Leftrightarrow216x-64x=1,52\)
\(\Rightarrow x=\dfrac{1,52}{152}=0,01\)
\(\Rightarrow n_{AgNO_3}=2x=2.0,01=0,02\left(mol\right)\)
Đổi 20ml = 0,02 l
\(\Rightarrow CM_{AgNO_3}=\dfrac{n}{v}=\dfrac{0,02}{0,02}=1\left(M\right)\)
Cu+ 2agno3= cu(no3)2 +2ag
Số mol cu là x mol nên số mol ag là 2x mol
Khối lượng tăng 1,52=2x. 108-64x
X=0,01 mol nên số mol agno3 là 0,01 mol
Nông độ mol của dd agno3 là 0,01: (20/1000)=0,5(mol/l)
Chọn D.