Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B
Tỉ lệ khối lượng giữa Fe và O là 7/3
=> Đặt khối lượng của Fe là 7 thì khối lượng của O là 3


tồng phần trăm của O và R trong oxit là
3/7% R + 7/7%R =10/7%R
%0 +%R =100%
10/7%R=100%
suy ra R=70%
O%=100% -70% =30%
gọi n là hóa trị của kim loại R thì CT oxit R2On
ta có tỉ lệ khối lượng:
2R/70%=16n /30% ==> R=18.7n
hóa trị của R là 1,2,3. ta xét bảng sau
|
|||||||||||
vậy kim loại phù hợp là Fe
CT của oxit là Fe0

Gọi cthh của oxit là AxOy (x,y là số tự nhiên > 0)
Ta có: \(\dfrac{x.M_A}{y.16}=\dfrac{9}{8}\Leftrightarrow18y=x.M_A\)
TH1: CTHH của oxit là trường hợp đặc biệt Fe3O4
=> \(\dfrac{m_{Fe}}{m_O}=\dfrac{3.56}{4.16}=\dfrac{21}{8}\left(L\right)\)
TH2: CTHH của oxit là A2Oy
=> 9y =MA => y = 3, MA = 27(g/mol) => A là nhôm (Al)
CTHH của oxit là Al2O3

Ta có; \(n_{Al}:n_O=\dfrac{9}{27}:\dfrac{8}{16}=2:3\)
\(\Rightarrow\) CTHH là Al2O3
7.
gọi CTHH của nhôm oxi là \(Al_xD_8\)
có :\(\dfrac{27x}{16y}=\dfrac{9}{8}\)
\(\dfrac{x}{y}=\dfrac{2}{3}\)
\(\rightarrow Al_2O_3\)

Đặt kim loại là M, oxit là MO
Giả sử có 1 mol MO phản ứng, 1 mol H2SO4 phản ứng:
MO + H2SO4 -> MSO4 + H2O
C% = mct / mdd . 100%
10% = 1 . 98 / mdd . 100%
-> mDd H2SO4 = 980 g
Theo định luật bảo toàn khối lượng ta có:
Mdd = mMO + mddH2SO4 = (M + 16) + 980
= M + 996
C%muối = m chất tan muối/ m dd muối . 100%
15.17% = (M + 96) / (M + 996) * 100%
M = 64.95 g
M là Zn
Công thức oxit ZnO

Phân tử khối của Oxi là:
\(2.286\cdot28\simeq64\)
Tỉ lệ khối lượng giữa RxOy với Oxi là 1:1
nên \(\%m_O=50\%\)
=>\(M_O=0.5\cdot64=32\)
Số nguyên tử O là 32/16=2
=>y=2
=>\(R_xO_2\)
Tổng khối lượng phi kim là 64-32=32
Nếu có 1 phân tử phi kim thì R là S
=>Oxit cần tìm là SO2
Nếu có 2 phân tử hoặc 3 phân tử phi kim thì loại
=>Oxit cần tìm là SO2
\(M_{R_xO_y}=d_{R_xO_y}.M_{N_2}=2,286.28=64\) (g/mol)
Mặt khác ta có: \(Rx=16y\)
\(\Leftrightarrow Rx+16y=64\)
\(\Leftrightarrow16y+16y=64\)
\(\Rightarrow y=2\)
\(Rx+16y=64\)
\(\Leftrightarrow Rx+32=64\)
\(\Leftrightarrow Rx=32\)
x=1\(\rightarrow R=32\) (g/mol)
Vậy CTHH là \(SO_2\)

Câu 1 :
\(CT:P_xO_y\)
Ta có :
\(\dfrac{m_P}{m_O}=\dfrac{31}{24}\Rightarrow\dfrac{31x}{16y}=\dfrac{31}{24}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:P_2O_3\)

Gọi công thức 2 oxit là A 2 Ox và A 2 Oy, đồng thời kí hiệu A là nguyên tử khối. Ta có tỉ lệ khối lượng oxi trong 2 oxit là : 50% và 60%. Vậy tỉ lệ khối lượng A trong 2 oxit là 50% và 40%.
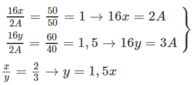
Chỉ có các cặp x, y sau có thể chấp nhận :
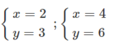
- Nếu chọn x = 2 → ta có 32 = 2A → A = 16 (loại) vì A = 16 là oxi.
- Nếu chọn x = 4 → ta có 64 = 2A → A = 32 → A là lưu huỳnh (S).
Tỉ lệ giữa các nguyên tố là tối giản, ta có hai oxit là : S O 2 và S O 2