Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

Coi hh gồm FeO và Fe2O3
nFeO=x,nFe2O3=y
72x + 160y = 5.36
x=0.01*3 ( bt e)
=> y=0.02
3Fe2+ + 4H+ + NO3- = 3Fe3+ + NO + 2H2O
0.02-----0.08-----0.01
=> nO2-=0.09=> nH+ pứ=0.09*2+0.01*4=0.22 => nH+ dư=0.17
=> nFe3+ = 0.03+0.02*2=0.07
3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO + 4H2O
0.03----0.08----0.02------0.03
Cu + 2Fe3+ =2Fe2+ + Cu2+
0.01--0.02------0.02
Áp dụng đl bt đt
=> nSO42- = (0.04*2 + 0.02*2 + 0.05*3)/2=0.135
=> mM' = 0.04*65 + 0.07*56 + 0.135*96 = 19.44g
=>ACoi hh gồm FeO và Fe2O3
nFeO=x,nFe2O3=y
72x + 160y = 5.36
x=0.01*3 ( bt e)
=> y=0.02
3Fe2+ + 4H+ + NO3- = 3Fe3+ + NO + 2H2O
0.02-----0.08-----0.01
=> nO2-=0.09=> nH+ pứ=0.09*2+0.01*4=0.22 => nH+ dư=0.17
=> nFe3+ = 0.03+0.02*2=0.07
3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO + 4H2O
0.03----0.08----0.02------0.03
Cu + 2Fe3+ =2Fe2+ + Cu2+
0.01--0.02------0.02
Áp dụng đl bt đt
=> nSO42- = (0.04*2 + 0.02*2 + 0.05*3)/2=0.135
=> mM' = 0.04*65 + 0.07*56 + 0.135*96 = 19.44g
=>C

Fe3O4 + 4H2SO4 -> FeSO4 + Fe2(SO4)3 + H2O;
sau đó Fe2(SO4)3 phản ứng với Cu :
Fe2(SO4)3 + Cu-> CuSO4 + 2FeSO4 (1); => dung dịch X chứa CuSO4 và FeSO4, H2SO4 dư
10FeSO4 + 2KMnO4 + 8H2SO4 -> 5Fe2(SO4)3 + 2MnSO4+ K2SO4 + 8H2O;
=> số mol FeSO4 là : 0,05;mà ban đầu ta có 0,02 mol FeSO4; từ (1) => số mol Cu là 0,015 => m= 0,96

A(Fe, S) ==nung==> B(Fe, S, FeS) ==HCl==> C(H2, H2S)
B(Fe, S, FeS) ==nung==> (Fe2O3, SO2)
Bằng phương pháp sơ đồ đường chéo bạn dễ dàng tính được tỉ lệ nH2/nH2S = 1/3
Mà nH2 + nH2S = V
=> nH2 = 0,25V và nH2S = 0,75V
Sau khi viết tất cả các phương trình phản ứng, bạn dễ dàng tính được những kết quả sau :
nFe (trong B) = nH2 = 0,25V mol => mFe = 14V g
nFeS (trong B) = nH2S = 0,75V mol => mFeS = 66V g
Phản ứng của B với O2 :
4FeS + 7O2 = 2Fe2O3 + 4SO2
0,75V....1,3125V mol
S + O2 = SO2
x.....x
Ta có 1,3125V + x = V'' => nS = x = V'' - 1,3125V
=> mS = 32V'' - 42V
mB = mFe + mS + mFeS = 14V + 32V'' - 42V + 66V = 38V + 32V'' g
b. nS = V'' - 1,3125V => V'' > 1,3125V => V''/V > 1,3125

C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag ↓ + 2NH4NO3
C2Ag2 + 2HCl → 2AgCl ↓ + C2H2 ↑
Y(AgCl, Ag) + HNO3 --> ...
Ag + 2HNO3 → AgNO3 + NO2 ↑ + H2O

Gọi số mol K và Al trong hỗn hợp x, y
2K + 2H2O → KOH + H2 (1)
x x (mol)
2Al + 2KOH + 2H2O → 2KAlO2 + 3H2↑ (2)
y y (mol)
Do x tan hết nên Al hết, KOH dư sau (2). Khi thêm HCl, ban đầu chưa có kết tủa vì:
HCl + KOH → KCl + H2O (3)
X – y x – y (mol)
Khi HCl trung hòa hết KOH dư thì bắt đầu có kết tủa:
KAlO2 + HCl + H2O → Al(OH)3 ↓ + KCl (4)
Vậy để trung hòa KOH dư cần 100 ml dung dịch HCl 1M.
Ta có: nHCl = nKOH dư sau phản ứng (2) = x – y = 0,1.1 = 0,1 (mol) (I)
Mặt khác: 39x + 27 y = 10,5 (II)
Từ (1) và (II) => x = 0,2; y = 0,1.
% nK = 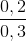 .100% = 66,67%;
.100% = 66,67%;
%nAl = 100% - 66,67% = 33,33%.
K + HOH --> KOH +1/2H2
Al + KOH + HOH --> KAlO2 +3/2H2
-Cho HCl vào bd kg có ket tua => KOH du
HCl + KOH --> KCl + HOH
-Sau đó có ket tua => KOH het => KAlO2 phan ung
KAlO2 + HCl + HOH --> Al(OH)3 + KCl
vì den 100ml dd HCl 1M co xuat hien ket tua nen => n(KAlO2) =n(HCl) = 0,1
=> n(Al) = 0,1
=> %Al = 25,71%
=> %K =74,29%
Luu y: hoi hóa xem bai giai co dung hay co van de nao kg gop ý dum nha thanks

Fe được hòa tan hoàn toàn bởi dd HNO3 thu được dd X, khi thêm HCl vào X có khí NO thoát ra → trong X có ion Fe2+ → HNO3 đã phản ứng hết
n(NO) = 1,12/22,4 = 0,05mol
Fe + 4HNO3 → Fe(NO3)3 + NO + 4H2O
0,05___0,2______________0,05
Fe + 2Fe(NO3)3 → 3Fe(NO3)2
x___________________3x
Theo ĐL bảo toàn nguyên tố, số mol NO3- có trong muối:
n(NO3- trong muối) = n(HNO3) - n(NO) = 0,15mol
n(NaOH) = 0,115.2 = 0,23mol
Sau khi NaOH pư hoàn toàn với các chất trong dd Y, dung dịch thu được có:
n(Na+) = n(NaOH) = 0,23mol; n(Cl-) = n(HCl) = 0,1mol
→ n(NO3-) = n(Na+) - n(Cl-) = 0,23 - 0,1 = 0,13mol
→ Số mol NO3- bị Fe2+ khử: 0,15 - 0,13 = 0,02mol
NO3- + 3Fe2+ + 4H+ → 3Fe3+ + NO + 2H2O
0,02___0,06____0,08
NO3- và H+ đều dư (H+ dư 0,02mol) → Fe2+ đã phản ứng hết → 3x = 0,06 → x = 0,02mol
Tổng số mol Fe: n(Fe) = 0,05 + x = 0,07mol
Khối lượng Fe đã sử dụng: m(Fe) = 0,07.56 = 3,92g

Đáp án : C
Vì Mg và Zn đều có hóa trị 2 nên gọi kí hiệu chung là M
Trước tiên có phương trình ion cho phản ứng với HNO3 như sau
(3b + 8c)/2 M + (b + 2c)N+5 -> (3b + 8c)/2M+2 + bN+2 + 2cN+1
số mol M là (3b + 8c)/2 và số mol HNO3 pư là (b + 2c + 3b + 8c) = 4b + 10c
=> Số mol HNO3 dư là (a – 4b – 10c) mol
Để lượng kết tủa lớn nhất thì NaOH trung hòa hết HNO3 và phần dư có tỉ lệ 2 : 1 với M(NO3)2
=>Số mol NaOH là V = (a - 4b - 10c) + 2.(3b + 8c)/2 = a - b – 2c