Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình điện phân: 4AgNO3 + 2H2O → 4Ag + O2 + 4HNO3 (1)
Dung dịch Y gồm: AgNO3, HNO3. Cho Fe + dd Y sau phản ứng thu được 14,5g hỗn hợp kim loại nên Fe dư có các phản ứng:
3Fe + 8HNO3 → 3Fe(NO3)3 + 2NO + 4H2O (2)
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag (3)
Gọi x là số mol AgNO3 bị điện phân® nHNO3 = x, dung dịch Y: HNO3: x mol; AgNO3 dư: 0,15 –x mol.
Theo (2,3) nFe phản ứng = 3x/8 + (0,15-x)/2 = 0,075 –x/8 mol
nAg = 0,15 – x mol
Vậy mhỗn hợp kim loại = mFedư + mAg =12,6 –(0,075-x/8).56 +(0,15-x).108 =14,5
Suy ra: x= 0,1 mol. Ta có mAg = 0,1.108 ® t = 1,0 h

Chọn B.
Dung dịch X chứa H+(x mol), Fe2+ (y mol), Fe3+ (z mol), Cu2+ (t mol), Cl- (0,6 mol)
![]()
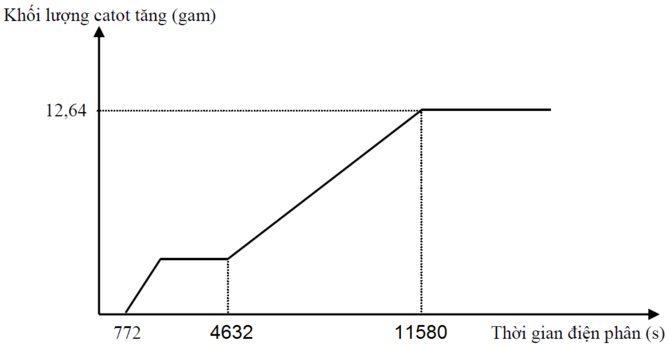
Tại thời điểm t1 = 772 (s): Fe3+ điện phân hết chuyển thành Fe2+ Þ ne (1) = z
Tại thời điểm t2 = 4632 (s): Cu2+, H+ điện phân hết Þ ne (2) = x + z + 2t
Tại thời điểm t3 = 11580 (s): Fe2+ điện phân hết Þ ne (3) = x + 2y + 3z + 2t và 56(y + z) + 64t = 12,64 (2)
+ Với t2 = 6t1 Þ x + z + 2t = 6z (3)
+ Với t3 = 15t1 Þ x + 2y + 3z + 2t = 15z. Thay (1) vào Þ z = 0,04
Từ (1), (2), (3) suy ra: x = 0,12 ; y = 0,14 ; t = 0,04
Khi cho AgNO3 đến dư vào X thì:
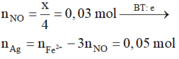
Kết tủa thu được là AgCl (0,6 mol) và Ag (0,03 mol) Þ m = 91,5 (g)

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

nFe = nFeCl3 = 0,06 mol => nO (oxit ) = ( 4 – 0,06.56)/16 = 0,04 mol
Quy đổi 4 gam A thành Fe và O. Cho tác dụng với HNO3 :
Fe à Fe3+ + 3e O + 2e à O2-
0,06 0,18 0,08 0,04
N+5 + 3e àNO => V = 0,1/3.22,4 = 0,747 lit
0,1 0,1/3

Gọi công thức của Oxit Sắt là : \(Fe_xO_y\)
Các PTHH khi X vào HCl :
\(Fe+2HCl\rightarrow FeCl_2+H_2\)(1)
\(Fe_xO_y+2yHCl\rightarrow FeCl_{\frac{2y}{x}}+yH_2O\) (2)
nHCl ban đầu =\(\frac{200.14,6}{100.36,5}=0.8\left(mol\right)\)
\(n_{H_2}=\frac{2,24}{22,4}=0,1\left(mol\right)\Rightarrow m_{H_2}=0,1.2=0,2\left(g\right)\)
Từ (1) \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(\Rightarrow m_{Fe_xO_y}=17,2-5,6=11,6\left(g\right)\Rightarrow n_{Fe_xO_y}=\frac{11,6}{56x+16y}\left(mol\right)\left(3\right)\) Từ (1) \(n_{HCl}=2n_{H_2}=2.0,1=0,2\left(mol\right)\)
\(m_{ddA}=200+17,2-0,2=217\left(g\right)\)
\(m_{ddB}=217+33=250\left(g\right)\)
\(n_{HCldu}=\frac{250.2,92}{100.36,5}=0,2\left(mol\right)\)
\(n_{HCl\left(2\right)}=0,8-0,2-0,2=0,4\left(mol\right)\)
\(n_{Fe_xO_y}=\frac{1}{2y}n_{HCl}=\frac{1}{2y}.0,4=\frac{0,2}{y}\left(mol\right)\)(4)
Từ (3) và (4) ta có pt :\(\frac{11,6}{56x+16y}=\frac{0,2}{y}\Rightarrow\frac{x}{y}=\frac{3}{4}\)
Vậy CT Oxit cần tìm là :Fe3O4

A. 184,1 gam và 91,8 gam.
B. 84,9 gam và 91,8 gam.
C. 184,1 gam và 177,9 gam.
D. 84,9 gam và 86,1 gam.

Bạn bấn vào đây, có người hỏi bài này rồi nhá Câu hỏi của Mạc Nhược Ca - Hóa học lớp 12 | Học trực tuyến
 với các chất sau:
với các chất sau:
Chọn A.
Dung dịch X chứa H+(x mol), Fe2+ (y mol), Fe3+ (z mol), Cu2+ (t mol), Cl- (0,6 mol)
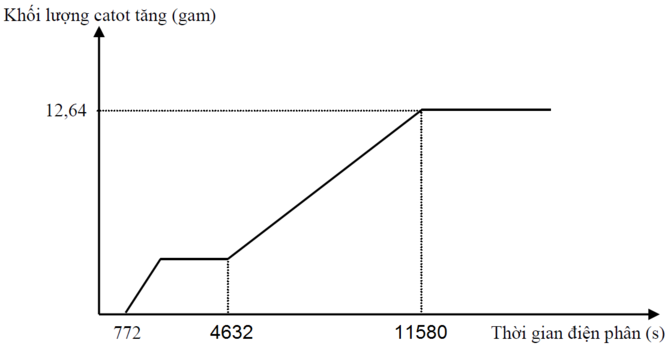
Tại thời điểm t1 = 772 (s): Fe3+ điện phân hết chuyển thành Fe2+ Þ ne (1) = z
Tại thời điểm t2 = 4632 (s): Cu2+, H+ điện phân hết Þ ne (2) = x + z + 2t
Tại thời điểm t3 = 11580 (s): Fe2+ điện phân hết Þ ne (3) = x + 2y + 3z + 2t và 56(y + z) + 64t = 12,64 (2)
+ Với t2 = 6t1 Þ x + z + 2t = 6z (3)
+ Với t3 = 15t1 Þ x + 2y + 3z + 2t = 15z. Thay (1) vào Þ z = 0,04
Từ (1), (2), (3) suy ra: x = 0,12 ; y = 0,14 ; t = 0,04
Khi cho AgNO3 đến dư vào X thì: