Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag ↓ + 2NH4NO3
C2Ag2 + 2HCl → 2AgCl ↓ + C2H2 ↑
Y(AgCl, Ag) + HNO3 --> ...
Ag + 2HNO3 → AgNO3 + NO2 ↑ + H2O

Câu a:
Có 3 dd là: H2O, NaOH, HCl
Cho quỳ tím vào:
\(\rightarrow\) Hóa đỏ: HCl
\(\rightarrow\) Hóa xanh: NaOH
\(\rightarrow\) Không chuyển màu: H2O
Câu b:
Có 4 dd: H2O, Ca(OH)2 (ở dạng dd), H2SO4 loãng, NaCl.
+ Cho quỳ tím vào:
\(\rightarrow\) Hóa xanh: dd Ca(OH)2
\(\rightarrow\) Hóa đỏ: H2SO4 loãng
\(\rightarrow\) Không chuyển màu quỳ tím: H2O và NaCl -----nhóm A
Với nhóm A:
- Cách 1:
Cho dd AgNO3 vào mỗi chất trong nhóm A:
\(\rightarrow\) Tạo kết tủa với AgNO3: NaCl
NaCl + AgNO3 \(\rightarrow\)AgCl\(\downarrow\) + NaNO3
\(\rightarrow\) Không hiện tượng: H2O
Nếu bạn chưa học tới thì có thể dùng cách 2:
- Cách 2:
Lấy ít mẫu thử của H2O và NaCl đun nóng.
\(\rightarrow\) Bay hơi hết : H2O
\(\rightarrow\) Bay hơi còn lại chất rắn kết tinh : NaCl
a, trích 3 mau thử ra 3 ống nghiệm có mẩu quỳ tím
chất lam cho quỳ tím hóa đỏ là HCl
chất lam quý tím xanh la NaOH
còn lại quỳ tím ko đổi mau la H2O

Đáp án B
Các phát biểu đúng (a), (c), (d).
- Do cấu tạo mạch ở dạng xoắn có lỗ rỗng, hồ tinh bột hấp thụ iot cho có màu xanh tím.
- Khi đun nóng, iot thăng hoa, bị giải phóng ra khỏi hồ tinh bột làm mất màu xanh tím.
- Khi để nguội, iot bị hấp thụ trở lại làm dung dịch lại có màu xanh tím.

chộ cái mặt nhà mi là biết rồi , vào trang chủ của tau rồi bấm theo dõi đi

Mg + HCl - MgCl2 + H2
Al + HCl - AlCl3 + H2
còn Cu đứng sau H nên không phản ứng với HCl.
nCuO = \(\dfrac{16}{80}=0,2\) mol
Pt: 2Cu + O2 --to--> 2CuO
0,2 mol<--------------0,2 mol
.....Mg + 2HCl --> MgCl2 + H2
0,2 mol<-----------0,2 mol
.....2Al + 6HCl --> 2AlCl3 + 3H2
....MgCl2 + 2NaOH --> Mg(OH)2 + 2NaCl
...0,2 mol<---------------0,2 mol
....AlCl3 + 3NaOH --> Al(OH)3 + 3NaCl
....Al(OH)3 + NaOH --> NaAlO2 + 2H2O
..........................................(tan)
...Mg(OH)2 --to--> MgO + H2O
0,2 mol<------------ 0,2 mol
nMgO = \(\dfrac{8}{40}=0,2\) mol
mCu = 0,2 . 64 = 12,8 (g)
mMg = 0,2 . 24 = 4,8 (g)
mAl = mhh - mCu - mMg = 20 - 12,8 - 4,8 = 2,4 (g)
% mCu = \(\dfrac{12,8}{20}.100\%=64\%\)
% mMg = \(\dfrac{4,8}{20}.100\%=24\%\)
% mAl = \(\dfrac{2,4}{20}.100\%=12\%\)

nZn = mol, nS =
mol.
Phương trình hóa học của phản ứng:
Zn + S -> ZnS
0,07 0,07 0,07 (mol)
Khối lượng các chất sau phản ứng:
mZn(dư) = (0,01 -0,007).65 = 0,195 gam.
mZnS = 0,007.97 = 0,679g.

Đáp án B
Phát biểu (a) sai vì sau bước 1 thu được chất khí không màu (H2) và dung dịch có màu xanh nhạt (màu của Fe2+).
Phát biểu (b) đúng vì để điều chế được Fe(OH)2 ta phải đẩy lượng khí O2 hòa tan có trong dung dịch NaOH để tránh hiện tượng Fe(OH)2 bị O2 oxi hóa thành Fe(OH)3.
Phát biểu (c) đúng, sau bước 3 ta thu được kết tủa màu trắng hơi xanh Fe(OH)2.
Phát biểu (d) đúng, đến cuối buổi thí nghiệm thì kết tủa Fe(OH)2 có màu trắng xanh sẽ bị O2 trong không khí oxi hóa thành Fe(OH)3 có màu nâu đỏ

Chọn đáp án B.
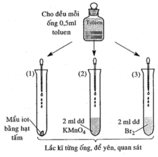
Phân tích tính chất hóa học của toluen (C6H5CH3) va xem xét các phát biểu:
Q A sai vì benzen không phản ứng được với dung dịch thuốc tím (KMnO4) nên ống (2) vẫn có màu tím.
þ B đúng vì benzene là dung môi hữu cơ có thể hòa tan được brom, iot, lưu huỳnh, cao su, chất béo,…
Q C sai vì benzen không phản ứng được với dung dịch Br2 ở điều kiện thường.
Q D sai vì như đã phân tích ở phát biểu A, benzen không phản ứng được với dung dịch (KMnO4).