Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
TH 1: Cả hai muối NaX và NaY đều cho kết tủa khi pư với AgNO3
NaZ + AgNO3 → NaNO3 + AgZ↓
a a
Áp dụng pp tăng giảm khối lượng ![]()
→ a = 0,03 (mol) → MNaZ= 201→ Z = 178
X và Y là I (127) và At (210), nhưng At không có tự nhiên nên TH này loại
TH 2: Chỉ có 1 muối tạo kết tủa nghĩa là hai muối này là NaF và NaCl
nAgCl = 8,61/143,5 = 0,06 mol
NaCl + AgNO3 → NaNO3 + AgCl↓
0,06 0,06
mY = mNaCl = 0,06.58,5 = 3,51g
mX = mNaF = 6,03 - 3,51 = 2,52g
%NaF = ![]() .100% = 41,8%
.100% = 41,8%

Chọn đáp án D
Gỉa sử X không phải Flo
Gọi CTTB của X và Y là X ¯
N a X - + A g N O 3 → A g X - + N a N O 3
23 + X ¯ → 108 + X ¯ (g)
6,03 → 8,61 (g)
8,61.(23 + X ¯ ) = 6,03. (108 + X ¯ )
X ¯ = 175,3 (loại)
X là Flo, Y là Clo
Kết tủa chỉ gồm AgCl; n A g C l = n N a C l = 8,61 : 143,5 = 0,06 mol
% m N a C l = 0 , 06 . 58 , 5 6 , 03 . 100 = 58,2 (%) → % m N a F = 41,8 (%).

TH1: NaX là NaF => NaY là NaCl
Do NaF không tác dụng với AgNO3 nên chỉ có NaCl phản ứng.
Ta có phương trình: NaCl + AgNO3 ===> NaNO3 + AgCl
nAgCl= 0,06(mol)= nNaCl => mNaCl= 3,51(g) => %mNaCl=58,2%=>%mNaF=41,8%
TH2: NaX không phải là NaF.
Gọi công thức chung của 2 muối cần tìm là NaB
Ta có phương trình: NaB+AgNO3==>NaNO3+AgB
nNaB= nAgB=0,06 mol ==> \(\dfrac{6,03}{23+M_B}\) = \(\dfrac{8,61}{108+M_B}\) ==> MB= 175,6
Vậy 2 muối là Iot và Atatin nhưng do Atatin không có trong tự nhiên nên loại.

Giả sử 2 muối NaX và NaY đều cho kết tủa:
Ta có
\(NaM+AgNO_3\rightarrow AgX+NaNO_3\)
\(m_{tang}=\left(108-23\right).n_M=8,61-6,03\)
\(\Rightarrow n_M=0,03\left(mol\right)\)
\(M_M=\frac{6,03}{0,03}-23=175,6\)
Không có một halogen nào thỏa mãn.
Phải có một muối là NaF (AgF không kết tủa), vì là 2 halogen thuộc 2 chu kì liên tiếp nên Y là Cl
\(n_{AgCl}=\frac{8,61}{143,5}=0,06\left(mol\right)\)
\(\Rightarrow n_{NaCl}=0,06\left(mol\right)\)
\(\Rightarrow m_{NaF}=6,03-0,06.58,5=2,52\left(g\right)\)
\(\%m_{NaF}=\frac{2,52}{6,03}.100\%=41,79\%\)

Bài 1
Đặt nCl2 = nBr2 = x (tỉ lệ mol 1:1)
Ta có \(35,5.2x+160x=23,1\)
\(\Leftrightarrow x=1\)
Đặt n(Cl2 phản ứng Fe)=a
n(Cl2 phản ứng Zn)=b
Br2 ko phản ứng Fe
\(2Fe+3Cl_2\rightarrow2FeCl_3\)
2/3a __ a ____________ (mol)
\(Zn+Cl_2\rightarrow ZnCl_2\)
b_____b________(mol)
\(3Br_2+2Fe\rightarrow2FeBr_3\)
0,1____1/15 __________(mol)
Ta có \(65b+56.\left(\frac{2}{3}a+\frac{1}{15}\right)=8,85\)
\(\Leftrightarrow65b+\frac{112}{3a}=\frac{307}{60}\)
Mà \(a+b=0,1\)
\(\rightarrow a=b=0,05\)
\(\rightarrow m_{Fe}=\left(\frac{2}{3}.0,05+\frac{1}{15}\right).56=5,6\left(g\right)\)
\(\Leftrightarrow\%m_{Fe}=\frac{5,6}{8,85}.100\%=63,28\%\)
Bài 2
Đổi 500ml = 0,5l
a)\(MnO_2+HCl\rightarrow Cl_2+H_2O+MnCl_2\)
\(Cl_2+2NaOH\rightarrow H_2O+NaCl+NaClO\)
b)\(n_{MnO2}=\frac{69,6}{87}=0,8\left(mol\right)\)
\(MnO_2+HCl\rightarrow Cl_2+H_2O+MnCl_2\)
0,8_______________0,8_________0,8______(mol)
\(n_{NaOH}=0,5.4=2\left(mol\right)\)
\(PTHH:Cl_2+2NaOH\rightarrow H_2O+NaCl+NaClO\)
Ban đầu__0,8 __ 2 ______________________________ (mol)
Phản ứng_ 0,8 __1,6________________0,8 ____0,8____(mol)
Sau phứng_0_____ 0,4 _______________0,8 ___ 0,8___(mol)
\(n_{Cl2}=0,8< \frac{n_{NaOH}}{2}=1\)
\(\rightarrow\) NaOH dư
Ta có : \(n_{NaOH_{spu}}=0,4\left(mol\right)\)
\(CM_{NaCl}=CM_{NaClO}=CM_{MnO2}=\frac{0,8}{0,5}=1,6M\)
\(CM_{NaOH_{spu}}=\frac{0,4}{0,5}=0,8M\)
Bài 3
\(m_A=37,05-4,8-8,1=24,15\left(g\right)\)
Gọi a; b là mol Cl2; O2
\(\rightarrow71a+32b=24,15\left(1\right)\)
\(n_{Mg}=0,2\left(mol\right)\)
\(n_{Al}=0,3\left(mol\right)\)
Bảo toàn e:
\(2a+4b=0,2.2+0,3.3=1,3\left(2\right)\)
(1)(2) \(\rightarrow\left\{{}\begin{matrix}a=0,25\\b=0,2\end{matrix}\right.\)
\(\%_{Cl2}=\frac{0,25.71}{24,15}.100\%=73,5\%\)
\(\%_{O2}=100\%-73,5\%=26,5\%\)
Bài 4
Giả sử NaX là NaF (ko tạo kết tủa) => NaY là NaCl
\(AgNO_3+NaCl\rightarrow AgCl+NaNO_3\)
\(\rightarrow n_{AgCl}=n_{NaCl}=0,06\left(mol\right)\)
\(\rightarrow m_{NaCl}=3,51\left(g\right)< 6,03\left(g\right)\left[TM\right]\)
\(m_{NaF}=6,03-3,51=2,52\left(g\right)\)
\(\rightarrow\%_{NaF}=\frac{2,52.100}{6,03}=41,8\%\)
- Giả sử cả X và Y cùng tạo kết tủa. Gọi chung X, Y là R
\(NaT+AgNO_3\rightarrow AgR+NaNO_3\)
\(n_{NaR}=n_{AgR}\)
\(\rightarrow\frac{6,03}{23+R}=\frac{8,61}{108+R}\)
\(\Leftrightarrow198,03+8,61R=651,24+6,03R\)
\(\Leftrightarrow R=175,67\)
Vậy X là I, Y là At (loại vì At là nguyên tố phóng xạ nhân tạo)


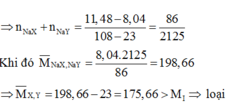
Đáp án C