Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Fe2O3 + 3H2 => 2Fe + 3H2O (1:3:2:3) (Phải H2O không cậu? cậu ghi thiếu)
b) 2HgO => 2Hg + O2 (2:2:1)
c) 4Al + 3O2 => 2Al2O3 (4:3:2)
d) Fe2O3 + 6HCl => 2FeCl3 + 3H2O (1:6:2:3)
e) 2KNO3 => 2KNO2 + O2 (2:2:1)
f) N2 + 3H2 => 2NH3 (1:3:2)
g) Fe2O3 + 3CO => 2Fe + 3CO2 (1:3:2:3)
h) P2O5 + 3H2O => 2H3PO4 (1:3:2)
Tỉ lệ dễ thôi, cậu tự tính nhé. Mị làm xong 8 ý mờ cả mắt rồi :v . Tích giùm mị nha, cảm ơn <333
b) 2HgO -> 2Hg+ O2
Tỉ lệ:
Số phâu tử HgO : Số nguyên tử Hg: Số phân tử O2 = 2:2:1

C1:
1/ a) C2H5OH + K --> C2H5OK + 1/2H2
K + H2O --> KOH + 1/2H2
b) Thể tích rượu etylic nguyên chất có trong 300ml cồn 92o:
Vr= 92*300/100=276 ml
Thể tích rượu 23o thu được:
Vr=276*100/23=1200ml
2/
a) A: C2H5OH
CH3-CH2-OH
B: CH3COOH
CH3-COOH
b) C2H4 + H2O -axit-> C2H5OH
C2H5OH + O2 -mg-> CH3COOH + H2O
nC2H4= 2.24/22.4=0.1 (mol)
Cứ 1 mol etilen chuyển hóa thành rượu tạo thành 1 mol axit
=> nCH3COOH= 0.1 (mol)
Vì: H=60% nên:
nCH3COOH (tt)= =0.1*60/100=0.06 (mol)
mCH3COOH= 0.06*60=3.6g
3/ Áp dụng đl BTKL có:
m= 4.29+0.6-0.184=4.696g
4/
n CO2= 44/44=1 (mol) => nC = 1 => mC= 12g
nH2O= 27/18=1.5 (mol) => nH = 3 mol
mO= 23-12-3= 8 (g)
nO= 0.5 (mol)
Gọi: CT là : CxHyOz
x : y : z= 1: 0.3: 0.5= 2: 6 :1
Vậy CT nguyên: (C2H6O)n
<=> 46n= 46
=> n=1
Vậy CTPT của A: C2H6O

Bài 1:
a) Số mol kẽm là:
nZn = m/M = 32,5/65 = 0,5 (mol)
PTHH: Zn + 2HCl -> ZnCl2 + H2↑
--------0,5-----1-------0,5---------0,5--
b) Thể tích H2 ở đktc là:
VH2 = 22,4.n = 22,4.0,5 = 11,2 (l)
c) Khối lượng ZnCl2 tạo thành:
mZnCl2 = n.M = 0,5.136 = 68 (g)
Vậy ...
Bài toán 1: Cho 32,5 gam kẽm tác dụng với dung dịch axit clohiđric dư.
a) Viết PTHH.
b) Tính thể tích khí hiđro sinh ra (đktc)
c) Tính khối lượng lượng muối kẽm clorua tạo thành ?
giải:
a, PTHH: Zn + 2HCl->ZnCl2+H2
Ta có nZn=32,5/65=0,5mol
Theo PTHH ta có nH2=nZn=0,5mol
=>VH2=0,5.22,4=11,2l
c,Theo PTHH ta có nZnCl2=nH2=0,5mol
=>mZnCl2=0,5.136=68g
Cho mik 1 tick đúng nha, đề dài quá nên mình ko làm hết

Tham khảo:
Gọi số mol Cl2 là a, số mol O2 là b. Theo bài ra ta có hệ PT:
Giải hệ tìm được a = 0,1; b = 0,2 .
Gọi nAl = x, nZn=y (mol)
Sử dụng định luật bảo toàn electron: 3x + 2y = 0,2.4 + 0,1.2 = 1 (1)
Áp dụng bảo toàn khối lượng:
m = 31,9 - 45.0,3 = 18,4 gam nên 27x + 65y = 18,4 (2)
Giải hệ được: x = 0,2 và y = 0,2 → %mAl = 29,35%; %mZn= 70,65%

a. Cân bằng pthh
Zn + 4 HNO3 à z = Zn(NO3 )2 + 2NO2 + 2 H2O
b. Số mol của Zn là 13/65 = 0,2 mol
Số mol của HNO3 là 0,4. 2,5 = 1 mol
Theo ptpu thì Zn phản ứng hết -> Số mol NO2 = 2. Số mol Zn = 0,4 mol.
VNO2 = 8,96 lit
Tham khảo
Câu 1:
Cho PTH H
a)Zn + 4HNO3 → Zn(NO3)2 + 4NO2 + 2H2O
b) Ta có
n\(_{Zn}=\frac{13}{65}=0,2\left(mol\right)\)
n\(_{HNO3}=0,4.2,5=1\left(mol\right)\)
=>HNO3 dư
Theo pthh
nNO2 =2n\(_{Zn}=0,4\left(mol\right)\)
V\(_{NO2}=0,4.22,4=\)8,96(l)
Chúc bạn học tôts

câu 5:
2Al + 6HCl -> 2AlCl3 + 3H2
4P + 5O2 -> 2P2O5
Fe3O4+ 4H2 -> 3Fe + 4H2O
BaO + H2O -> BaOH
Câu 6:
Trích mẫu thử
Cho nước vào các mẫu thử
tan=>P2O5,Na2O
Không tan=>MgO
pt:P2O5+3H2O--->2H3PO4
Na2O+H2O--->2NaOH
Cho quỳ tím vào
Quỳ tím chuyển thành màu xanh=>NaOH
_____________________đỏ=>H3PO4

a, 4Al+3O2-> 2Al2O3
b, 3H2O +P2O5 -> 2H3PO4
c, 2K+ 2H2O -> 2KOH + H2
d, K2O + H2O -> 2KOH
e, KMnO4 -> K2MnO4 + MnO4 + O2
g, CuO+ H2-> Cu+H2O
h, FexOy+H2-> xFe +yH2O


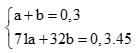
Các nguyên tử có cùng số proton thì thuộc cùng 1 nguyên tố hóa học
Suy ra :
X,Z thuộc cùng 1 nguyên tố hóa học
Y,T,G thuộc cùng 1 nguyên tố hóa học