Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nOH- = 0,04 mol
Vì nAlO2- = 0,02 mol mà chỉ thu được 0,01 mol kết tủa nên nHCl = 4n kết tủa + nAlO2- dư = 0,05 mol
=> tổng nH+ = 0,09 mol => V = 45ml
Vậy : B đúng
H+ + OH- => H2O 1
0,02......0,02
H+ + AlO2 - + H2O => Al(OH)3 2
0,02.....0,02.........................0,02
3H+ + Al(OH)3 => Al3+ +3H2O 3
0,03.........0,01
do cần V lớn nhất nên xét TH tạo kết tủa xong hòa tan 1 phần kết tủa
n Al(OH)3 =0,01 => nAl(OH)3 ở 3 =0,01
=> nHCl= 0,03 +0,02 +0,02 =0,07 => V=0,035 => C

Al(x) Na(2x)
Na+H2O->NaOH + H2
2x -> 2x
Al + NaOH + H2O ->
x -> x
nNaOH dư x
NaOHdư + CuCl2 -> NaCl + Cu(OH)2
0,025 <- 0,025
NaOHdư + HCl -> ...
0,05 <- 0,05
----> nNaOH = (0,025.2 + 0,5).2 = 0,2
nAl = 0,1

Cho m gam hỗn hợp X gồm ( Fe , FeO , Fe2O3 ) có tỷ lệ khối lượng tương ứng là 7:18:40 .Hỗn hợp X tan vừa hết trong 500 ml H2SO4 loãng 0,68 M thu được dung dịch B và thoát ra V lít khí H2 ( đktc). Cho dung dịch B tác dụng NaOH dư lọc kết tủa nung khô trong không khí thu được 22,4 gam chất rắn. Giá trị của V là ?
A. 0,448
B. 0,896
C. 2,24
D. 1,12

Đáp án D
► Bảo toàn electron: 3nAl = 2nH2 ⇒ nAl = 0,02 mol.
"vừa đủ" ⇒ X chỉ chứa AlCl3 || 0,09 mol hay 0,13 mol NaOH cho cùng 1 lượng ↓
⇒ 0,09 mol NaOH thì ↓ chưa đạt cực đại và 0,13 mol NaOH thì ↓ bị hòa tan 1 phần.
⇒ n↓ = 0,09 ÷ 3 = 0,03 mol. ||► Mặt khác, khi bị hòa tan 1 phần thì:
nOH– = 4nAl3+ – n↓ ⇒ nAl3+ = (0,03 + 0,13) ÷ 4 = 0,04 mol.
Bảo toàn nguyên tố Al: nAl2O3 = 0,01 mol ||⇒ m = 1,56(g)

A. 184,1 gam và 91,8 gam.
B. 84,9 gam và 91,8 gam.
C. 184,1 gam và 177,9 gam.
D. 84,9 gam và 86,1 gam.

Đáp án B
Ta có:
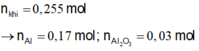
Dung dịch Y chứa 0,23 mol AlCl3.
Cho dung dịch chứa 0,3 mol Ba(OH)2 và 0,37 mol NaOH tác dụng với Y thu được dung dịch Z.
Z chứa Ba2+ 0,3 mol, Na+ 0,37 mol, AlO2- 0,23 mol, OH- dư 0,05 mol.
Cho H2SO4 vào Z.
Để kết tủa Al(OH)3 lớn nhất thì :
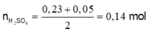
Để kết tủa BaSO4 lớn nhất thì : n H 2 S O 4 = 0 , 3 m o l
Lúc kết tủa BaSO4 tối đa thì Al(OH)3 bị hòa tan nhưng lượng BaSO4tạo thành lớn hơn Al(OH)3 bị hòa tan nên kết tủa vẫn tăng


Đáp án B
Ta có: n k h i = 0 , 255 m o l
![]()
Dung dịch Y chứa 0,23 mol AlCl3.
Cho dung dịch chứa 0,3 mol Ba(OH)2 và 0,37 mol NaOH tác dụng với Y thu được dung dịch Z.
Z chứa Ba2+ 0,3 mol, Na+ 0,37 mol, AlO2- 0,23 mol, OH- dư 0,05 mol.
Cho H2SO4 vào Z.
Để kết tủa Al(OH)3 lớn nhất thì :
n H 2 S O 4 = 0 , 23 + 0 , 05 2 = 0 , 14 m o l
Để kết tủa BaSO4 lớn nhất thì : n H 2 S O 4 = 0 , 3
Lúc kết tủa BaSO4 tối đa thì Al(OH)3 bị hòa tan nhưng lượng BaSO4tạo thành lớn hơn Al(OH)3 bị hòa tan nên kết tủa vẫn tăng
→ V = 0 , 3 2 = 150 m l

Đặt a, b, c là số mol Al203, CuO , FeO mA = 102a + 80b + 72c = 20,3 m rắn = 102a + 64b + 56c = 17,1 nHCl = 6a + 2b + 2c = 0,7 -> a = 0,05 ; b = c = 0,1 Trong B chứa nCO2 = b + c = 0,2 nCaCO3 = 0,1 -> nCa(HCO3)2 = 0,05 -> nCa(OH)2 = 0,15 -> Vdd =105 ml

Giải thích:
nBa = nAl = x mol
nOH- = 2nBa(OH)2 = 2x
Ba + 2H2O → Ba(OH)2 + H2
x x → x
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2
x → 0,5x → 0,5x →1,5x
=> x+1,5x = 0,05 => x = 0,02 mol
Dung dịch sau phản ứng gồm: Ba(OH)2 dư (0,01 mol) và Ba(AlO2)2 (0,01 mol)
nH+ = 0,075 mol
H+ + OH- → H2O
0,02←0,02
H+ + AlO2- + H2O → Al(OH)3
0,02←0,02→ 0,02
3H+ + Al(OH)3 → Al3+ + 3H2O
0,035→7/600
mAl(OH)3 = (0,02 – 7/600).78 = 0,65 gam
Đáp án B

Đáp án cần chọn là: A