Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Đặt số mol 3 axit lần lượt là a b và c ta có:
60a + 74b + 72c = 6,3 gam (PT theo khối lượng hỗn hợp). (1)
c = 6,4:160 = 0,04 mol (PT theo số mol brom phản ứng). (2)
Để pứ hoàn toàn với 3,15 gam X cần 0,045 mol NaOH ⇒ 6,3 gam X cần 0,09 mol NaOH.
⇒ a + b + c = 0,09 (PT theo số mol NaOH pứ) (3).
+ Giải hệ (1) (2) và (3) ⇒ a = nAxit axetic = a = 0,02 mol ⇒ mAxit axetic = 1,2 gam
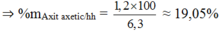

Đáp án : C
Ta có:
60nCH3COOH + 72nC2H3COOH + 74nC2H5COOH=3,15
nC2H3COOH=nBr2=0,02
nCH3COOH + nC2H3COOH + nC2H5COOH=nNaOH=0,045
=> nCH3COOH = 0,01 mol
=> % CH3COOH = 0 , 01 . 60 3 , 15 = 19,05 %

Ta có: \(n_{COOH\left(X\right)}=n_{CO_2}=0,7mol\)
Khi đốt X có: \(n_{CO_2}=0,4mol;n_{CO_2}=0,8mol\)
Theo ĐLBT oxi có \(n_O=2n_{COOH\left(X\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=y=0,6mol\)

Phần trăm về khối lượng của CH3CHO là 44,0%, của CH3COOH LÀ 56,0%. Thể tích dung dịch NaOH là 0,46 lít.

Dễ thấy cả 2 axit đều có 2 H => HCOOH và HCOO - COOH
Đặt số mol 2 chất là x và y,đặt a = 1 thì
x + y = 1
x + 2y = 1,4
=> x = 0,6 ; y = 0,4
=> %mHCOOH = 43,4%

104,48gam104,48gam
Giải thích các bước giải:
Sơ đồ phản ứng:
⎧⎪ ⎪ ⎪⎨⎪ ⎪ ⎪⎩AlMgFeOFe3O4+HNO3−−−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩NO,N2OH2O⎧⎪⎨⎪⎩Al(NO3)2Mg(NO3)2Fe(NO3)2to→⎧⎨⎩Al2O3MgOFe2O3+NO2+O2{AlMgFeOFe3O4→+HNO3{NO,N2OH2O{Al(NO3)2Mg(NO3)2Fe(NO3)2→to{Al2O3MgOFe2O3+NO2+O2
Oxi chiếm 20,22%20,22% khối lượng hỗn hợp.
mO=25,32%.25,32=5,12gammO=25,32%.25,32=5,12gam
→nO=0,32mol→nO=0,32mol
Gọi số mol của NONO và N2ON2O lần lượt là xx và yy mol
⎧⎨⎩x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02{x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02
Quy đổi hỗn hợp X thành các nguyên tố: Al,Mg,Fe,OAl,Mg,Fe,O
→mKl=25,32−5,12=20,2g→mKl=25,32−5,12=20,2g
→mO(cr)=30,92−20,2=10,72gam→mO(cr)=30,92−20,2=10,72gam
→nO=0,67mol→nO=0,67mol
3nAl+3nFe+2nMg=2nO(cr)3nAl+3nFe+2nMg=2nO(cr)
Gọi số mol của NH4NO3NH4NO3 là xx mol
Bảo toàn e:
3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O
0,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.80,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.8
→nNH4NO3=0,015mol→nNH4NO3=0,015mol
Khối lượng muối:
m=mKl+mNO−3+mNH4NO3m=mKl+mNO3−+mNH4NO3
=20,2+0,67.2.62+0,015.80=104,48gam

Đáp án C
Đặt số mol 3 axit lần lượt là a b và c ta có:
60a + 74b + 72c = 6,3 gam (PT theo khối lượng hỗn hợp). (1)
c = 6,4:160 = 0,04 mol (PT theo số mol brom phản ứng). (2)
Để pứ hoàn toàn với 3,15 gam X cần 0,045 mol NaOH ⇒ 6,3 gam X cần 0,09 mol NaOH.
⇒ a + b + c = 0,09 (PT theo số mol NaOH pứ) (3).
+ Giải hệ (1) (2) và (3) ⇒ a = nAxit axetic = a = 0,02 mol ⇒ mAxit axetic = 1,2 gam