Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Định hướng tư duy giải:
Vì có kim loại dư (Cu) nên muối chỉ là muối Fe2+ và Cu2+.Ta đó đầu bằng các BTE cho cả quá trình. Khi đó
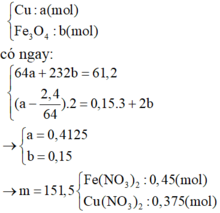

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

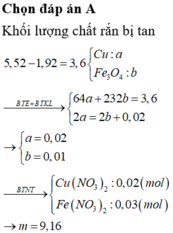
| CHÚ Ý : Với bài toàn này sau khi các phản ứng xong có kim loại không tan nên ta tư duy chặn đầu → muối chỉ là muối Fe2+ và Cu2+. |

\(n_{Fe\left(NO_3\right)_3}=0,14mol\)
Đặt \(n_{Fe}=n_{FeO}=n_{Fe_2O_3}=n_{Fe_3O_4}=x\)
\(Fe\rightarrow Fe^{3+}\)
x x
\(FeO\rightarrow Fe^{3+}\)
x x
\(Fe_2O_3\rightarrow2Fe^{3+}\)
x 2x
\(Fe_3O_4\rightarrow3Fe^{3+}\)
x 3x
\(\Rightarrow7x=0,14\Rightarrow x=0,02\Rightarrow m=10,4g\)

Đáp án D
Vì Cu dư ⇒ Dung dịch chứa 2 muối
Cu(NO3)2 và Fe(NO3)2.
+ Khí thoát ra là NO với
nNO = 0,01 mol.
Đặt nCu pứ = a và nFe3O4 = b ta có hệ:
64a + 232b = 5,045 – 1,125
& 2a – 2b = 3nNO = 0,03.
+ Giải hệ ta có:
nCu = 0,025 và b = 0,01 mol.
⇒ Muối bao gồm:
0,025 mol Cu(NO3)2
và (0,01×3) = 0,03 mol Fe(NO3)2.
⇒ mMuối = 0,025×188 + 0,03×180
= 10,1 gam
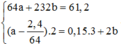
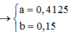
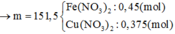
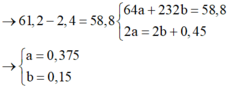
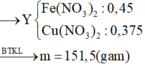
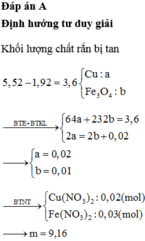
Chọn C.
Ta có: nNO = 0,15 mol.
Gọi a là số mol Cu trong X đã phản ứng; b là số mol Fe3O4 trong X, ta có:
64a + 232b = 61,2 - 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo định luật bảo toàn electron, ta có:
2a + 2.3b - 2.4b = 3.0,15 → a = 0,375; b = 0,15
Muối khan gồm: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
→ mmuối = 188.0,375 + 180.0,45 = 151,5 gam