Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi a ,b là số mol của NaCl và KCl.(Khi vào nước tạo dd thì số mol chấ tan không đổi )
NaCl + AgNO3 ----. AgCl + NaNO3 (1)
a mol ------------> a mol
KCl + AgNO3 -----> AgCl + KNO3 (2)
b mol ------------> b mol
ta có :
mNaCl + m KCl = 0,325
<=> 58,5 a + 74,5 b = 0,325 (*)
m AgCl PƯ1 + m AgCl PƯ2 = 0,717
<=> 143,5a + 143,5b = 0,717 (**)
ừ (*) và (**) được hệ phương rình. Giải ra được a = 0,003 => m NaCl = 0,1755 --> 54,2 %
b = 0,002 => m KCl = 0,149 --> 45,8%
Gọi a ,b là số mol của NaCl và KCl.(Khi vào nước tạo dd thì số mol chấ tan không đổi )
NaCl + AgNO3 ----. AgCl + NaNO3 (1)
a mol ------------> a mol
KCl + AgNO3 -----> AgCl + KNO3 (2)
b mol ------------> b mol
ta có :
mNaCl + m KCl = 0,325
<=> 58,5 a + 74,5 b = 0,325 (*)
m AgCl PƯ1 + m AgCl PƯ2 = 0,717
<=> 143,5a + 143,5b = 0,717 (**)
ừ (*) và (**) được hệ phương rình. Giải ra được a = 0,003 => m NaCl = 0,1755 --> 54,2 %
b = 0,002 => m KCl = 0,149 --> 45,8%

Gọi số mol của BaO, BaCO3, NaHCO3 trong 30,19g hh lần lượt là x, y, z
Có 153x + 197y + 84z = 30,19
Phần 1:
BaO + H2O → Ba(OH)2
x x
OH- + HCO3- → CO32- + H2O
Ba2+ + CO32- → BaCO3
n kết tủa = 0,11
Phần 2:
BaCO3 →BaO + CO2
y y
2NaHCO3 → Na2CO3 + H2O + CO2
z z/2 z/2
=> mCO2 + mH2O = 30,19 – 26,13 = 4,06
=> 44 (y + z/2) + 18 . z/2= 4,06
TH1: Ba tạo kết tủa hoàn toàn thành BaCO3 và NaHCO3 dư
=> nBaCO3 = nBaCO3 + nBaO = 0,11 => Không thỏa mãn
TH2: Ba(OH)2 dư và NaHCO3 hết
=> x + y = 0,11 và y + z = 0,11
=> x = 0,1; y = 0,05 và z = 0,06
a.
hh Y gồm BaO: 0,15 mol; Na2CO3: 0,03 mol
BaO + H2O → Ba(OH)2
0,15 0,15
Ba(OH)2 + Na2CO3 → BaCO3 + 2NaOH
0,15 0,03 0,03 0,06
=> m kết tủa = 0,03 . 197 = 5,91g
m dd = m chất rắn + mH2O – mBaCO3 = 26,13 + 79,78 – 5,91 = 100
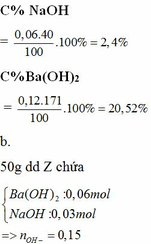
nAl2(SO4)3 = 0,02 => nAl3+ = 0,04; nSO42- = 0,06
Ba2+ + SO42- → BaSO4
0,06 0,06 0,06
nAl(OH)3 = 0,01 => mAl(OH)3 = 0,78g
m = 0,78 + 0,06 . 233 = 14,76g

PTHH:
Cu + H2SO4 ---x--->
Fe + H2SO4 ---> FeSO4 + H2 (1)
2Cu + O2 ---to---> 2CuO (2)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT(1): \(n_{Fe}=n_{H_2}=0,3\left(mol\right)\)
=> \(m_{Fe}=0,3.56=16,8\left(g\right)\)
Ta có: \(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
Theo PT(2): \(n_{Cu}=n_{CuO}=0,05\left(mol\right)\)
=> \(m_{Cu}=0,05.64=3,2\left(g\right)\)
=> \(\%_{m_{Cu}}=\dfrac{3,2}{3,2+16,8}.100\%=16\%\)
\(\%_{m_{Fe}}=100\%-16\%=84\%\)







\(Đặt:\left\{{}\begin{matrix}n_{NaCl}=x\left(mol\right)\\n_{KCl}=y\left(mol\right)\end{matrix}\right.\\ Theođề:\Rightarrow\left\{{}\begin{matrix}58,5x+74,5=0,325\\x+y=\dfrac{0,717}{143,5}=0,005\left(BTNT\left(Cl\right)\right)\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,003\\y=0,002\end{matrix}\right.\\ \Rightarrow m_{NaCl}=0,1755\left(g\right);m_{KCl}=0,149\left(g\right)\\ \Rightarrow\%NaCl=54,2\%,\%KCl=45,8\%\)