Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

N+5 +1e =>N+4
0,02 mol<=0,02 mol
2N+5 +2.4e =>2N+1
0,04 mol<=0,01 mol
ne nhận=ne nhường=0,06 mol
nNO3- tạo muối=ne nhận=0,06 mol
=>mNO3-=0,06.62=3,72g
mKL=5,04g=>m muối=m gốc KL+mNO3-=3,72+5,04=8,76g
nHNO3 =0,06+0,02+0,005.2=0,09 mol
=>CM dd HNO3=0,09/0,1=0,9M
Phương trình nhận electron:
N+5 + 8e → N2O
N+5 +1e→NO2
nNO tạo muối = nNO + 8nN2O = 0,02 + 8.0,005 = 0.02 + 0,04 = 0,06 mol
mNO tạo muối =0,06.62 = 3,72g
m =mKL+ mNO tạo muối = 5,04 + 3,72 = 8,76g
nHNO3 tham gia phản ứng = 2nNO + 10nN2O = 2.0,02 + 10.0,005= 0,09 mol
x =0.09:0,1=0,9M ==>> Đáp án thứ nhất

Đáp án A
dancol/H2 = 31 => Mancol = 62
=> Ancol Z có CTCT HOCH2CH2OH(C2H6O2)
Ta có:
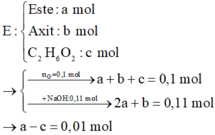
Khi đốt cháy E có:
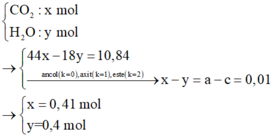
Áp dụng ĐLBTNT.O:
nO(E) + 2nO2 = 2nH2O => 4a + 2b + 2c + 0,47.2 = 0,41.2 + 0,4
→ 4a + 2b + 2c + 0,47.2 = 0,41.2 +0,4 → 4a + 2b + 2c = 0,28 mol
Giả hệ PT:
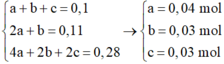
Áp dụng ĐLBTKL cho phản ứng cháy:
mE + mO2 = mH2O + mCO2
→ mE = 0,41.44 + 0,4.18 – 0,47.32 = 10,2
0,1 mol E + 0,11 mol NaOH
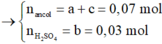
Áp dụng ĐLBTKL cho phản ứng thủy phân: mE + mNaOH = mRCOONa + mancol + mnước
→ mRCOONa = 10,2 + 0,11.40 – 0,07.62 – 0,03.18 = 9,72 gam.
→ mRH = 9,72 – 0,11.(69 – 1) = 2,46 g

Đặt công thức trung bình 2 ancol là CnH2n+1OH, công thức trung bình 3 ete là (CnH2n+1)2O, phân tử khối trung bình 3 ete là 6,76/0,08 = 84,5. Do đó: 28n + 18 = 84,5 suy ra n = 2,375. Vì vậy, 2 ancol cần tìm là C2H5OH (a mol) và C3H7OH (b mol).
Để đốt cháy hoàn toàn Z cần một lượng O2 đúng bằng lượng cần dùng để đốt cháy T:
C2H6O + 3O2 \(\rightarrow\) 2CO2 + 3H2O
C3H8O + 9/2O2 \(\rightarrow\) 3CO2 + 4H2O
Nên ta có: 40a + 60b = 27,2 và 3a + 4,5b = 43,68/22,4 = 1,95. Tính được: a = 0,2 và b = 0,3 mol.
Gọi x, y tương ứng là số mol ancol tạo ete, ta có: x + y = 2.0,08 = 0,16 và 46x + 60y = 6,76 + 18.0,02 = 8,2.
Thu được: x = 0,1 và y = 0,06 mol.
Do đó, hiệu suất tạo ete của X = 0,1/0,2 = 50%; của Y = 0,06/0,3 = 20%.

Đáp án là A
M a n c o l = 62 ⇒ C 2 H 4 ( O H ) 2
Quy đổi E thành:
=> a= 0,26; b= 0,1; c= -0,12