Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Ba thí dụ phản ứng phân hủy là phản ứng oxi hóa – khử:
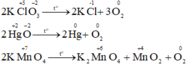
- Ba thí dụ phản ứng phân hủy không phải là phản ứng oxi hóa – khử:
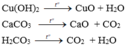

Phản ứng oxi hoá - khử là phản ứng hoá học trong đó có sự chuyển electron giữa các chất phản ứng.
Thí dụ:
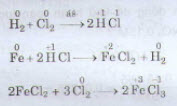
: Phản ứng oxi hoá – khử là phản ứng hoá học trong đó có xảy ra đồng thời sự oxi hoá và sự khử.
Ví dụ: Fe2O3 + 3H2 −to→ 2Fe + 3H2O
CuO + H2 −to→ Cu + H2O

- Ba thí dụ phản ứng hóa hợp thuộc loại phản ứng oxi hóa – khử :
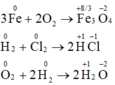
- Ba thí dụ phản ứng hóa hợp không thuộc loại phản ứng oxi hóa – khử :
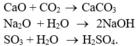

Sở dĩ phản ứng thế luôn luôn là loại phản ứng oxi hoá – khử vì trong phản ứng thế, bao giờ cũng có sự thay đổi số oxi hoá của các nguyên tố.
phản ứng thế luôn luôn là loại phản ứng oxi hoá - khử vì trong phản ứng thế, bao giờ cũng có sự thay đổi sô' oxi hoá của các nguyên tố.

Chất oxi hoá là chất nhận electron.
Sự oxi hoá một chất là làm cho chất đó nhường electron.
Chất khử là chất nhường electron.
Sự khử một chất là sự làm cho chất đó thu electron.
Thí dụ: Fe + CuSO4 \(\rightarrow\)FeSO4 + Cu
- Nguyên tử Fe nhường elcctron, là chất khử. Sự nhường electron của Fe được gọi là sự oxi hoá nguyên tử sắt.
- Ion đồng nhận electron, là chất oxi hoá. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
.jpg)
Ba thí dụ phản ứng phân hủy là phản ứng oxi hoá – khử :
CaCO3 -tº\(\rightarrow\) CaO + CO2\(\uparrow\)
NH4Cl -tº\(\rightarrow\) NH3 + HCl
Cu(OH)2 -tº\(\rightarrow\) CuO + H2O
Ba thí dụ phản ứng phân hủy không là phản ứng oxi hoá – khử
Cu(OH)2 -tº\(\rightarrow\)CuO + H2O
СаСОз -tº\(\rightarrow\) CaO + CO2
H2CO3 -tº\(\rightarrow\) CO2 + H2O.