Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{Mg}=1,2\left(g\right)\)
=> \(n_{Mg}=\dfrac{1,2}{24}=0,05\left(mol\right)\)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
____0,05--------------------->0,05
2Al + 6HCl --> 2AlCl3 + 3H2
\(\dfrac{1}{30}\)<--------------------0,05
=> \(m_{Al}=\dfrac{1}{30}.27=0,9\left(g\right)\)
=> \(\left\{{}\begin{matrix}\%Al=\dfrac{0,9}{0,9+1,2}.100\%=42,857\%\\\%Mg=\dfrac{1,2}{0,9+1,2}.100\%=57,143\%\end{matrix}\right.\)

Gọi số mol của Fe và Cu trong hỗn hợp lần lượt là x và y.
2Fe + 3Cl2 → 2FeCl3 (1)
x(mol) x(mol)
Cu + Cl2 → CuCl2 (2)
y(mol) y(mol)
Fe + 2HCl → FeCl2 + H2 (3)
x (mol) 2x(mol) x(mol).
Theo điều kiện bài toán và phương trình hoá học (3) ta có: 127x = 25,4 → x = 0,2
Theo phương trình phản ứng (1) và (2) ta có: 162,5x + 135y = 59,5
Vậy y = 0,2.
Khối lượng mỗi muối là: m FeCl3=32,5gam
m CuCl2=27gam
%FeCl3 = 54,62%.
%CuCl2 = 45,38%

Gọi số mol của Cu, Fe, Al trong 23,8 gam hhX lần lượt là x, y, z mol
→ mX = 64x + 56y + 27z = 23,8 (1)
\(n_{Cl_2}\) = x + 1,5y + 1,5z = 0,65 (2)
0,25 mol X + HCl → 0,2 mol H2 nên 0,2.(x + y + z) = 0,25.(y + 1,5z) (3)
Từ (1), (2), (3) => x = 0,2 mol; y = 0,1 mol; z = 0,2 mol
\(\%_{Cu} = \dfrac{0,2. 64}{23,8} \approx 53,78\%\)
\(\%_{Fe} = \dfrac{0,1 .56}{23,8} \approx 23,53\%\)
%Al ≈ 22,69%

Phần 1
2Al +6 HCl ----> 2AlCl3 + 3H2 (1)
Fe + 2HCl ----> FeCl2 + H2 (2)
Cu ko pư với dd HCl
Phần 2
2Al + 2NaOH + 2H20 ---> 2NaAlO2 + 3H2 (3)
Fe và Cu ko pư với dd NaOH
Theo pt(3) n Al = \(\frac{2}{3}\).n H2=\(\frac{2}{3}\). \(\frac{3,36}{22,4}\)=0,1 (mol)
%m Al= \(\frac{0,1.27}{20}\).100%= 13,5%
Theo pt(1)(2) tổng n H2=\(\frac{3}{2}\). nAl + n Fe=\(\frac{5,6}{22,4}\)
==> 0,15 + n Fe = 0,25 ==> n Fe = 0,1 (mol)
%m Fe= \(\frac{0,1.56}{20}\).100%= 28%
%m Cu=100% - 13,5% - 28% =58,5%
tại sao % Al lại đem chia 20 vậy 0,1 mol là ở 1 phần thôi là chia 10 chứ .% Fe cũng thế vậy
==> tổng mAl + mFe trong 1 phần = 0,1.27 + 0,1.56=8,3
%Cu =100% - \(\dfrac{8,3}{10}\).100=17%

Mg+2HCl->MgCl2+H2
x x
2Al+6HCl->2AlCl3+3H2
y 3/2 y
mMg+mAl=23.4
->24x+27y=23.4
nH2=1.2(mol)
x+3/2 y=1.2
x=0.3(mol)->mMg=7.2(g)
y=0.6(mol)_>mAl=16.2(g)
Bạn tự tính % nhé ^^

2Al + 3H2SO4 -> Al2(SO4)3 + 3H2 (1)
2 3 1 3 ( mol)
2x 3x x 3x
Mg + H2SO4 -> MgSO4 +H2 (2)
1 1 1 1
y y y y
Gọi số mol của Al là x
=> nAl = 2x, nH2SO4 = 3x, nAl2(SO4)3= x , nH2= 3x
Gọi số mol của Mg là y
=> nMg = y, nH2SO4 = y, nMgSO4 = y, nH2= y
Ta có:
mhh = mAl + mMg
1,41= 27.2x + 24y
1,41= 54x + 24y
V H2 (1) + V H2 (2) = 1,568 (1568ml = 1,568 l)
22,4 . 3x + 22,4y = 1,568
67,2x + 22.4y = 1,568
Có : - 54x + 24y=1,41
- 67,2x + 22.4y = 1,568
Bấm máy tính => x = 0,015
y = 0,025
mAl = 54x = 54 . 0,015 = 0,81 9(g)
mMg = 1,41 - 0,81 = 0,6 (g)
%mAl = 0,81 . 100 / 1,41 = 57,45%
%mMg = 100% - 57,45% = 42,55%

2 A l + 3 H 2 S O 4 → A l 2 S O 4 3 + 3 H 2
x 3/2 x mol
F e + H 2 S O 4 → F e S O 4 + H 2
y y mol
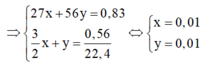
⇒ % m A l = 0,01.27 0,83 .100 = 32,53 % ⇒ % m F e = 100 % − 32,53 % = 67,47 %
⇒ Chọn D.