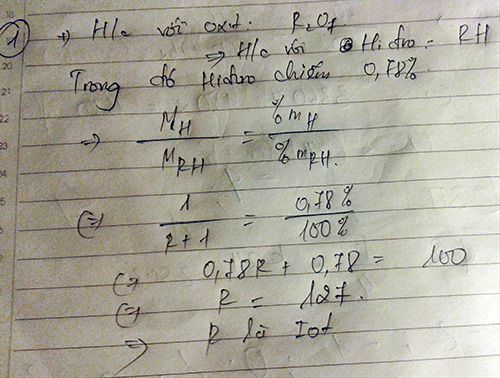Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1.
Oxit cao nhất của R là R2O5 → R thuộc nhóm VA
Hợp chất khí của R với H là RH3 trong đó:
\(\%H=\frac{3.1}{3.1+M_R}.100\%=17,65\%\)
\(\rightarrow M_R=14\)
→ R là nito
2.
Oxit cao nhất của R là R2O7 → R thuộc nhóm VIIA
Hợp chất khí của R với H là HR trong đó:
\(\%H=\frac{1.1}{1.1+M_R}.100\%=2,74\%\)
\(\rightarrow M_R=35,5\)
→ R là Clo

1.
Cấu hình e lớp ngoài cùng là ns2np4 nên R thuộc nhóm VIA
→ Công thức oxit cao nhất là RO3
\(\%mR=\frac{R}{R+3.16}.100\%=40\%\)
\(\rightarrow R=32\)
Vậy R là lưu huỳnh (S)
2.Oxit cao nhất R2O5 → R thuộc nhóm VA → Hợp chất khí với H là RH3
\(\%mH=\frac{3}{R+3}.100\%=8,82\%\)
\(\rightarrow R=31\)
Vậy R là photpho (P)

HD:
CT oxit cao nhất của R với oxi là R2O5 (suy ra từ RH3).
Ta có: 80/(2R+80) = 0,5634 suy ra: R = 14 (N).
H:N:H H cấu tạo: H-N-H H
Hóa trị cao nhất vs khí H là 3
>> hóa trị cao nhất vs O là 8_3=5
>>hợp chất vs oxit cao nhất là R2O5
Có %mO=56.34%
Xét tỉ số MO/Mo+MR =%mo
Hay80/80+2×MR=0.5634
>>MR=14(N)
>>hợp chất vs oxit cao nhất là N2O5
b) hợp chất vs H là NH3

Bạn tham khảo lời giải ở đây nhé!
Câu hỏi của Huong LE - Hóa học lớp 8 | Học trực tuyến
Từ đó suy ra A là N2O5 và B là NH3.

Công thức oxit cao nhất : \(RO_2\)
⇒ R thuộc hóa trị IV
Ta có: hóa trị oxit cao nhất + hóa trị trong hợp chất với hidro = 8
⇔ hóa trị trong hợp chất với hidro là IV
Công thức trong hợp chất với hidro : \(RH_4\)
Ta có: %H = \(\dfrac{4M_H.100}{M_R+4M_H}\)
⇔ 25 = \(\dfrac{400}{M_R+4}\)
⇔ \(25M_R+100=400\)
⇔ \(M_R\) = 12 (g/mol)
Vậy R là Cacbon (C)
Cấu hình electron: \(1s^22s^22p^2\)
Công thức hợp chất với hidro: RH4
Ta có: %H=25%
%R= 75%
\(\dfrac{M_R}{4M_H}=\dfrac{75}{25}\)
\(\Leftrightarrow\dfrac{M_R}{4\times1}=\dfrac{75}{25}\)
\(\Rightarrow M_R=12\)
Suy ra R là C (Z=6)
cấu hình e: 1s22s22p2

ta có nguyên tố R có hoá trị 5
=> CTHC với Hiđro là RH3
Ta có \(\frac{\%R}{\%H}\)= \(\frac{82,35}{17,65}\)=\(\frac{M_R}{3}\)
=> MR=14 đvC
=> R là Nitơ