Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

â)
b) Nếu điều chế cùng một thể tích khí O2 thì dùng KClO3 để điều chế kinh tế hơn, tuy giá tiền 1 kg cao hơn nhưng thể tích khí O2 sinh ra nhiều hơn. Giair thích
2KClO3to⟶2KCl+3O2
2 mol 3 mol
1 mol 1,5 mol
mKClO2=1×122,5=122,5(g
Số tiền mua 122,5 g để điều chế 1,5 mol O2là
0,1225 x 96000 = 11760(đ)
2KMnO4to⟶K2MnO4+O2↑+MnO2
2 mol 1 mol
3 mol 1,5 mol
mKMnO4=3×158=474(g
Số tiền mua 474 g KMnO4 để điều chế 1,5 mol O2 là:
0,474 x 30000 = 14220(đ)
Nên....

Giả sử cần điều chế 3,36lit O 2 tương đương với 0,15 mol O 2
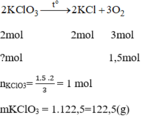
Số tiền mua 122,5g để điều chế 1,5mol O 2 :
0,1225.96000 = 11760 (đồng)
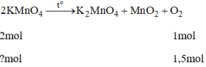
n K M n O 4 = 1,5 . 2 =3 mol
n K M n O 4 = 3.158 = 474 (g)
Số tiền mua 474g để điều chế 1,5 mol O 2 :
0,474.30000 = 14220(đồng)
Vậy để điều chế cùng 1 thể tích khí O 2 thì dùng K C l O 3 để điều chế kinh tế hơn mặc dù giá tiền cao mua 1 kg K C l O 3 cao hơn nhưng thể tích khí O 2 sinh ra nhiều hơn.

\( {M_{KCl{O_3}}} = 122,5(g/mol);{M_{KMn{O_4}}} = 158(g/mol)\)
Giả sử ta lấy cùng một khối lượng là a gam
\(2KCl{O_3}\buildrel {{t^o}} \over\longrightarrow 2KCl + 3{O_2} \uparrow \)
2 mol..............................3 mol
\({a \over {122,5}}mol ............. {{3a} \over {2 \times 122,5}}mol\)
\(2KMn{O_4}\buildrel {{t^o}} \over\longrightarrow {K_2}Mn{O_4} + {O_2} \uparrow + Mn{O_2}\)
2 mol......................................1 mol
\({a \over {158}}mol...................{a \over {2 \times 158}}mol\)
\({{3a} \over {2 \times 122,5}}mol > {a \over {2 \times 158}}mol\)
Khi nhiệt phân cùng một lượng, chất cho nhiều \({O_2}\)hơn là \(KCl{O_3}\)
b) Nếu điều chế cùng một thể tích khí O2 thì dùng KClO3 để điều chế kinh tế hơn, tuy giá tiền 1 kg cao hơn nhưng thể tích khí O2 sinh ra nhiều hơn. Tính toán cụ thể như sau :
\(2KCl{O_3}\buildrel {{t^o}} \over\longrightarrow 2KCl + 3{O_2} \uparrow \)
2 mol...............................3 mol
1 mol...............................1,5 mol
\({m_{KCl{O_2}}} = 1 \times 122,5 = 122,5(g)\)
Số tiền mua 122,5 g để điều chế 1,5 mol \({O_2}\) là
0,1225 .11100=1359,75 đ
\(2KMn{O_4}\buildrel {{t^o}} \over\longrightarrow {K_2}Mn{O_4} + {O_2} \uparrow + Mn{O_2}\)
2 mol......................................1 mol
3 mol............................................1,5 mol
\({m_{KMn{O_4}}} = 3 \times 158 = 474(g)\)
Số tiền mua 474 g \(KMn{O_4}\) để điều chế 1,5 mol \({O_2}\) là:
0,474*45000=21330đ
\(2KMn{O_4}\buildrel {{t^o}} \over\longrightarrow {K_2}Mn{O_4} + {O_2} \uparrow + Mn{O_2}\)
2 mol......................................1 mol

* Ta có PTHH:
2KMnO4 \(\rightarrow\) K2MnO4 + MnO2 + O2 (1)
2KClO3 \(\rightarrow\) 2KCl + 3O2 (2)
Gọi mKMnO4 = mKClO3 =a (g)
=> nKMnO4 = a/158 (mol) và nKClO3 = a/122.5 (mol)
Theo PT (1) => nO2 = 1/2 . nKMnO4 = 1/2 . a/158 = a/316 (mol)
Theo PT(2) => nO2 = 3/2 . nKClO3 = 3/2 . a/122.5 = 3/245 .a (mol)
Có : 1/316 < 3/245 => a/316 < 3/245 .a
hay nO2(PT1) < nO2(PT2)
=> KClO3 cho nhiều khí O2 hơn
TheO PT(2)

2KClO3 \(\underrightarrow{t^o}\) 2KCl + 3O2\(\uparrow\)
2KMnO4 \(\underrightarrow{t^o}\) K2MnO4 + MnO2 + O2\(\uparrow\)
KClO3 => (to) KCl + 3/2 O2
2KMnO4 => (to) K2MnO4 + MnO2 + O2
Một số phương trình điều chế O2:
2H2O => 2H2 + O2
H2O2 => H2O + 1/2O2
O3 + 2Ag => Ag2O + O2
2NaOH => (đpnc kiềm) Na + H2O + 1/2 O2
F2 + H2O => 2HF + 1/2 O2

1) nFe3O4= 46,4:232=0,2 mol
PTHH :3Fe+2O2\(\rightarrow\) Fe3O4
0,6 0,4 \(\leftarrow\)0,2 (mol)
PTHH: 2KMnO4\(\rightarrow\) K2MnO4+MnO2+O2
0,8 \(\leftarrow\) 0,4 (mol)
\(\Rightarrow\) m KMnO4= 0,8.158=126,4 g
1) 3Fe + 2O2 ---> Fe3O4 ---> nO2 = 2nFe3O4 = 2.46,4/232 = 0,4 mol.
2KMnO4 ---> K2MnO4 + MnO2 + O2 ---> nKMnO4 = 2nO2 = 0,8 mol
---> mKMnO4 = 158.0,8 = 126,4 g.
2) KClO3 ---> KCl + 3/2O2 ---> nKClO3 = 2/3nO2
---> nKClO3:nKMnO4 = 2/3:2 = 1:3 ---> mKClO3:mKMnO4 = 158/3.122,5 = 0,43
3) KNO3 ---> KNO2 + 1/2O2 ; Cu(NO3)2 ---> CuO + 2NO2 + 1/2O2
Như vậy nếu thu được cùng lượng oxi thì KClO3 sẽ có khối lượng nhỏ nhất.

Theo bài ra : KMnO4 và KClO3 có cùng khối lượng x (g)
Suy ra : nKMnO4 = \(\dfrac{x}{158}\) (mol)
nKClO3 = \(\dfrac{x}{122,8}\) (mol)
PTHH có : 2KMnO4 \(\rightarrow\) K2MnO4 + MnO2 + O2
(mol) \(\dfrac{x}{158}\) \(\dfrac{x}{316}\)
2KClO3 \(\rightarrow\) 2KCl + 3O2
(mol) \(\dfrac{x}{122,8}\) \(\dfrac{3x}{245,8}\)
Ta có: \(\dfrac{x}{136}< \dfrac{3x}{245,8}\) (mol)
Vậy Nếu lấy KClO3 và KMnO4 cùng khối lượng thì KClO3 điều chế đc nhiều oxi hơn.

a) Phương trình phản ứng hóa học :
S + O2 \(\rightarrow\) SO2
b) Số mol lưu huỳnh tham gia phản ứng :
\(n_S=\frac{3,2}{32}=0,1\left(mol\right)\)
Theo phương trình, ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
\(V_{SO_2}=22,4.0,1=2,24\left(l\right)\)
Tương tự thể tích khí oxi cần dùng ở đktc là :
\(V_{O_2}=22,4.0,1=2,24\left(l\right)\)
Vì khí oxi chiếm 20% thể tích của không khí nên thể tích không khí cần là :
\(V_{kk}=5.V_{O_2}=5.2,24=11,2\left(l\right)\)
Nếu thế số vào phương trình thì là :
Ta có phương trình hóa học :
S + O2 \(\rightarrow\) SO2
1mol 1mol 1mol
0,1 0,1 0,1
.PNG)
Mình không hiểu kinh tế hơn là gì ạ. Nhưng theo mình kinh tế hơn chắc là đắt hơn
Nên dùng KMnO4 "kinh tế" hơn.
Chúc bạn học tốt.
Với cùng 1 kg thì KClO3 cho ra lượng oxi cao gấp khoảng 4 lần, mà giá tiền chỉ gấp 3 lần thì dùng KClO3 sẽ rẻ hơn