Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CTHH dạng TQ là MH3
Có :
%H = (3. MH / MMH3).100%=17.65%
=> %H =(3/MMH3) =0.1765
=> MMH3 = 3/0.1765 = 17 (g)
hay 1 . MM + 3 . MH =17g
=> MM + 3=17(g)
=> MM = 17-3=14(g)
=> M là nguyên tử thuộc nguyên tố hóa học Nito
=> CTHH củaaX là NH3

Gọi CTHH là $H_3X$
$\%H = \dfrac{3}{3 + X}.100\% = 17,65\%$
$\Rightarrow X = 14$
Vậy X là Nito
Hợp chất MH3
%H=3.1/M+3.100%=17,65%
⇔3/M+3=0,1765
⇔0,1765M=2,4705
⇔M≈14(g/mol)
⇒Nitơ
có gì sai mong bạn thôm cảm

a)Gọi hợp chất cần tìm là \(X_2O_3\)
Theo bài ta có: \(PTK_{X_2O_3}=76M_{H_2}=76\cdot2=152\left(đvC\right)\)
b)Mà \(2M_X+3M_O=152\Rightarrow M_X=\dfrac{152-3\cdot16}{2}=52\left(đvC\right)\)
X là nguyên tố Crom(Cr).
Vậy CTHH là \(Cr_2O_3\).
c)\(\%X=\dfrac{2\cdot52}{2\cdot52+3\cdot16}\cdot100\%=68,42\%\)

CTHH dạng TQ là MH3
Có :
%H = (3. MH / MMH3).100%=17.65%
=> %H =(3/MMH3) =0.1765
=> MMH3 = 3/0.1765 = 17 (g)
hay 1 . MM + 3 . MH =17g
=> MM + 3=17(g)
=> MM = 17-3=14(g)
=> M là nguyên tử thuộc nguyên tố hóa học Nito
=> CTHH củaaX là NH3

6. Gọi công thức hoá học của oxit là X
ta có: \(\%O=\dfrac{16}{2X+16}.100\%=25,8\%\)
\(\Leftrightarrow0,258.\left(2X+16\right)=16\)
\(\Leftrightarrow0,516X=11,872\)
\(\Rightarrow X\approx23\)
=>X là natri
=> CTHH oxit là Na2O

Gọi hợp chất hữu cơ đó là X, ta có :
Nguyên tố H chiếm số % về khối lượng là :
100% - 85,71% = 14,29%
Khối lượng mol của hợp chất hữu cơ đó là :
mX = 21.2 = 42 (g/mol)
Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất X là :
mC = \(\frac{42.85,71}{100}\approx36\left(g\right)\)
mH = 42 - 36 = 6 (g)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất là :
nC = \(\frac{36}{12}\) = 3 (mol)
nH = \(\frac{6}{2}\) = 3 (mol)
Suy ra trong một phân tử hợp chất có 3 nguyên tử C và 3 nguyên tử H => CTHH của X là C3H3.
Vậy công thức hóa học của hợp chất hữu cơ đó là C3H3.
Ta có :
PTKH = 2*1 = 2 (đvC)
=> PTKhợp chất = 2 * 21 = 42 ( đvC )
Do nguyên tố C chiếm 85,71% về khối lượng
=> Khối lượng của C trong hợp chất trên là :
42 * 85,71% = 36 (đvC)
Mà nguyên tố C nặng 12 đvC => Số nguyên tử C có trong hợp chất trên là 3 nguyên tử
Khối lượng của H trong hợp chất trên là :
42 - 36 = 6 ( đvC )
=> Số nguyên tử H có trong hợp chất trên là 6 nguyên tử
Vậy công thức hóa học của hợp chất là : C3H6
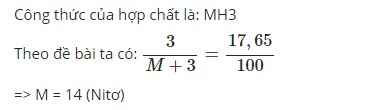
Hợp chất \(M\)\(H_3\)
\(\%H=\frac{3.1}{M+3}.100\%=17,65\%\)
\(\Leftrightarrow\frac{3}{M+3}=0,1765\)
\(\Leftrightarrow0,1765M=2,4705\)
\(\Leftrightarrow M\approx14\left(g/mol\right)\)
\(\Rightarrow Nitơ\)