Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

pthh 2Na + 2H2O ---> 2NaOH + H2
nNaOH = 16 : 40 = 0,4 (mol)
theo pthh , nNa = nNaOH = 0,4(mol)
=> mNa = 0,4 . 23 = 9,2 (g)
theo pthh , nH2 = 1/2 nNa = 0,2 (mol)
=> VH2 = 0,2 . 22,4 = 4,48 (l)

a,\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right);n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 0,2 0,1
PTHH: 2K + 2H2O → 2KOH + H2
Mol: 0,1 0,05
b, \(n_{H_2}=0,1+0,05=0,15\left(mol\right)\)
\(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
c,mdd sau pứ=4,6+3,9+91,5-0,15.2=99,7 (g)
\(\%m_{NaOH}=\dfrac{0,2.40.100\%}{99,7}=8,02\%\)
\(\%m_{KOH}=\dfrac{0,1.56.100\%}{99,7}=5,62\%\)
Bài 3 :
\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
\(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
a) Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
0,2 0,2 0,1
\(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
0,1 0,1 0,05
b) \(n_{H2\left(tổng\right)}=0,1+0,05=0,15\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,15.22,4=3,36\left(l\right)\)
c) \(n_{NaOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{NaOH}=0,2.40=8\left(g\right)\)
\(n_{KOH}=\dfrac{0,05.2}{1}=0,1\left(mol\right)\)
⇒ \(m_{KOH}=0,1.56=5,6\left(g\right)\)
\(m_{ddspu}=8,5+91,5-\left(0,15.2\right)=99,7\left(g\right)\)
\(C_{NaOH}=\dfrac{8.100}{99,7}=8,02\)0/0
\(C_{KOH}=\dfrac{5,6.100}{99,7}=5,62\)0/0
Chúc bạn học tốt

`2Na+2H_2O->2NaOH+H_2`
x-----------------------------`1/2`x mol
`2K+2H_2O->2KOH+H_2`
y---------------------------`1/2` y mol
`n_(H_2)=(6,72)/(22,4)=0,3 mol`
Ta có phương trình :
\(\left\{{}\begin{matrix}23x+39y=9,3\\\dfrac{1}{2}x+\dfrac{1}{2}y=0,3\end{matrix}\right.\)
-> nghiệm vô lí
`#YBTran~`

a) PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\) (1)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\) (2)
b) Vì H2SO4 chắc chắn còn dư nên tính theo mol của H2
Ta có: \(n_{H_2}=\dfrac{0,224}{22,4}=0,01\left(mol\right)\)
Gọi số mol của Zn là \(a\) \(\Rightarrow n_{H_2\left(1\right)}=a\left(mol\right)\)
Gọi số mol của Mg là \(b\) \(\Rightarrow n_{H_2\left(2\right)}=b\left(mol\right)\)
Ta lập được hệ phương trình:
\(\left\{{}\begin{matrix}a+b=0,01\\65a+24b=0,445\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,005\\b=0,005\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=0,005\cdot65=0,325\left(g\right)\\m_{Mg}=0,005\cdot24=0,12\left(g\right)\end{matrix}\right.\)
PTHH Zn+ H2SO4--->ZnSO4 +H2
Mg+H2SO4----->MgSO4+H2
Đặt nZn=a,nMg=b
=>mhh=65a+24b=0,445(I)
Theo các phương trình phản ứng
=>\(n_{H_2}\)=a+b=\(\dfrac{0,224}{22,4}=0,01\)(II)
Từ(I),(II)=>a=b=0.005(mol)
=>mZn=0,005.65=0,325(g)
mMg=0,005.24=0.12(g)

\(n_{Na}=\dfrac{4.6}{23}=0.2\left(mol\right)\)
\(n_K=\dfrac{3.9}{39}=0.1\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
\(n_{H_2}=0.1+0.05=0.15\left(mol\right)\)
\(V_{H_2}=0.15\cdot22.4=3.36\left(l\right)\)
a) nNa=4,6/23=0,2(mol)
nK=3,9/39=0,1(mol)
PTHH: 2 Na + 2 H2O -> 2 NaOH + H2
0,2____________0,2______0,2__0,1(mol)
2 K + 2 H2O -> 2 KOH + H2
0,1____0,1______0,1___0,05(mol)
b) V(H2,đktc)=(0,05+0,1).22,4=3,36(l)

a) 2Na+2H2O→2NaOH+H2(1)
2K+2H2O→2KOH+H2(2)
b) nNa=\(\dfrac{4,6}{23}\)=0,2(mol)
Theo PTHH (1): nNa:nH2=2:1
⇒nH2(1)=nNa.12=0,2.12=0,1(mol)
⇒VH2(1)=0,1.22,4=2,24(l)
nK=\(\dfrac{3,9}{39}\)=0,1(mol)
Theo PTHH (2): nK:nH2=2:1
⇒nH2(2)=nK.12=0,1.12=0,05(mol)
⇒VH2(2)=0,05.22,4=1,12(l)
⇒Vh2=2,24+1,12=3,36(l)
c) Dung dịch thu được sau phản ứng làm giấy quỳ tím chuyển đổi thành màu xanh vì nó là dung dịch bazơ.
d)
Fe2O3+3H2-to>2Fe+3H2O
0,15------0,1
n Fe2O3=0,1 mol
=>Fe2O3 dư
=>m Fe=0,1.56=5,6g
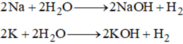
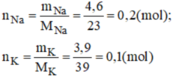
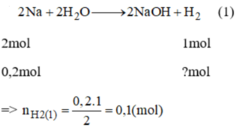
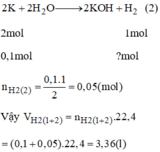
\(n_{Na}=\dfrac{4.6}{23}=0.2\left(mol\right)\)
\(n_K=\dfrac{3.9}{39}=0.1\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
\(V_{H_2}=\left(\dfrac{0.2}{2}+\dfrac{0.1}{2}\right)\cdot22.4=3.36\left(l\right)\)
\(m_{bazo}=0.2\cdot40+0.1\cdot56=13.6\left(g\right)\)