Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nước clo dần dần bị mất màu theo thời gian, không bảo quản được lâu là do quá trình phân huỷ HClO :
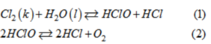
Phản ứng (2) làm cho nồng độ HClO giảm, cân bằng hoá học của phản ứng (1) chuyển dịch theo chiều thuận, clo sẽ phản ứng với nước cho đến hết, do đó nước clo không bền.

1.Vì trong nước javen có NaClO có tính oxi hóa mạnh làm mất màu và khử mùi
2.Vì nước clo có HClO có tính oxi hóa mạnh nên làm sạch nước
1.Nước javen thường được dùng để tẩy trắng vải, quần áo , vệ sinh chuồng trại vì tính oxi hóa mạnh nên dùng để khử trùng và tẩy trắng
*Giải thích thêm:
(Nước Javel có tính OXH mạnh là do:
NaClO : Cl(+1) tính OXH mạnh
NaClO + H2O + CO2 --> NaHCO3 + HClO ( HClO có Cl +1 ) )

Câu 2 :
\(n_{FeCl_3} = \dfrac{16,25}{162,5} = 0,1(mol)\)
2Fe + 3Cl2 \(\xrightarrow{t^o}\) 2FeCl3
0,1......0,15.........0,1.................(mol)
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,06.............0,48...................................0,15....................(mol)
Suy ra :
m = 0,06.158 = 9,48(gam)
\(m_{HCl} = 0,48.36,5 = 17,52(gam)\)
Giải thích các bước giải:
1. khi chó khí clo vào giấy quỳ ẩm thì ngay lập tức clo tác dụng vs nc đk ánh sáng sẽ tạo thành HCL ==> quỳ chuyển đỏ vì HCl là ãit

Dùng natri hidrocacbonat \(\left(NaHCO_3\right)\)
Do natri hidrocacbonat tác dụng với axit trong dạ dày tạo thành muối, khí và nước => làm hết lượng axit trong dạ dày làm hết đau dạ dày
\(NaHCO_3+HCl\rightarrow NaCl+CO_2\uparrow+H_2O\)

a) Chlorine có mùi xốc, nên khi sử dụng nước sinh có chlorine, chúng ta sẽ ngửi thấy mùi của nước chlorine
b) Trong quá trình khử trùng, người ta phải cho một lượng chlorine dư vào nước sinh hoạt. Lượng chlorine dư trong nước sinh hoạt còn có tác dụng ngăn ngừa sự tái nhiễm của vi khuẩn trong quá trình phân phối trong đường ống dẫn nước và trữ nước tại nhà
c) Một số phương pháp để loại bỏ khí chlorine dư trong nước sinh hoạt:
- Sử dụng máy lọc nước than hoạt tính
- Phơi chậu nước ra ngoài ánh nắng mặt trời => Tia cực tím với cường độ cao vào nước cùng làm giảm lượng chlorine
- Sử dụng máy lọc nước RO (thẩm thấu ngược) cũng có thể giúp loại bỏ lượng chlorine trong nước

3)
Đơn chất halogen kí hiệu là X2
X2+ Ca\(\underrightarrow{^{to}}\) CaX2
nCaX2= \(\frac{10}{\text{40+ 2X}}\) mol
\(\rightarrow\) nX2= \(\frac{10}{\text{40+ 2X}}\) mol
2Al+ 3X2 \(\underrightarrow{^{to}}\) 2AlX3
Lượng halogen phản ứng là \(\frac{10}{\text{40+ 2X}}\) mol
\(\rightarrow\) nAlX3=\(\frac{20.\left(\text{40+ 2X}\right)}{3}\)= \(\frac{\text{800+40X}}{3}\) mol
Mà mAlX3= 8,9g \(\rightarrow\) nAlX3= \(\frac{8,9}{\text{27+ 3X}}\)
Ta có pt: \(\frac{\text{800+ 40X}}{3}\)= \(\frac{8,9}{\text{27+ 3X}}\)
\(\Leftrightarrow\) 26,7= \(\frac{\text{800+ 40X}}{3X+27}\)
\(\Leftrightarrow\) 26,7= 21600+ 2400X+ 1080X+ 120X2
\(\Leftrightarrow\) 120X2 + 3480X+ 21573,3= 0
PT ra 2 nghiệm âm nên ko có X thoả mãn đb
4)
C1: Khí clo màu vàng lục, oxi ko màu
C2: Đưa quỳ ẩm vào 2 khí. Clo làm quỳ hoá đỏ, sau đó mất màu. Oxi ko hiện tươngj
Cl2+ H2O\(⇌\) HCl+ HClO
C3: Dẫn 2 khí vào dd NaBr. Clo làm dd chuyển màu nâu đỏ. Oxi ko hiện tượng
Cl2+ 2NaBr\(\rightarrow\) 2NaCl+ Br2

Câu 1:
Người bị đau dạ dày thường uống thuốc có chứa thành phần NaHCO3, vì nó sẽ làm giảm lượng axit clohidric trong dạ dày
PTHH: \(NaHCO_3+HCl\rightarrow NaCl+CO_2\uparrow+H_2O\)
Câu 2:
Dưới áp suất khí quyển 1 ATM thì nước sôi ở 100oC. Nếu cho muối ăn vào nước thì nhiệt độ sôi cao hơn 100oC khi đó luộc rau sẽ mềm, xanh và chín nhanh hơn