Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Vì bên trái có tổng số nguyên tử H = tổng số nguyên tử H bên phải
nhưng bên tráicó tổng số nguyên tử O > tổng số nguyên tử O bên phải
Cách thăng bằng : Thêm vào bên phải 1 nguyên tử O
b) Cách giải thích : tương tự câu a)
c) Số nguyên tử ở cả 2 phía cân hình 3 bằng nhau
=====> Cách viết PTHH
2H2 + O2 ===> 2H2O

a) Mg + 2HCl --> MgCl2 + H2
b) \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
_____0,2--->0,4--------------->0,2
=> mHCl = 0,4.36,5 = 14,6 (g)
c) VH2 = 0,2.22,4 = 4,48 (l)

1. Tính khối lượng chất tham gia và sản phẩm
* Các bước giải:
- Đổi số liệu đầu bài. Tính số mol của chất mà đầu bài cho.
- Lập phương trình hoá học.
- Dựa vào số mol chất đã biết để tính số mol chất cần tìm.
2. Tính thể tích khí tham gia và tạo thành
H2+Cl2->2HCl
\(n_{H_2}=67,2:22,4=3\left(mol\right)\)
Ta có: \(n_{H_2}=n_{Cl_2}=3\left(mol\right)\)
\(V_{Cl_2}=3.22,4=67,2l\)
\(n_{HCl}=2n_{Cl_2}=2.3=6\left(mol\right)\)
\(m_{HCl}=6.36,5=219g\)

Bài 3 :
- PTHH : \(S+O_2\left(t^o\right)->SO_2\) (1)
- PƯ trên thuộc loại PƯ cháy vì ta phải đốt lưu huỳnh nên có sự cháy giữa lưu huỳnh và oxi
- Ta có : \(n_S=\dfrac{6,4}{32}=0,2\left(mol\right)\)
Từ (1) -> \(n_{O_2}=n_S=0,2\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=n.22,4=0,2.22,4=4,48\left(l\right)\)
Bài 4 :
- PTHH : \(3Fe+2O_2\left(t^o\right)->Fe_3O_4\) (2)
\(n_{Fe}=\dfrac{m}{M}=\dfrac{42}{56}=0,75\left(mol\right)\)
Từ (2) -> \(n_{O_2}=\dfrac{2}{3}n_{Fe}=0,5\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=n.22,4=0,5.22,4=11,2\left(l\right)\)
Từ (2) -> \(n_{Fe_2O_3}=\dfrac{1}{3}n_{Fe}=0,25\left(mol\right)\)
=> \(m_{Fe_2O_3}=n.M=0,25.\left(56.2+16.3\right)=40\left(g\right)\)

ví dụ fe tác dụng với hcl dư tạo thành fecl2 và h2
=> nfecl2 và nh2 sẽ được tính theo fe vì lượng fe pư hết, hcl dư đó bạn
và lượng hcl pư hết cũng đc tính theo lượng fe: nhcl pư= 2nfe
nhcl dư=nhcl ban đầu- nhcl pư hếT
TÓM LẠI TRONG BÀI TOÁN ĐỀ CHO 1 CHẤT DƯ THÌ CHẤT CÒN LẠI SẼ PƯ HẾT, VÀ CÁC CHẤT THU ĐƯỢC TÍNH THEO CHẤT PƯ HẾT ĐÓ BẠN!
mong bạn sẽ hiêu

Cách 1: Tính theo định luật bảo toàn khối lượng:
m K C l = m K + m C l 2 = 39 + 35,5 = 74,5g
Cách 2: Tính theo phương trình hóa học:
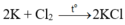
Cứ 6 , 02 . 10 23 nguyên tử K tác dụng với 3 , 01 . 10 23 phân tử Cl2 tạo ra 6 , 02 . 10 23 phân tử KCl. Vậy khối lượng của KCl trong 6 , 02 . 10 23 sẽ bằng 74,5g. (theo câu a)

2. a) 2O
b) 3Ca(OH)2
c) 7NH3
3. Br hóa trị I
S hóa trị II
C hóa trị IV
4. a) - PH3
- CS2
- Fe2O3
b) - Ca(NO3)2
- NaOH
- Al2(SO4)3

Các bước giải :
B1 : Tính khối lượng mol của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
Các bước giải:
Bước 1:Tính khối lượng M của hợp chất.
Bước 2 :Tính số M nguyên tử của mỗi nguyên tố có trong 1 M hợp chất.
Bước 4:Tính phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
☆♡CHÚC BẠN HỌC TỐT♡☆

a) V O2 cần dùng= 20 . 100=2000 ml=2 (l)
--> n O2 =\(\frac{2}{22,4}\)=\(\frac{5}{56}\)(mol)
2KMnO4 --t*--> K2MnO4 + MnO2 + O2
\(\frac{5}{28}\) <------- \(\frac{5}{56}\)(mol)
m KMnO4 = \(\frac{5}{28}\). 158 . (100% + 10%)= 31,04 (g)
b) 2KClO3 ----t*,V2O5----> 2KCl + 3O2 (nhiệt độ, xúc tác)
\(\frac{5}{84}\) <------- \(\frac{5}{56}\)(mol)
m KClO3=\(\frac{5}{84}\).122,5= 7,29(g)
a) Thể tích oxi cần dùng là : (lít).
Số mol khí oxi là : = 0,099 (mol).
Phương trình phản ứng :
2KMnO4 K2MnO4 + MnO2 + O2
2mol 1mol
n mol 0,099 mol
=> n = = 0,198 (mol).
Khối lượng Kali pemaganat cần dùng là :
m = 0,198. (39 + 55 + 64) = 31,3 (g).
b) Phương trình hóa học.
KClO3 2KCl + 3O2
2.122,5 gam 3.22,4 lít
m gam 2,22 lít
Khối lượng kali clorat cần dùng là :
m = (gam).


 A) tại sao cân lệch về phía bên trái hình 1
A) tại sao cân lệch về phía bên trái hình 1
bạn chỉ cần tính số mol hai chất tham gia phản ứng rồi lấy hai số đó chia cho hệ số tỉ lệ trong PTHH, nếu chất nào cao hơn thì chất đó dư
Khi đề cho những dữ kiện liên quan đến tất cả những chất tham gia