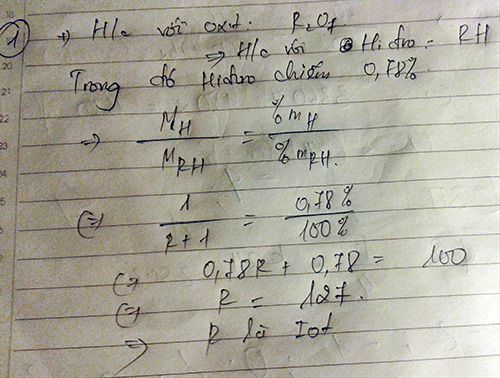Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1 : \(\%_H=\frac{3}{R+3}\cdot100=17.65\)
\(\Rightarrow R=14\)
Vậy R là N(Nitơ)
Câu 2:
Nguyên tố X có hóa trị cao nhất với Oxi gấp 3 lần so vs hc của Hidro nên X thuộc nhóm VIA
hóa trị cao nhất vs Oxi là XO3
mà tỉ khối hơi so với Nitơ là 2.875 tức MXO3 =80.5
MX=32.5
Vậy X là S(Lưu huỳnh)
1.
\(\text{% R= 100-% H= 100-17,65 = 82.35 %}\)
Ta có :
\(\frac{MR}{\%R}=\frac{MH}{\%H}\Rightarrow\frac{MR}{82,35}=\frac{3}{17,65}\)
\(\Rightarrow MR=13,99\approx14\left(đvC\right)\)
\(\rightarrow\)R là nitơ (NH3)
2.
Hóa trị của X vs oxi, hidro lần lượt là x,y
\(\Rightarrow\left\{{}\begin{matrix}\text{x + y = 8}\\\text{x =3y}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\text{x = 6}\\\text{y = 2}\end{matrix}\right.\)
Hợp chất của X vs oxi là XO3
\(\rightarrow\text{M(XO3) = 2,857.28=80}\)
\(\rightarrow\text{X = 32 }\)
\(\rightarrow\)Lưu huỳnh(S)
3.
Hợp chất của R vs Oxi là R2O5
\(\%R=\frac{2R}{\left(2R+16.5\right)}\text{= 0,4366}\)
\(\rightarrow R=31\left(\frac{g}{mol}\right)\)
\(\rightarrow\) R là Photpho
4.
Y tạo vs Oxi hợp chất YO3
\(\rightarrow\) Y tạo vs H hợp chất H2Y
Và Y ở chu kì 3\(\rightarrow\) Y là S
\(\%M=\frac{M}{\left(M+2.32\right)}\text{ = 0,4667}\)
\(\rightarrow\text{M = 56}\)
\(\Rightarrow\)M là Sắt(Fe)
Lần sau bn đăng tách câu hỏi ra cho dễ nhìn nhé

RH4 -> RO2
%R= 53,3% => %O = 100-53,3= 46,7%
\(\dfrac{R}{53,3}\)=\(\dfrac{32}{46,7}\)
giải tìm R

BT1: Công thức trong hợp chất khí với hidro : \(RH_4\)
⇒ Công thức oxit cao nhất : \(RO_2\)
% O = 53,33% ➞ % R= 100 - 53,33 = 46,67%
Ta có : \(\dfrac{\%R}{\%O}=\dfrac{M_R}{M_O}\)
⇔ \(\dfrac{46,67}{53,33}=\dfrac{M_R}{2.16}\)
⇔ \(M_R\)= 28
BT2: Công thức oxit cao nhất: R\(O_3\)
⇒ Công thức trong hợp chất khí với hidro: R\(H_2\)
%H= 5,882% ⇒ %R = 100 - 5,882 = 94,118%
Ta có : \(\dfrac{\%R}{\%H}=\dfrac{M_R}{M_H}\)
⇔ \(\dfrac{94,118}{5,882}=\dfrac{M_R}{2}\)
⇔ \(M_R\)= 32

Công thức hợp chất khí với hidro : \(RH_3\)
⇒ Công thức oxit cao nhất : \(R_2O_5\)
%R = 25,9259% ➝ %O = 100 - 25,9259 = 74,0741%
Ta có : \(\dfrac{\%R}{\%O}=\dfrac{M_R}{M_O}\)
⇔ \(\dfrac{25,9259}{74,0741}=\dfrac{2M_R}{5.16}\)
⇔ \(2M_R\) ≃ 28
⇔ \(M_R\) = 14
⇒ R là Nito (N)
Công thức của \(RH_3\)là : \(NH_3\)
Vậy chọn C

1.
Oxit cao nhất của R là R2O5 → R thuộc nhóm VA
Hợp chất khí của R với H là RH3 trong đó:
\(\%H=\frac{3.1}{3.1+M_R}.100\%=17,65\%\)
\(\rightarrow M_R=14\)
→ R là nito
2.
Oxit cao nhất của R là R2O7 → R thuộc nhóm VIIA
Hợp chất khí của R với H là HR trong đó:
\(\%H=\frac{1.1}{1.1+M_R}.100\%=2,74\%\)
\(\rightarrow M_R=35,5\)
→ R là Clo

1.a. Sơ đồ các quá trình phản ứng
Kim loại + Oxi \(\rightarrow\) (hỗn hợp oxit ) + axit \(\rightarrow\) muối + H2O
Từ quá trình trên => số mol H2SO4 phản ứng = số mol oxi trong oxit
Theo bài ta có: moxi = 39,2 – 29,6 = 9,6(g)
=> \(n_O=\frac{9,6}{16}=0,6mol\)
=> số mol H2SO4 phản ứng = 0,6 (mol)
b. Khối lượng muối = khối lượng kim loại + khối lượng gốc sunfat
=> mm = 29,6 + 96. 0,6 = 87,2 (g)
2. Gọi công thức của oxit cần tìm là MxOy
Phương trình phản ứng.
MxOy + yH2 \(\rightarrow\) xM + yH2O (1)
\(n_{H_2}=\frac{985,6}{22,4.1000}=0,044\left(mol\right)\)
Theo định luật bảo toàn khối lượng
=> khối lượng kim loại = 2,552 + 0,044.2 – 0,044.18 = 1,848(g)
Khi M phản ứng với HCl
2M + 2nHCl \(\rightarrow\) 2MCln + nH2 (2)
\(n_{H_2}=\frac{739,2}{22,4.1000}=0,033\left(mol\right)\)
(2) => \(\frac{1,848}{M}.n=2.0,033\)
=> M = 28n
Với n là hóa trị của kim loại M
Chỉ có n = 2 với M = 56 (Fe) là thỏa mãn
Theo (1) \(\frac{x}{y}=\frac{n_M}{n_{H_2}}=\frac{0,033}{0,044}=\frac{3}{4}\)
=> oxit cần tìm là Fe3O4
1.a. Sơ đồ các quá trình phản ứng
Kim loại + Oxi (hỗn hợp oxit ) + axit muối + H2O
Từ quá trình trên => số mol H2SO4 phản ứng = số mol oxi trong oxit
Theo bài ta có: moxi = 39,2 – 29,6 = 9,6(g)
=>
=> số mol H2SO4 phản ứng = 0,6 (mol)
b. Khối lượng muối = khối lượng kim loại + khối lượng gốc sunfat
=> mm = 29,6 + 96. 0,6 = 87,2 (g)
2. Gọi công thức của oxit cần tìm là MxOy
Phương trình phản ứng.
MxOy + yH2 xM + yH2O (1)
Theo định luật bảo toàn khối lượng
=> khối lượng kim loại = 2,552 + 0,044.2 – 0,044.18 = 1,848(g)
Khi M phản ứng với HCl
2M + 2nHCl 2MCln + nH2 (2)
(2) =>
=> M = 28n
Với n là hóa trị của kim loại M
Chỉ có n = 2 với M = 56 (Fe) là thỏa mãn
Theo (1)
=> oxit cần tìm là Fe3O4