Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- P1 :
CH3COOH + Na -> CH3COONa + ½ H2
CnH2n+1OH + Na -> CnH2n+1ONa + ½ H2
=> mrắn sau = mmuối + mNa dư = mX(1) + 5
Bảo toàn khối lượng : mX(1) + mNa = mrắn sau + mH2
=> nH2 = 0,05 mol => nX(1) = 0,1 mol => naxit = nancol = 0,05 mol
=> mX(1) = 60.0,05 + (14n + 18).0,05 = 3,9 + 0,7n
=> mX(2) = 7,6 – 0,7n
- P2 : Đốt cháy hoàn toàn X(2)
C2H4O2 + 2O2 -> 2CO2 + 2H2O
CnH2n+2O + 1,5nO2 -> nCO2 + (n+1)H2O
CO2 + Ca(OH)2 -> CaCO3 + H2O
2CO2 + Ca(OH)2 -> Ca(HCO3)2
Ca(HCO3)2 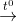 CaCO3 + CO2 + H2O
CaCO3 + CO2 + H2O
Bảo toàn C : nCO2 = nCaCO3(đầu) + 2nCaCO3(sau) = 0,225 mol
=> nX(2) = 0,45/(2+n) (mol)
Mà số mol 2 chất bằng nhau => nX(1) : nX(2) = mX(1) : mX(2)
=> (3,9 + 0,7n).0,45/(2 + n) = (7,6 – 0,7n).0,1
=> n = 1
Vậy ancol là CH3OH

\(n_{hh}=\frac{V}{22,4}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{CaCO_3}=\frac{m}{M}=\frac{30}{100}=0,3\left(mol\right)\)
Gọi x là số mol Ch4 ; y là số mol C2H6
\(CH_4+2O_2\rightarrow CO_2+2H_2O\)
x x
\(C_2H_6+\frac{7}{2}O_2\rightarrow2CO_2+3H_2O\)
y 2y
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,3 0,3
Ta có hê phương trình
\(\hept{\begin{cases}x+y=0,2\\x+2y=0,3\end{cases}}\)
\(\Rightarrow\hept{\begin{cases}x=0,1\left(mol\right)\\y=0,1\left(mol\right)\end{cases}}\)
Vì Số mol hai chất bằng nhau nên thể tích hai chất cũng bằng nhau nên phần trăm thể tích mỗi chất là 50%

- P1:
Gọi x là mol C2H5OH, y là mol CH3COOH mỗi phần
=> 46x+ 60y=(4,6+4,5)/2= 4,55 (1)
C2H5OH+3O2->2CO2+3H2O
CH3COOH+2O2->2CO2+2H2O
=> 88x+ 54x+ 88y+ 36y= 11,75
<=> 142x+ 124y= 11,75 (2)
từ (1) và (2)=> x= 0,05; y= 0,0375
-P2:
C2H5OH+CH3COOH->CH3COOC2H5+H2O
ta có 0,05/1>0,0375/1
=>C2H5OH dư
nCH3COOC2H5=0,0375 mol
mà H=60%
=>m=0,0375x88x60%=1,98 g

\(M_{NO}=M_{C2H6}=30\rightarrow M_{Y'}=1,35.30=40,5,y=0,04mol\)
Gọi x,y là số mol của NO,N2O trong hh ta có hệ:
\(\begin{cases}30x+44y=0,04.40,5\\x+y=0,04\end{cases}\) \(\Rightarrow n_{NO}=x=0,01,n_{N2O}=0,03\)
Gọi a,b là số mol của Fe,R trong 3,3 gam hỗn hợp:
\(Fe+HCl\rightarrow FeCl_2+H_2\)
\(R+nHCl\rightarrow RCl_n+\frac{n}{2H2}\)
\(\Rightarrow56a+Rb=3,3\) (*)
\(\Rightarrow a+\frac{bn}{2}=0,12\) (**)
Hòa tan X trong HNO3
Quá trình oxi hóa
Fe →Fe3+ +3e
R→ Rn+ +ne
Quá trình khử:
NO3- +4H+ +3e → NO +2H2O
0,04 ← 0,03 ←0,01
NO3- +8H+ +8e → N2O +2H2O
0,3 ← 0,24 ←0,03
Áp dụng bảo toàn electron ta có
3a+ nb =0,27 (3)
Từ 2,3 → a=0,03 ,nb=0,18 thay vào 1 ta có: R=9n → n=3,R=27 → là Al
%Fe=(0,03.56/3,3).100%=50,91% → %Al = 49,09%
b, nHNO3pu =nH+ =0,04+0,3=0,34 mol
%Fe=(0,03.56/3,3).100%=50,91% → %Al = 49,09%
b, nHNO3pu =nH+ =0,04+0,3=0,34 mol
nHNO3du =0,01.0,34=0,034 mol=nH+ dư
cho NaOH vào Z
H+ + OH- → H2O
0,034→0,034
Fe3+ + 3OH- → Fe(OH)3
0,03→0,09→0,03
Al3+ + 3OH- → Al(OH)3
Al(OH)3 + OH- →AlO2- + 2H2O
Vì Fe(OH)3 kết tủa hết → nAl(OH)3 =(4,77-3,21)/78=0,02 mol < nAl3+ =0,06 mol → có 2 trường hợp
TH1 : Al3+ dư → nNaOH =0,034 +0,09 +0,06 =0,184 mol → CM(NaOH)=0,184/0,4=0,46M
TH2: Al3+ hết → nNaOH =0,034 +0,09 +0,18 +0,04 =0,344 mol → CM(NaOH)=0,344/0,4=0,86M
