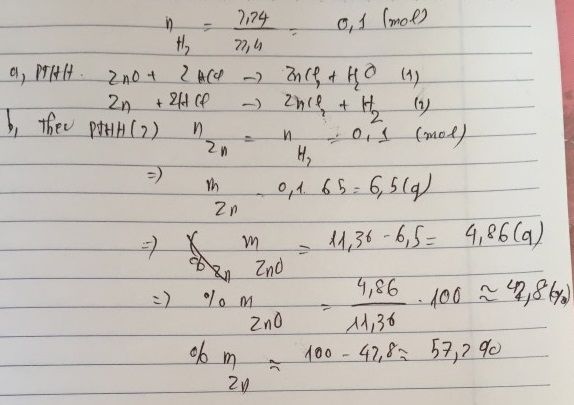Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sửa đề: Sau phản ứng thu đc \(2240(cm^3)\) lít khí (đktc)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ ZnO+2HCl\to ZnCl_2+H_2O\\ b,n_{Zn}=n_{H_2}=0,1(mol)\\ \Rightarrow m_{Zn}=0,1.65=6,5(g)\\ \Rightarrow \%_{Zn}=\dfrac{6,5}{14,6}.100\%= 44,52\%\\ \Rightarrow \%_{ZnO}=100\%-44,52\%=55,48\%\\ n_{ZnO}=\dfrac{14,6-6,5}{81}=0,1(mol)\\ \Sigma n_{ZnCl_2}=n_{Zn}+n_{ZnO}=0,1+0,1=0,2(mol)\\ \Rightarrow C_{M_{ZnCl_2}}=\dfrac{0,2}{0,2}=1M\)

a) $Zn + 2HCl \to ZnCl_2 + H_2$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
b)
Theo PTHH : $n_{Zn} = n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$m_{Zn} = 0,2.65 = 13(gam)$
$m_{ZnO} = 21,1 - 13 = 8,1(gam)$
c) $n_{ZnO} = 0,1(mol)$
Theo PTHH : $n_{HCl} = 2n_{Zn} + 2n_{ZnO} = 0,6(mol)$
$m_{dd\ HCl} = \dfrac{0,6.36,5}{16,6\%} = 132(gam)$
d) $m_{dd\ sau\ pư} = 21,1 + 132 - 0,2.2 = 152,7(gam)$
$n_{ZnCl_2} = n_{Zn} + n_{ZnO} = 0,3(mol)$
$C\%_{ZnCl_2} = \dfrac{0,3.136}{152,7}.100\% = 26,72\%$

\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2.........0.4.........0.2......0.2\)
\(m_{Zn}=0.2\cdot65=13\left(g\right)\Rightarrow m_{ZnO}=14.6-13=1.6\left(g\right)\)
\(\%Zn=\dfrac{13}{14.6}\cdot100\%=89.04\%\)
\(\%ZnO=100\%-89.04\%=10.96\%\)
\(n_{ZnO}=\dfrac{1.6}{81}\approx0.02\left(mol\right)\)
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
\(0.02........0.04........0.02........0.02\)
\(n_{HCl}=0.4+0.04=0.44\left(mol\right)\)
\(C_{M_{HCl}}=\dfrac{0.44}{0.8}=0.55\left(M\right)\)
Eeeee ngồi tính sang chấn thật nó ra số xấu lần mò hơn 20p chưa biết tính sai chỗ nào

\(n_{Fe}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1
a) \(n_{Fe}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
⇒ \(m_{Cu}=12-5,6=6,4\left(g\right)\)
b) \(n_{HCl}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddHCl}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
c) 0/0Fe = \(\dfrac{5,6.100}{12}=46,67\)0/0
0/0Cu = \(\dfrac{6,4.100}{12}=53,33\)0/0
Chúc bạn học tốt

Tiếp bài của creeper nhé:
c. Ta có: \(n_{ZnO}=\dfrac{4,86}{81}=0,06\left(mol\right)\)
Theo PT(1): \(n_{HCl}=2.n_{ZnO}=2.0,06=0,12\left(mol\right)\)
Theo PT(2): \(n_{HCl}=2.n_{Zn}=2.0,1=0,2\left(mol\right)\)
=> \(n_{HCl}=0,12+0,2=0,32\left(mol\right)\)
=> \(m_{HCl}=0,32.36,5=11,68\left(g\right)\)
Ta có: \(C_{\%_{HCl}}=\dfrac{11,68}{m_{dd_{HCl}}}.100\%=12\%\)
=> \(m_{dd_{HCl}}=\dfrac{292}{3}\left(g\right)\)
Theo đề, ta có:
\(D=\dfrac{\dfrac{292}{3}}{V_{dd_{HCl}}}=1,2\)(g/ml)
=> \(V_{dd_{HCl}}=81,1\left(ml\right)\)

Do sau phản ứng là hh chất rắn nên Mg dư, FeCl3 hết
PTHH
Mg + 2FeCl3 --> MgCl2 + 2FeCl2
x 2x 2x
Mg + FeCl2 --> MgCl2 + Fe
2x 2x 2x
3Mg + 2FeCl3 --> 3MgCl2 + 2Fe
y 2/3y 2/3y
Theo PTHH ta có: nFeCl3 = nFe = 0.2
2nMg = 3nFe = 0.3
nMg = nMgCl2 = 0.3
Nồng độ mol của các chất trong hh:
CmFeCl2 = 0.2/0.4 = 0.5M
CmMgCl2 = 0.3/0.4 = 0.75M
PTHH
Fe + 2HCl --> FeCl2 + H2
0.2 0.4
Mg + 2HCl --> MgCl2 + H2
0.3 0.6
Khối lượng HCl cần dùng: m = 1*36.5 = 36.5g
với lại bài này có cho Mg tác dụng với FeCl2 hay là chỉ cho tác dụng với FeCl3 với lại cho mình bik vì sao khi làm nhớ giải thích giùm mình nhé thank you

nH2=\(\frac{6,72}{22,4}=0,3\)mol
PTHH
M+2HCl--> MCl2+H2
0,3mol<---------------0,3mol
=>MM=\(\frac{19,5}{0,3}=64\)
=> km loại là kẽm (Zn)
b) nNaOH=0,2.1=0,2 mol
PTHH
NaOH+HCl-->NaCl + H2O
0,2 mol--> 0,2 mol
---> thể tích HCl 1M đã dùng là V=\(\frac{0,2+0,3}{1}=0,5\)lít
=> CM(ZnCl2)=\(\frac{0,3}{0,5}=0,6M\)