Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sản phẩm oxi hoá qua bình (1) đựng dung dịch H2SO4 đặc làm khối lượng bình (1) tăng 0,63 g chính là lượng nước bị giữ lại => mH = 0,63180,6318 x 2 = 0,07 g.
Qua bình (2) chứa dung dịch Ca(OH)2 dư, làm cho bình xuất hiện kết tủa chính là do lượng CO2 bị giữ lại vì tham gia phản ứng sau:
Ca(OH)2 + CO2 → CaCO3 + H2O
0,05 51005100 = 0,05 mol
=> mC = 0,05 x 12 = 0,6 (g).
=> mO = 0,67 - (mC + mH) = 0
Từ đó tính được %mC = 89,55%; %mH = 10,45%.

Gọi công thức phân tử của X là CxHyOz .
Sản phẩm cháy gồm CO2 và H2O.
Ở lần thí nghiệm thứ nhất, bình 1 chứa H2SO4 đậm đặc dư hấp thụ H2O và bình 2 chứa dung dịch nước vôi trong dư hấp thụ CO2.
Ở lần thí nghiệm thứ hai, bình 1 chứa CaO dư hấp thụ CO2 và toàn bộ hơi nước, bình 2 chứa P2O5 dư không hấp thụ gì vì toàn bộ lượng khí đã được hấp thụ ở bình 1. Do đó m2 = 0. Theo định luật bảo toàn khối lượng ta có
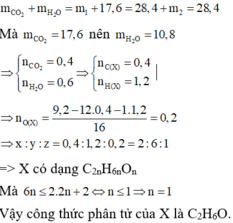

$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{CO_2} = n_{CaCO_3} = \dfrac{12}{100} = 0,12(mol)$
Ta có : $m_{bình\ tăng} = m_{CO_2} + m_{H_2O}$
$\Rightarrow m_{H_2O} = 8,16 - 0,12.44 = 2,88(gam)$
$\Rightarrow n_{H_2O} = 0,16(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 0,12(mol)$
$n_H = 2n_{H_2O} = 0,32(mol)$
$\Rightarrow m_O = m_X - m_C - m_H = 1,28(gam) \Rightarrow n_O = \dfrac{1,28}{16} = 0,08(mol)$
Ta có :
$n_C : n_H : n_O = 0,12 : 0,32 : 0,08 = 3 : 8 : 2$
Vậy CTPT của X : $(C_3H_8O_2)_n$
$M_X = 76n = M_{H_2}.38 = 76 \Rightarrow n = 1$
Vậy CTPT là $C_3H_8O_2$

Đáp án A
Khối lượng bình 1 tăng là khối lượng của H2O => nH2O = 1,8/18 = 0,1 mol
Khối lượng bình 2 tăng là khối lượng của CO2 => nCO2 = 3,52/44 = 0,08 mol
Nhận thấy: nCO2 < nH2O => hidrocacbon là ankan;
Số mol ankan là nankan = 0,1 – 0,08 = 0,02 mol
Phương trình phản ứng:
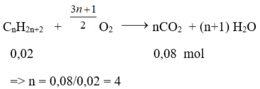
CTPT của A là C4H10

\(M_{luminol}=6,65518.29=193\left(g/mol\right)\)
\(n_{N_2}=\dfrac{1,1088}{22,4}=0,0495\left(mol\right)\)
Phân tích 6,369 gam luminol thu được 0,0495 mol khí N2
`=>` Phân tích 2,895 gam luminol thu được 0,0225 mol khí N2
Ta có: \(\left\{{}\begin{matrix}m_{b\text{ìn}h.1.t\text{ăng}}=m_{H_2O}=0,945\left(g\right)\\m_{b\text{ình}.2.t\text{ăng}}=m_{CO_2}=5,28\left(g\right)\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}n_{H_2O}=\dfrac{0,945}{18}=0,0525\left(mol\right)\\n_{CO_2}=\dfrac{5,28}{44}=0,12\left(mol\right)\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}n_C=n_{CO_2}=0,12\left(mol\right)\\n_H=2n_{H_2O}=0,105\left(mol\right)\\n_N=2n_{N_2}=0,045\left(mol\right)\\n_O=\dfrac{m_{luminol}-m_C-m_H-m_N}{16}=\dfrac{2,895-0,12.12-0,105-0,045.14}{16}=0,045\left(mol\right)\end{matrix}\right.\)
`=>` \(n_C:n_H:n_O:n_N=0,12:0,105:0,045:0,045=8:7:3:3\)
`=>` CTHH của luminol có dạng \(\left(C_8H_7O_3N_3\right)_n\)
`=>` \(n=\dfrac{193}{193}=1\)
Vậy CTHH của luminol là C8H7O3N3