Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Kết tủa là CaCO3 \(\rightarrow\)nCaCO3=\(\frac{150}{100}\)=1,5 mol
Đun kĩ dung dịch thu được thêm 0,5 mol CaCO3 nữa
Chứng tỏ dung dịch có chứa Ca(HCO3)2
Ca(HCO3)2 \(\rightarrow\) CaCO3 + CO2 + H2O
\(\rightarrow\)nCa(HCO3)2=nCaCO3 tạo ra thêm =0,5 mol
Bảo toàn C: nCO2=nCaCO3 (ban đầu) +2nCa(HCO3)2
=1,5+0,5.2=2,5 mol
\(\rightarrow\) V CO2=2,5.22,4=56 lít

Điều nào sau đây không đúng cho phản ứng của khí CO với khí O2?
A. Phản ứng thu nhiệt.
B. Phản ưng tỏa nhiệt.
C. Phản ứng kèm theo sự giảm thể tích.
D. Phản ứng không xảy ra ở điều kiện thường.
Điều nào sau đây không đúng cho phản ứng của khí CO với khí O2?
A. Phản ứng thu nhiệt.
B. Phản ưng tỏa nhiệt.
C. Phản ứng kèm theo sự giảm thể tích.
D. Phản ứng không xảy ra ở điều kiện thường.

CO2 + Ca(OH)2 → CaCO3 + H2O
0,1 0,1 0,1
2CO2 + CaCO3 + H2O → Ca(HCO3)2
0,16 – 0,1 → 0,06
=> n↓= 0,04 mol
n↓= 0,04 mol => m ↓ = 4g < 0,16 . 44 = 7,04g
=> mdd tăng = 7,04 – 4 = 3,04g
nCa(OH)2 = 2.0,05=0,1(mol)
ta có nCO2/nCa(OH)2 = 0,16/0,1 = 1,6
=> có 2 phản ứng xảy ra
CO2 + Ca(OH)2 ---> CaCO3 + H2O (1)
2CO2 +Ca(OH)2 ---> Ca(HCO3)2 (2)
bảo toàn C ta có x +2y = 0,16(3)
bảo toàn Ca ta có x +y = 0,1 (4)
từ (3) và (4) => x= 0,04(mol) y= 0,06(mol)
mCa(HCO3) = 0,06.145= 8,7(g)
m Ca(OH)2 = 0,1.57 = 5,7g
vậy khối lượng của Ca(HCO3)2 tăng 3g so với Ca(OH)2 ban đầu

Quy đổi hỗn hợp 19.20g gồm Fe, FeO, Fe3O4 vào Fe2O3 dư.thành Fe và O bạn lập hệ giữa khối lượng và bảo toàn e với No2 tính đc nFe , vì Hỗn hợp A gồm Fe2O3,Fe3O4, FeO với số mol như nhau nên bạn gọi a là mol mỗi oxit và bảo toàn nguyên tố với nFe mk vừa tính đc xong tính đc x bảo toàn khối lượng --> y . nCo=nCo2=y/197
Chúc bạn học tốt!

1. nCa(OH)2=15*0,01=0,15 mol
Khi sục khí CO2 vào thì kết tủa xuất hiện:
CO2 + Ca(OH)2 -> CaCO3 + H20
Ta có: nCO2 : nCa(OH)2 = 1:1
Mà: 0,02 <= n CO2 <= 0,17 nên CO2 dư,kết tủa bị hòa tan
CaCO3 +H20 + CO2 -> Ca(HCO3)2 (tan)
Tỉ lệ là 1:1 nên kết tủa thu được nhiều nhất khi nCO2=nCa(OH)2=0,15 mol => mCaCO3=15g
* Xét khoảng 0,02 <= n CO2 <= 0,15, lúc này số mol CO2 càng tăng thì khối lượng kết tủa càng lớn => Khối lượng kết tủa nhỏ nhất khi nCO2 = 0,02 mol => mCaCO3=0,02* 100 = 2g
* Xét khoảng 0,15 < n CO2 <= 0,17, lúc này số mol CO2 càng tăng thì khối lượng kết tủa càng giảm=> nCO2 có thể dư nhiều nhất là 0,17 - 0,15=0,02 mol => nCaCO3 bị hòa tan = nCO2 =0,02
=> mCaCO3 thu được khi nCO2= 0,17 mol là: 0,15 - 0,02*100 = 13g
Vậy khối lượng kết tủa thu được trong khoảng [2;15]g
Chúc bạn học tốt!

phương trình phản ứng : mgco3---->mgo+co2
0.28(mol) <-- 0.28
koh+co2--->k2co3(muối tan)+h2o
0.2->0.2(mol)
ca(oh)2+co2--->caco3 (kết tủa)+ h20
0.08 < -- 0.08 < -- 0.08 (mol)
nkoh=0.1*2=0.2(mol)
nca(oh)2=005*2=0.1(mol)
ncaco3=8/100=0.08 (mol)
\(\Sigma\)no2=0.28(mol)
--->mmgco3=0.28*84=23.52(gam)
phương trình phản ứng : mgco3---->mgo+co2
0.28(mol) <-- 0.28
koh+co2--->k2co3(muối tan)+h2o
0.2->0.2(mol)
ca(oh)2+co2--->caco3 (kết tủa)+ h20
0.08 < -- 0.08 < -- 0.08 (mol)
nkoh=0.1*2=0.2(mol)
nca(oh)2=005*2=0.1(mol)
ncaco3=8/100=0.08 (mol)
Σno2=0.28(mol)
--->mmgco3=0.28*84=23.52(gam)
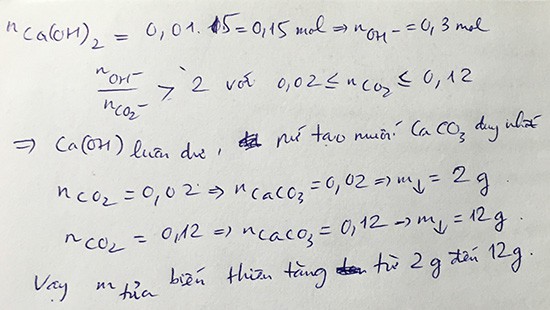

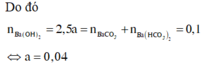
\(n_{CO_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=1.0,1=0,1\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
______0,1------->0,1--------->0,1
CaCO3 + CO2 + H2O --> Ca(HCO3)2
_0,02<--0,02
=> mCaCO3 = (0,1-0,02).100 = 8(g)