Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
b, Gọi: \(\left\{{}\begin{matrix}n_{KClO_3}=x\left(mol\right)\\n_{KMnO_4}=y\left(mol\right)\end{matrix}\right.\) ⇒ 122,5x + 158y = 43,85 (1)
Ta có: \(n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{3}{2}n_{KClO_3}+\dfrac{1}{2}n_{KMnO_4}=\dfrac{3}{2}x+\dfrac{1}{2}y=0,25\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{0,1.122,5}{43,85}.100\%\approx27,94\%\\\%m_{KMnO_4}\approx72,06\%\end{matrix}\right.\)

1)
Gọi số mol KMnO4, KClO3 là a, b (mol)
=> 158a + 122,5b = 308,2 (1)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
a-------------------------------->0,5a
2KClO3 --to--> 2KCl + 3O2
b------------------>1,5b
=> mO2 = (0,5a + 1,5b).32 = 16a + 48b (g)
mD = 308,2 - 16a - 48b(g)
\(m_{Mn}=\dfrac{\left(308,2-16a-48b\right).10,69}{100}=32,94658-1,7104a-5,1312b\left(g\right)\)
=> \(n_{Mn}=\dfrac{32,94658-1,7104a-5,1312b}{55}=0,6-\dfrac{1069}{34375}a-\dfrac{3207}{34375}\left(mol\right)\)
Mà \(n_{Mn}=n_{KMnO_4}=a\left(mol\right)\)
=> \(\dfrac{35444}{34375}a+\dfrac{3207}{34375}b=0,6\) (2)
(1)(2) => a = 0,4 (mol); b = 2 (mol)
=> \(\left\{{}\begin{matrix}\%m_{KMnO_4}=\dfrac{0,4.158}{308,2}.100\%=20,506\%\\\%m_{KClO_3}=\dfrac{2.122,5}{308,2}.100\%=79,494\%\end{matrix}\right.\)
2)
Giả sử nung 100 (g) đá vôi
=> \(m_{CaCO_3\left(bđ\right)}=\dfrac{80.100}{100}=80\left(g\right)\)
\(m_{rắn.sau.pư}=\dfrac{100.73,6}{100}=73,6\left(g\right)\)
=> mCO2 = 100 - 73,6 = 26,4 (g)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
0,6<----------------0,6
=> mCaCO3(pư) = 0,6.100 = 60 (g)
\(H\%=\dfrac{60}{80}.100\%=75\%\)

PTHH: \(2KClO_3\xrightarrow[t^o]{MnO_2}2KCl+3O_2\\ xmol\rightarrow xmol:\dfrac{3}{2}xmol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\\ ymol\rightarrow\dfrac{y}{2}mol:\dfrac{y}{2}mol:\dfrac{y}{2}mol\)
Gọi số mol của Kaliclorat và Kali pemaganat lần lượt là x và y.
\(n_{O_2}=\dfrac{73,92}{22,4}=3,3\left(mol\right)\)
\(122,5x+158y=410,1\left(g\right)\left(1\right)\)
\(\dfrac{3}{2}x+\dfrac{1}{2}y=3,3\left(mol\right)\left(2\right)\)
Giải phương trình (1) và (2) ta được: \(\left\{{}\begin{matrix}x=1,8\\y=1,2\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_{KClO_3}=122,5.1,8=220,5\left(g\right)\\m_{KMnO_4}=410,1-220,5=189,6\left(g\right)\end{matrix}\right.\)
\(n_{O_2}=\dfrac{73,92}{22,4}=3,3\left(mol\right)\)
PTHH:
\(2KClO_3-t^o->2KCl+3O_2\uparrow\)
x...........................................x....................1,5x
\(2KMnO_4-t^o->K_2MnO_4+MnO_2+O_2\uparrow\)
y..................................................0,5y.................0,5y...............0,5y
Gọi x, y lần lượt là số mol của \(KClO_3;KMnO_4\)
Ta có hệ PT:
\(\left\{{}\begin{matrix}122,5x+158y=410,1\\1,5x+0,5y=3,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=1,8\\y=1,2\end{matrix}\right.\)
=> \(m_{KClO_3}=122,5.1,2=220,5\left(g\right)\)
=> \(m_{KMnO_4}=1,2.158=189,6\left(g\right)\)

a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, Ta có: \(n_{HCl}=0,5.0,2=0,1\left(mol\right)\)
\(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
Theo PT: \(n_{HCl\left(pư\right)}=2n_{H_2}=0,08\left(mol\right)< 0,1\left(mol\right)\)
→ HCl dư.
Gọi: \(\left\{{}\begin{matrix}n_{Zn}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
Theo PT: \(n_{H_2}=n_{Zn}+n_{Fe}=x+y=0,04\left(1\right)\)
\(\left\{{}\begin{matrix}n_{ZnCl_2}=n_{Zn}=x\left(mol\right)\\n_{FeCl_2}=n_{Fe}=y\left(mol\right)\end{matrix}\right.\)⇒ 136x + 127y = 5,26 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,02\left(mol\right)\\y=0,02\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,02.65}{0,02.65+0,02.56}.100\%\approx53,72\%\\\%m_{Fe}\approx46,28\%\end{matrix}\right.\)

\(a.MgCO_3-t^{^0}->MgO+CO_2\\ CaCO_3-t^{^0}->CaO+CO_2\\ b.n_{MgCO_3}=a,n_{CaCO_3}=b\\ 84a+100b=26,8\\ 40a+56b=13,6\\ a=0,2;b=0,1\\ \%m_{MgCO_3}=\dfrac{84a}{26,8}.100\%=62,69\%\\ \%m_{CaCO_3}=37,31\%\\ c.V_{CO_2}=22,4\left(a+b\right)=6,72L\)

Khối lượng oxi thoát ra: m O 2 = 197 + 3 – 152 = 48(g)
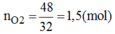
PTHH của phản ứng:
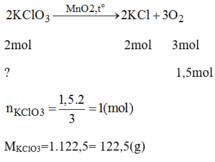
Khối lượng của KCl trong hỗn hợp ban đầu:
m K C l = 197-122,5 = 74,5(g)
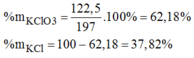

Gọi \(n_{KClO_3}=a,n_{KMnO_4}=b\)
\(2KClO_3\underrightarrow{t_o}2KCl+3O_2\)
a \(\dfrac{3}{2}a\)
\(2KMnO_4\underrightarrow{t_o}K_2MnO_4+MnO_2+O_2\)
b \(\dfrac{1}{2}b\)
\(n_{O_2}=\dfrac{49,28}{22,4}=2,2mol\)
Ta có hệ:
\(\left\{{}\begin{matrix}122,5a+158b=47,2\\\dfrac{3}{2}a+\dfrac{1}{2}b=2,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}a=\dfrac{1296}{703}\\b=-\dfrac{3974}{3515}\end{matrix}\right.\)
Đề bị lỗi rồi em nhé!!!

$n_{Kali} = \dfrac{21,65.36,03\%}{39} = 0,2(mol)$
Gọi $n_{KMnO_4} = a ; n_{KClO_3} = b$
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
Bảo toàn Kali : $a + b = 0,2$
$n_{O_2} = 0,5a + 1,5b(mol)$
Bảo toàn khối lượng : $158a + 122,5b = 21,65 + (0,5a + 1,5b).32$
Suy ra: a = b = 0,1
$n_{O_2} = 0,5a + 1,5b = 0,2(mol)$
$V_{O_2} = 0,2.22,4 = 4,48(lít)$

\(2KClO_3\rightarrow3O_2+2KCl\)
\(m_{KClO_3}=m_{O_2}+m_{KCl}\)
\(\Rightarrow m_{KCl}=m_{KClO_3}-m_{KCl}=24,5-9,6=14,9\left(g\right)\)
phân tích 273g hỗn hợp muối KClO3 và KMnO4 ta thu được 49.27l oxi (đktc)
a,Viết phương trình hóa học phản ứng
b, Tính thành phần % khối lượng của các chất có trong hỗn hợp muối
\(a) PTHH:\)
\(2KClO3 -(nhiệt)-> 2KCl + 3O2\) (1)
\(2KMnO4 -(nhiệt)-> K2MnO4 + MnO2 +O2\)(2)
\(b)\)
Đặt a là nKClO3, b là nKMnO4
Ta có: 122,5a 158b
Ta có: \(122,5a + 158b = 273 \) (I)
nO2 thu được = \(\dfrac {49,27} {22,4}\)= \(2,1995 (mol) \)
Theo (1) và (2): \(1,5a + 0,5b = 2,1995\) (II)
Giai hệ (I) và (II), \(\begin{cases} a=1,2 \\ b = 0,8 \end{cases}\)
%mKClO3 = \(\frac{1,2.122,5.100}{273}\) = 53,85%
=> %mKMnO4 = 100% - 53,85% = 46,15%
PTHH: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\left(1\right)\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\left(2\right)\)
\(n_{O_2}=\dfrac{49,27}{22,4}=\dfrac{4927}{2240}\left(mol\right)\)
Đặt số mol KClO3 là x, số mol KMnO4 là y, ta có hệ:
\(\left\{{}\begin{matrix}122,5x+158y=273\\1,5x+0,5y=\dfrac{4927}{2240}\end{matrix}\right.\)
\(\left\{{}\begin{matrix}x=1,200736639\\y=0,7968972262\end{matrix}\right.\)
\(m_{KClO_3}=1,200736639.122,5=147,0902383\left(g\right)\)
\(m_{KMnO_4}=273-147,0902383=125,9097617\left(g\right)\)
\(\%KClO_3=\dfrac{147,0902383}{273}.100\%=53,88\%\)
\(\%KMnO_4=100\%-53,88\%=46,12\%\)