
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1) Ta coi H2SO4 điện li mạnh hai nấc.
\(n_{H_2SO_4}=0,03\) mol; \(n_{HCl}=0,16\) mol
\(H_2SO_4\rightarrow2H^++SO_4^-\)
0,03 -----> 0,06 ---> 0,03
\(HCl\rightarrow H^++Cl^-\)
0,16 --> 0,16 --> 0,16
\(\Rightarrow n_{H^+}=2n_{H_2SO_4}+n_{HCl}=2.0,03+0,16=0,22\) mol
+ \(\left[H^+\right]=\dfrac{0,22}{1+4}=0,044\) mol/lít
\(\Rightarrow pH=-lg\left[H^+\right]=-lg0,044=1,36\)
+ \(\left[SO_4^-\right]=\dfrac{0,03}{1+4}=6.10^{-3}\) mol/lít
+ \(\left[Cl^-\right]=\dfrac{0,16}{1+4}=0,032\) mol/lít
2) + \(n_{OH^-}=n_{NaOH}+2n_{Ba\left(OH\right)_2}=0,12\) mol
\(\Rightarrow\left[OH^-\right]=\dfrac{0,12}{5}=0,024\) mol/lít
\(\Rightarrow pOH=-lg\left[OH^-\right]=1,62\)
\(\Rightarrow pH=14-pOH=12,38\)
+ \(n_{Na^+}=n_{NaOH}=0,06\) mol
\(\Rightarrow\left[Na^+\right]=\dfrac{0,06}{5}=0,012\) mol/lít
+ \(n_{Ba^{2+}}=n_{Ba\left(OH\right)_2}=0,03\) mol
\(\Rightarrow\left[Ba^{2+}\right]=\dfrac{0,03}{5}=0,006\) mol/lít

Trong 100 ml thì :
\(n_{H^+}=0.1\cdot\left(0.015\cdot2+0.03+0.04\right)=0.01\left(mol\right)\)
Trong 200 ml :
\(n_{H^+}=0.01\cdot2=0.02\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.02.......0.02\)
\(V_{dd_{NaOH}}=\dfrac{0.02}{0.2}=0.1\left(l\right)\)

\(n_{HCl}=0,1.0,1=0,01\left(mol\right);n_{HCl}=0,3.0,04=0,012\left(mol\right)\)
Dung dịch gồm H+ và Cl-
\(n_{H^+}=0,01+0,012=0,022\left(mol\right)\)
=> \(\left[H^+\right]=\dfrac{0,022}{0,4}=0,055M\)
\(n_{Cl^-}=0,01+0,012=0,022\left(mol\right)\)
=>\(\left[Cl^-\right]=\dfrac{0,022}{0,4}=0,055M\)
Trộn 100ml dung dịch HNO3 0.1M với 400ml dung dịch H2SO4 0.03M
\(n_{HNO_3}=0,1.0,1=0,01\left(mol\right);n_{H_2SO_4}=0,04.0,3=0,012\left(mol\right)\)
Dung dịch sau khi trộn gồm :
\(n_{H^+}=0,01+0,012.2=0,034\left(mol\right)\)
=> \(\left[H^+\right]=\dfrac{0,034}{0,5}=0,068M\)
\(n_{NO_3^-}=0,01\left(mol\right)\)
=>\(\left[NO_3^-\right]=\dfrac{0,01}{0,5}=0,02M\)
\(n_{SO_4^{2-}}=0,012\left(mol\right)\)
=> \(\left[SO_4^{2-}\right]=\dfrac{0,012}{0,5}=0,024M\)

Đáp án C
2 dung dịch có thể tích bằng nhau ⇒ nOH-/ Ba(OH)2 = 2nH+/ HCl
H+ + OH- → H2O
0,2V 0,4V (mol)
Phản ứng : 0,2V → 0,2V (mol)
⇒ Trong dung dịch thu được có OH- dư
Trộn 2 dung dịch có cùng thể tích ⇒ [OH-] dư = 0,2 : 2 = 0,1M
⇒ pH = 13.
Đáp án C.

Đáp án C
nBa(OH)2 = 0,2.a mol; nOH-= 0,4a mol
dung dịch H2SO4 có pH = 1 nên [H+] = 10-1 M
→nH+ = [H+].Vdd = 0,3.10-1 = 0,03 mol, nSO4(2-) = 0,015 mol
H2SO4→ 2H++ SO42-
0,03 →0,015 mol
Ba(OH)2→ Ba2++ 2OH-
0,2a→ 0,2a 0,4a
H+ + OH- → H2O
0,4a 0,4a
Dung dịch sau phản ứng có pH = 2 nên axit dư
nH+ dư = 0,03-0,4a
[H+] dư = nH+ dư/ Vdd = (0,03-0,4a)/0,5 = 10-2 suy ra a = 0,0625 M
Ba2++ SO42- → BaSO4
0,0125 0,015 0,0125 mol
mBaSO4 = 2,9125 gam
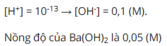
\(\left[OH^-\right]=0,04.2=0,08M\\ pOH=-log\left(0,08\right)=1,097\\ \Rightarrow pH=14-1,097=12,903\)