
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O(1)$
$Fe_2(SO_4)_3 + Fe\ to 3FeSO_4(2)$
Gọi $n_{Fe_2(SO_4)_3} = a(mol) ; n_{FeSO_4} = b(mol)$
Ta có : $400a + 152b = 62,8(1)$
$n_{SO_2} = 0,15(mol)$
$n_{Fe_2(SO_4)_3(1)} = \dfrac{1}{3}n_{SO_2} = 0,05(mol)$
$n_{Fe_2(SO_4)_3(2)} = \dfrac{1}{3}n_{FeSO_4} = \dfrac{b}{3}$
Suy ra:
$0,05 - \dfrac{b}{3} = a(2)$
Từ (1)(2) suy ra $a = \dfrac{45}{112} ; b = -1,055<0$
=> Sai đề

X: Fe3O4
Y: FeCl2
Z: FeCl3
T: Fe(OH)2
U: Fe(OH)3
A: NaCl (hoặc H2O)
B: H2O (hoặc NaCl)
D: H2 (hoặc Cl2)
E: Cl2 (hoặc H2)
F: NaOH
G: HCl
PTHH:
a) NaCl + H2O -dpmn----> 1/2 H2 + 1/2 Cl2 + NaOH
H2 + Cl2 -to-> 2 HCl
HCl + NaOH -> NaCl + H2O
b) 3 Fe +2 O2 -to->Fe3O4
Fe3O4 + 8 HCl -> FeCl2 +2 FeCl3 + H2O
FeCl2 + 2 NaOH -> Fe(OH)2 + 2 NaCl
FeCl3 +3 NaOH -> Fe(OH)3 + 3NaCl
Chúc em học tốt!

PTHH: Al2O3+6HCl➝2AlCl3+3H2O(1)
a)nAl2O3=\(\dfrac{10,2}{102}\)=0,1(mol)
mHCl=\(\dfrac{5\%.219}{100\%}\)=10,95(g)
⇒nHCl=\(\dfrac{10,95}{36,5}\)=0,3(mol)
Xét tỉ lệ Al2O3:\(\dfrac{0,1}{1}\)=0,1
Xét tỉ lệ HCl:\(\dfrac{0,3}{6}\)=0,05
⇒HCl pứng hết,Al2O3 còn dư
Theo PTHH(1) ta có nAl2O3 pứng=\(\dfrac{nHCl}{6}\)=\(\dfrac{0,3}{6}\)=0,05(mol)
⇒nAl2O3 dư=nAl2O3ban đầu-nAl2O3 pứng=0,1-0,05=0,05(mol)
⇒mAl2O3 dư=0,05.102=5,1(g)
b) C%HCl=\(\dfrac{0,3.36,5}{219+10,2}\).100%=4,8%
nAlCl3=0,1(mol)
⇒C%AlCl3=\(\dfrac{0,1.136,5}{10,2+219}\).100%=6%

alo giúp mik Nhân dịp đi du lịch về, Mai mang đến lớp 51 móc chìa khóa để tặng cho cácbạn. Sau khi chia hết cho các bạn (tính cả mình) thì Mai còn thừa3chiếc. Hỏi lớpMai có bao nhiêu bạn, biết số học sinh nhiều hơn 20 và ít hơn 30 bạn.

PTHH: \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
Ta có: \(\left\{{}\begin{matrix}m_{H_2SO_4}=588\cdot5\%=29,4\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\\n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,3}{3}\) \(\Rightarrow\) Al2O3 còn dư
\(\Rightarrow n_{Al_2\left(SO_4\right)_3}=0,1\left(mol\right)=n_{Al_2O_3\left(dư\right)}\)
\(\Rightarrow C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,1\cdot342}{20,4+588-0,1\cdot102}\cdot100\%\approx5,72\%\)

CuO + H2SO4 \(\rightarrow\)CuSO4 + H2O (1)
Cr2O3 + 3H2SO4 \(\rightarrow\)Cr2(SO4)3 + 3H2O (2)
Đặt nCuO=a
nCr2O3=b
Ta có :
\(\left\{{}\begin{matrix}80a+152b=69,2\\160a+392b=169,2\end{matrix}\right.\)
=>a=0,2;b=0,35
mCuO=80.0,2=16(g)
mCr2O3=69,2-16=53,2(g)
b;Theo PTHH 1 và 2 ta có:
nCuO=nH2SO4=0,2(mol)
3nCr2O3=nH2SO4=1,05(mol)
nCuO=nCuSO4=0,2(mol)
nCr2O3=nCr2(SO4)3=0,35(mol)
mH2SO4=(1,05+0,2).98=122,5(g)
mdd H2SO4=122,5:\(\dfrac{1,96}{100}=6250\left(g\right)\)
mCuSO4=0,2.160=32(g)
mCr2(SO4)3=392.0,35=137,2(g)
C% dd CuSO4=\(\dfrac{32}{6250+69,2}.100\%=0,5\%\)
C% dd Cr2(SO4)3=\(\dfrac{137,2}{6250+69,2}.100\%=2,17\%\)

https://hoc24.vn/hoi-dap/question/71825.html bạn vào đây tham khảo nè

Ta có : Độ rượu=
(Vrượu nguyên chất (ml) /Vrượu nguyênchất(ml)+Vnước(ml) )*100%
=> Độ rượu = \(\dfrac{30}{30+90}\cdot100\) = 25 độ
Chúc bạn học tốt


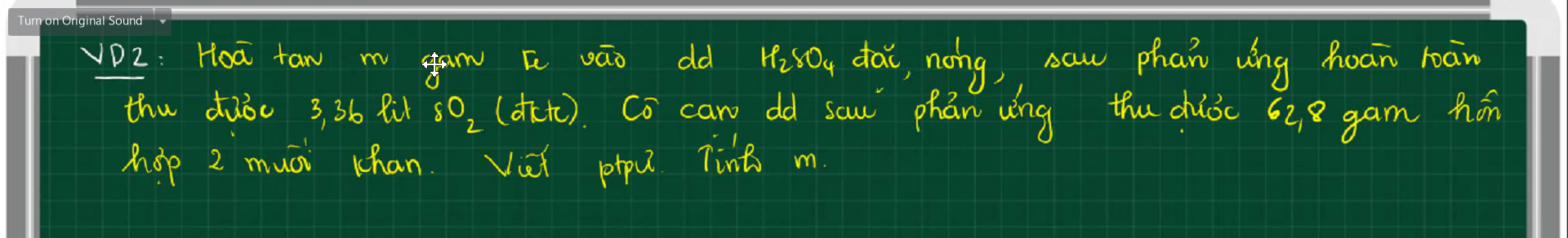



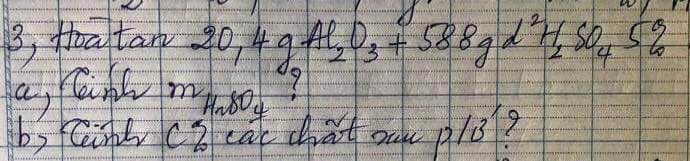
Bài 4 :
\(n_{H2}=\dfrac{V_{H2}}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Pt : \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
0,1 0,15 0,05 0,15
a) \(n_{Al}=\dfrac{0,15.2}{3}=0,1\left(mol\right)\)
⇒ \(m_{Al}=n_{Al}.M_{Al}\)
= 0,1 . 27
= 2,7 (g)
\(m_{Cu}=10-2,7=7,3\left(g\right)\)
0/0Al = \(\dfrac{m_{Al}.100}{m_{hh}}=\dfrac{2,7.100}{10}=27\)0/0
0/0Cu = \(\dfrac{m_{Cu}.100}{m_{hh}}=\dfrac{7,3.100}{10}=13\)0/0
b) \(n_{Al2\left(SO4\right)3}=\dfrac{0,15.1}{3}=0,05\left(mol\right)\)
⇒ \(m_{Al2\left(SO4\right)3}=n_{Al2\left(SO4\right)3.}M_{Al2\left(SO4\right)3}\)
= 0,05 . 342
= 17,1 (g)
\(n_{H2SO4}=\dfrac{0,1.3}{2}=0,15\left(mol\right)\)
⇒ \(m_{H2SO4}=n_{H2SO4}.M_{H2SO4}\)
= 0,15 .98
= 14,7 (g)
\(C_{H2SO4}=\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\)\(\dfrac{14,7.100}{15}=98\left(g\right)\)
mdung dịch sau phản ứng = (mAl + mCu) + mH2SO4 - mH2
= 10 + 98 - (0,15 . 2)
=107,7 (g)
\(C_{Al2\left(SO4\right)3}=\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{17,1.100}{107,7}=15,88\)0/0
Chúc bạn học tốt
Mình xin lỗi bạn nhé , bạn sửa kết quả : phần trăm của của đồng '130/0' thành ' 730/0' giúp mình