Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Hiện tượng: Đường kính hoặc bột gạo hay bột mì dần dần hoá thành chất rắn màu đen, sau đó trong cốc sủi bọt đẩy chất rắn màu đen trào ra ngoài cốc.
- Giải thích: Các hợp chất đường kính, bột gạo hay bột mì,… (công thức tổng quát có dạng Cn(H2O)m) bị sulfuric acid đặc hút nước tạo ra chất rắn màu đen là carbon. Một phần carbon sinh ra tiếp tục bị oxi hoá bởi sulfuric acid tạo thành khí CO2 và SO2 , đẩy carbon trào ra ngoài cốc.
- Phương trình hóa học:
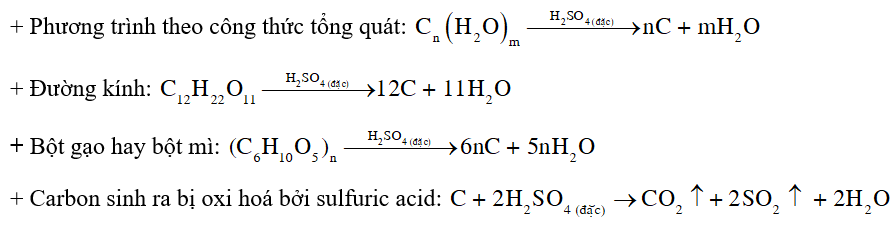

Đường kính dần dần hoá thành chất rắn màu đen, sau đó trong cốc sủi bọt đẩy chất rắn màu đen trào ra ngoài cốc.

1:
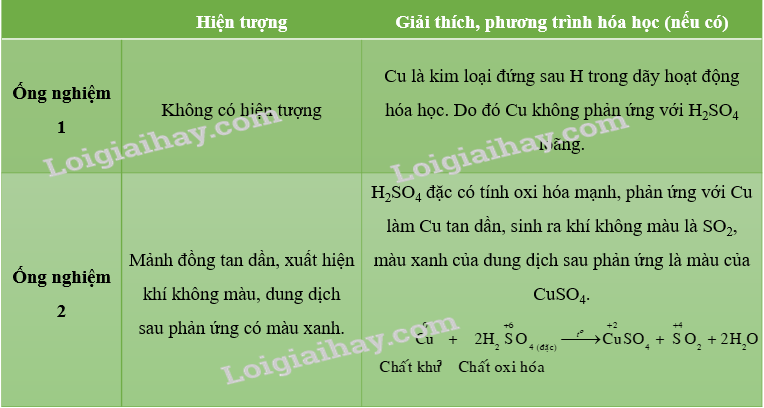
\(Cu+2H_2SO_4\left(đặc\right)\rightarrow CuSO_4+SO_2+2H_2O\)
Chất oxi hóa: H2SO4
Chất khử: Cu
2: Dung dịch H2SO4 đặc có tính oxi hóa mạnh, có thể oxi hóa kim loại hoạt động kém như đồng

- Trong Thí nghiệm 1, chất lỏng xuất hiện ở đáy cốc không phải là benzene (benzene không màu).
- Vì benzene phản ứng với dung dịch nitric acid tạo nitrobenzene có màu vàng nhạt .
PTHH: C6H6 + HNO3 → C6H5NO2 + H2O

CH3CH2CH2OH \(\underrightarrow{H_2SO_{4đ}}\) CH3CH=CH2 + H2O
CH3CH(OH)CH3 \(\underrightarrow{H_2SO_{4đ}}\) CH3CH=CH2 + H2O
=> alkene sinh ra khi đun propan-1-ol và propan-2-ol với dung dịch sulfuric acid đặc ở nhiệt độ thích hợp đều là CH3CH=CH2.

Thí nghiệm 1:
Khí sinh ra làm mất màu dung dịch bromine/thuốc tím.

CH2=CH2 + Br2 → CH2Br–CH2Br
3CH2=CH2 + 4H2O + 2KMnO4 → 3HO–CH2–CH2–OH + 2MnO2 + 2KOH

- Tính chất của sulfuric acid loãng:
Dung dịch sulfuric acid loãng có đầy đủ tính chất của một acid mạnh:
+ Đổi màu quỳ tím thành đỏ.
+ Tác dụng với kim loại hoạt động trong dãy hoạt động hoá học.
+ Tác dụng với basic oxide và base.
+ Tác dụng với nhiều muối.
- Tính chất của sulfuric acid đặc: Ngoài tính acid, dung dịch sulfuric acid đặc còn có tính oxi hoá và tính háo nước.
- Cách bảo quản sulfuric acid:
+ Sulfuric acid được bảo quản trong chai, lọ có nút đậy chặt, đặt ở vị trí chắc chắn.
+ Đặt chai, lọ đựng dung dịch sulfuric acid đặc tránh xa các lọ chứa chất dễ gây cháy, nổ như chlorate, perchlorate, permanganate, dichromate.
- Cách sử dụng sulfuric acid để đảm bảo an toàn:
Sulfuric acid gây bỏng khi rơi vào da, do vậy cần tuân thủ các nguyên tắc:
(1) Sử dụng găng tay, đeo kính bảo hộ, mặc áo thí nghiệm.
(2) Cầm dụng cụ chắc chắn, thao tác cẩn thận.
(3) Không tì, đè chai đựng acid lên miệng cốc, ống đong khi rót acid.
(4) Sử dụng lượng acid vừa phải, lượng acid còn thừa phải thu hồi vào lọ đựng.
(5) Không được đổ nước vào dung dịch acid đặc.
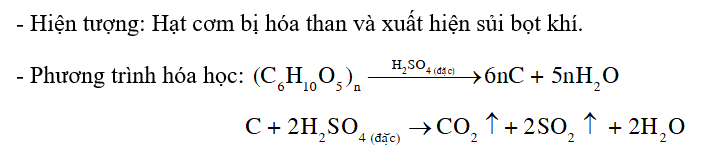

Hiện tượng: Đường mía dần dần hoá than, có hiện tượng sủi bọt đẩy cacbon trào ra ngoài cốc
1:
\(C_{12}H_{22}O_{11}\rightarrow12C+11H_2O\)
\(C+2H_2SO_4\left(đặc\right)\rightarrow CO_2+2SO_2+H_2O\)
2: Dự đoán: cellulose và tinh bột sẽ hóa đen bởi vì H2SO4 đặc có khả năng hút nước