Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
\(n_{HCl}=1.0,18=0,18(mol)\\ 4M+3O_2\xrightarrow{t^o}2M_2O_3\\ M_2O_3+6HCl\to 2MCl_3+3H_2O\\ \Rightarrow n_{M_2O_3}=0,03(mol)\\ \Rightarrow n_M=0,06(mol)\\ \Rightarrow M_M=\dfrac{1,62}{0,06}=27(g/mol)(Al)\\ \Rightarrow B\)
Câu 2:
\(n_{Al}=\dfrac{5,4}{27}=0,2(mol);n_{H_2SO_4}=0,3.0,1=0,03(mol)\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ LTL:\dfrac{0,2}{1}>\dfrac{0,03}{3}\Rightarrow Al\text{ dư}\\ \Rightarrow n_{H_2}=0,03(mol)\Rightarrow V_{H_2}=0,03.22,4=0,672(l)\\ n_{Al_2(SO_4)_3}=0,01(mol)\Rightarrow C_{M_{Al_2(SO_4)_3}}=\dfrac{0,01}{0,1}=0,1M\)
Chọn D

Ca(OH)2 + SO2 -------> CaSO3 + H2O
\(n_{CaSO_3}=n_{SO_2}=0,2\left(mol\right)\)
Z + 2H2SO4 --------> ZSO4 + SO2 + 2H2O
Ta có : \(n_Z=n_{SO2}=0,2\left(mol\right)\)
=> MZ= \(\dfrac{12,8}{0,2}=64\left(Cu\right)\)
=> Chọn C
\(2Z+2nH_2SO_4 \buildrel{{t^o}}\over\longrightarrow Z_2(SO_4)_n+nSO_2+2H_2O\\ Ca(OH)_2+SO_2 \to CaSO_3+H_2O\\ n_{CaSO_3}=\frac{24}{120}=0,2(mol)\\ n_{CaSO_3}=n_{SO_2}=0,2(mol)\\ n_Z=\frac{2}{n}.n_{SO_2}=\frac{2}{n}.0,2=\frac{0,4}{n}(mol)\\ M_Z=\frac{12,8n}{0,4}=32n (g/mol)\\ n=2; Z=64 (Cu)\\ \to C\)

Gọi 2 kim loại cần tìm là: A và B
PTHH: A + H2SO4 → ASO4 + H2
B + H2SO4 → BSO4 + H2
(Gọi a là số mol của cả 2 kim loại A , B vì 2 kim loại có số mol bằng nhau.)
Tổng số mol của hiđrô là: 1,12 : 22,4 = 0,05(mol)
=> Số mol hiđrô ở pt (1) = số mol hiđrô ở pt (2) = 0,05 / 2 = 0,025 (mol)
=> Số mol của A = Số mol của B = 0,025
=> 0,25 ( MA + MB ) = 2(gam)
=> MA + MB = 80
Mà trong các kim loại nói trên chỉ có 2 kim loại là Mg và Fe thoả mãn điều kiện (vì 56 + 24 = 80)
=> 2 kim lại đó là Mg vad Fe

1) Gọi công thức của oxit là AO. Số mol HCl là 0,4.1=0,4 (mol).
AO (0,2 mol) + 2HCl (0,4 mol) \(\rightarrow\) ACl2 + H2\(\uparrow\).
Phân tử khối của oxit là 8,0/0,2=40 (g/mol).
Vậy A là magie (Mg) và công thức hóa học của oxit là MgO.
2) Số mol MgCO3 và H2SO4 lần lượt là 8,4/84=0,1 (mol) và 0,5.1=0,5 (mol).
Các chất tan trong dung dịch sau phản ứng gồm MgSO4 (0,1 mol) và H2SO4 dư (0,4 mol) có nồng độ mol lần lượt là 0,1/0,5=0,2 (M) và 0,4/0,5=0,8 (M).
\(1,n_{HCl}=0,4.1=0,4\left(mol\right)\\ PTHH:AO+2HCl\rightarrow ACl_2+H_2O\\ Mol:0,2\leftarrow0,4\\ M_{AO}=\dfrac{8}{0,2}=40\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow A+16=40\\ \Leftrightarrow A=24\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow A.là.Mg\\ CTHH:MgO\)
\(2,n_{H_2SO_4}=1.0,5=0,5\left(mol\right)\\ PTHH:MgCO_3+H_2SO_4\rightarrow MgSO_4+CO_2\uparrow+H_2O\\ Mol:0,5\leftarrow0,5\rightarrow0,5\\ C_{M\left(MgSO_4\right)}=\dfrac{0,5}{0,5}=1M\)

R + Cl2 → RCl2
R + 2HCl → RCl2 + H2
nHCl = 0,2.1 = 0,2 mol => nR = 0,2/2 = 0,1 mol
Mà nRCl2 = nR
=> MRCl2 = \(\dfrac{13,6}{0,1}\)= 136 (g/mol) => MR = 136 - 35,5.2 = 64 g/mol
Vậy R là kim loại đồng (Cu)
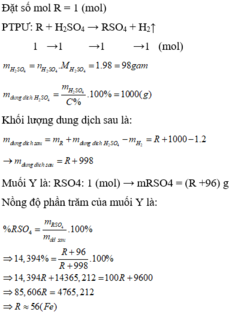
\(R+H_2SO_4\rightarrow RSO_4+H_2\\ n_R=n_{H_2SO_4}=0,2.1=0,2\left(mol\right)\\ M_R=\dfrac{12,8}{0,2}=64\left(\dfrac{g}{mol}\right)\)
Thật ra nó hơi vô lí vì anh thấy 200ml dd H2SO4 là dung dịch loãng, PT như trên, tính ra đồng mà đồng không tác dụng axit sunfuric loãng. Em hỏi lại cô đề bài nha :D