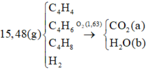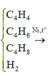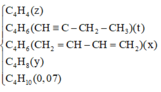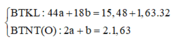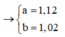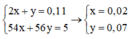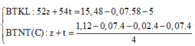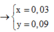Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_C=n_{CO_2}=n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
\(n_{N_2}=\dfrac{9,632}{22,4}=0,43\left(mol\right)\)
Gọi: \(\left\{{}\begin{matrix}n_{O_2\left(pư\right)}=0,2a\left(mol\right)\Rightarrow n_{N_2\left(trongkk\right)}=0,8a\left(mol\right)\\n_{H_2O}=b\left(mol\right)\Rightarrow n_H=2b\left(mol\right)\end{matrix}\right.\)
BTNT O, có: \(2n_{O_2\left(pư\right)}=2n_{CO_2}+n_{H_2O}\)
⇒ 0,2a.2 = 0,06.2 + b (1)
Ta có: \(n_{N\left(trongY\right)}=\left(n_{N_2}-n_{N_2\left(trongkk\right)}\right).2=\left(0,43-0,8a\right).2\)
Có: mY = mC + mH + mN
⇒ 1,18 = 0,06.12 + 2b.1 + (0,43 - 0,8a).2.14 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,525\left(mol\right)\\b=0,09\left(mol\right)\end{matrix}\right.\)
⇒ x:y:z = 0,06:0,18:0,02 = 3:9:1
→ CTPT của Y có dạng (C3H9N)n.
Theo đề: Y có CTPT là CxHyN.
→ n = 1
Vậy: Y có CTPT là C3H9N.

Khi dẫn sản phẩm vào Ca(OH)2 dư thì:
nCO2 = nCaCO3 = 6/100 = 0,06 mol
Đặt nB = a và nH2O = b mol
+ Bảo toàn N → nN2(do B) = 1/2.nB = 0,5a (mol)
+ Bảo toàn O → nO2 = (2nCO2 + nH2O)/2 = (2.0,06+b)/2 = 0,06 + 0,5b (mol)
Mà không khí có 20% O2 và 80% N2 về thể tích
→ nN2(kk) = 4.nO2 = 0,24 + 2b (mol)
→ nN2 bay ra = 0,5a + 0,24 + 2b (mol)
Lập hệ pt:
+) nN2 bay ra = 0,5a + 2b + 0,24 = 9,632/22,4 (1)
+) Bảo toàn nguyên tố C, H, N tính được số mol các nguyên tố:
nC = nCO2 = 0,06 mol
nH = 2nH2O = 2b mol
nN = nB = a mol
Mà mB = mC + mH + mN → 1,18 = 0,06.12 + 2b + 14a (2)
Giải (1) (2) được a = 0,02 và b = 0,09
→ nC : nH : nN = 0,06 : 0,18 : 0,02 = 3 : 9 : 1
Vậy CTPT của B là C3H9N

quy đổi hh thành fe,cu,s : 56x+64y+32z=6,48 (1)
Fe--->fe+3+3e
cu--->cu+2+2e
s--->s+4+4e
o2+4e---->2o2-
bte:3x+2y+0,28=0,45 (2)
giải 12--->x=0,03 ,y=0,04
phần :2 fe--->fe+3+3e
cu---->cu+2+2e
n+5+1e--->
s--->s+6
<=>0,03.3+0,04.2+0,07.6=nNO2====>v=13,216 l
ket tủa có :Fe(oH)3=nFe;cu(oh)2=nCu;BaSO4=nS--->m=23,44g